Активные ингредиенты: лидокаин.
Versatis 5% лечебный пластырь
Почему используется Версатис? Для чего это?
Versatis содержит лидокаин, местный анальгетик, уменьшающий боль в коже. Вам прописали его для лечения боли, вызванной постгерпетической невралгией. Это состояние обычно характеризуется локализованными симптомами, такими как жжение, колющая или колющая боль.
Противопоказания Когда нельзя использовать Версатис
Не используйте Versatis
- если у вас аллергия на лидокаин или какие-либо другие ингредиенты этого лекарства (перечислены в разделе 6)
- если у вас была аллергическая реакция на другие лидокаиноподобные продукты, такие как бупивакаин, этидокаин, мепивакаин или прилокаин
- на сломанной коже или открытых ранах.
Меры предосторожности при использовании Что следует знать перед приемом Версатиса
Перед использованием Versatis проконсультируйтесь со своим врачом или фармацевтом. Если у вас тяжелое заболевание печени или серьезные проблемы с сердцем или почками, вам следует поговорить с врачом перед использованием Versatis. Versatis следует наносить на кожу после заживления повреждений опоясывающего лишая. Его нельзя наносить на глаза или рот или рядом с ними.
Лидокаин метаболизируется в печени до множества соединений. Одним из таких соединений является 2,6 ксилидин, который, как было показано, вызывает опухоли у крыс при постоянном приеме в очень высоких дозах. Значение этих данных для людей неизвестно.
Дети и подростки
Версатис не изучался у пациентов младше 18 лет, поэтому его применение не рекомендуется.
Взаимодействие Какие лекарства или продукты могут изменить действие Versatis
Сообщите своему врачу или фармацевту, если вы принимаете или недавно принимали или собираетесь принимать какие-либо другие лекарства.
Предупреждения Важно знать, что:
Беременность, кормление грудью и фертильность
Если вы беременны, подозреваете, что беременны или планируете родить ребенка, или если вы кормите грудью, перед применением этого лекарства проконсультируйтесь с врачом или фармацевтом. Версатис не следует использовать во время беременности, за исключением случаев, когда это явно необходимо. Нет исследований по применению пластыря в период грудного вскармливания. При использовании Versatis в крови может присутствовать только небольшое количество активного ингредиента, лидокаина. Воздействие на детей, находящихся на грудном вскармливании, маловероятно.
Вождение и использование машин
Влияние Versatis на способность управлять автомобилем или работать с механизмами маловероятно. Таким образом, с Versatis можно управлять автомобилем или работать с механизмами.
Versatis содержит пропиленгликоль, метилпарагидроксибензоат и пропилпарагидроксибензоат.
Пластыри содержат пропиленгликоль (E1520), который может вызвать раздражение кожи. Кроме того, они содержат метилпарагидроксибензоат (E218) и пропилпарагидроксибензоат (E216), которые могут вызывать аллергические реакции. Иногда аллергические реакции могут появиться после использования пластырей в течение определенного периода времени.
Доза, способ и время приема Как использовать Версатис: Дозировка
Всегда принимайте это лекарство точно так, как вам сказал врач. В случае сомнений проконсультируйтесь с врачом или фармацевтом. Обычно суточная доза составляет от одного до трех пятен размером с пораженный участок кожи. Versatis можно разрезать на более мелкие кусочки, чтобы покрыть пораженный участок. Вы не должны использовать более 3 патчей одновременно. Патчи необходимо удалить через 12 часов после нанесения; таким образом у вас будет 12 часов без пластыря. Вы можете выбрать, применять ли Versatis днем или ночью. Как правило, вы почувствуете некоторое облегчение боли с первого дня использования, но может пройти до 2-4 недель, прежде чем обезболивающий эффект Versatis станет полным. Если по прошествии этого времени боль все еще будет очень сильной, сообщите об этом своему врачу, так как польза от лечения должна быть сопоставлена с потенциальными рисками (см. «Предупреждения и меры предосторожности»).
Ваш врач будет регулярно проверять, работает ли Versatis.
Перед нанесением Версатиса на пораженный участок
- если болезненный участок кожи покрыт волосами или волосами, его следует срезать ножницами, их нельзя сбривать.
- Кожа должна быть чистой и сухой.
- Кремы или лосьоны можно использовать на обработанной коже только в период, когда пластырь не применяется.
- Если вы только что приняли ванну или душ, перед нанесением пластыря подождите, пока кожа не остынет.
Применить патч
Шаг 1. Откройте пакет и удалите один или несколько пластырей.
- порвите или разрежьте конверт по пунктирной линии
- при использовании ножниц будьте осторожны, чтобы не повредить патчи.
- возьмите один или несколько пластырей, в зависимости от размера болезненного участка кожи
Шаг 2: закройте конверт
- плотно закройте пакет после использования
- пластырь содержит воду и может высохнуть, если пакет не закрыт должным образом
Шаг 3: При необходимости отрежьте пластырь.
- при необходимости перед снятием пленки отрежьте пластырь до размера, необходимого для покрытия болезненного участка кожи.
Шаг 4: Снимите пленку
- снимите прозрачную пленку с патча
- старайтесь не касаться липкой части пластыря
Шаг 5: Нанесите пластырь и плотно прижмите к коже.
- нанести до трех пластырей на болезненный участок кожи
- прижать пластырь к коже
- нажмите и удерживайте пластырь не менее 10 секунд, чтобы пластырь хорошо прилегал к коже
- убедитесь, что весь пластырь, включая края, прилегает к коже.
Оставьте пластырь только на 12 часов
Важно, чтобы Versatis наносился на кожу только на 12 часов. Например, если ночью вы чувствуете сильную боль, вы можете наложить пластырь в 19:00 и удалить его в 7:00. Если вы чувствуете сильную боль в течение дня, вы можете нанести Versatis в 7 часов утра и снять его в 7 часов вечера.
Ванна, душ и плавание
Так как следует избегать контакта Versatis с водой, любые ванны, душ или плавание можно делать в то время, когда пластырь не наложен.После купания или душа необходимо дать коже остыть перед нанесением.Нанесите пластырь.
Если пластырь отвалится
Очень редко пластырь может отслоиться или плохо держаться. Если это так, попробуйте снова прикрепить его к той же области. Если он не прилипает, удалите его полностью и нанесите новый патч, всегда на тот же участок.
Как удалить Версатис
Чтобы сменить патч, медленно снимите старый патч. Если он не снимается легко, вы можете намочить его в горячей воде в течение нескольких минут, прежде чем снимать.
Передозировка Что делать, если вы приняли слишком много Версатиса
Если вы забыли удалить пластырь через 12 часов
Снимите пластырь, как только вспомните. Новый пластырь можно наносить через 12 часов.
Если вы используете больше патчей, чем предусмотрено
Если вы используете больше пластырей, чем вам нужно, или держите их слишком долго, риск побочных эффектов может возрасти.
Если вы забыли нанести Версатис
Если вы забыли применить новый патч после 12-часового перерыва без предыдущего патча, примените новый патч, как только вспомните.
Если у вас есть дополнительные вопросы по применению этого лекарства, обратитесь к врачу или фармацевту.
Побочные эффекты Каковы побочные эффекты Versatis
Как и все лекарства, это лекарство может вызывать побочные эффекты, хотя они возникают не у всех. Если при нанесении пластыря возникает раздражение или ощущение жжения, пластырь следует удалить.Не наносите другой пластырь на эту область, пока раздражение не исчезнет.
Ниже перечислены очень распространенные побочные эффекты, которые могут возникать более чем у 1 из 10 человек.
К ним относятся изменения кожи в области наложения пластыря или рядом с ней и могут включать покраснение, сыпь, зуд, жжение, дерматит и волдыри.
Ниже перечислены редкие побочные эффекты, которыми может обладать до 1 человека из 100.
Изменения кожи и раны
Ниже перечислены очень редкие побочные эффекты, которыми может обладать 1 человек из 10 000.
Открытые раны, тяжелые аллергические реакции и аллергия.
Сообщение о побочных эффектах
Если вы заметили какие-либо побочные эффекты, обратитесь к врачу или фармацевту, включая любые возможные побочные эффекты, не указанные в данном информационном листке. Вы также можете сообщить о побочных эффектах напрямую через национальную систему отчетности по адресу http://www.agenziafarmaco.gov.it/it/responsabili. Сообщив о побочных эффектах, вы поможете получить больше информации о безопасности этого лекарства.
Срок действия и удержание
Храните это лекарство в недоступном для детей месте. Не используйте это лекарство после истечения срока годности, указанного на упаковке и картонной коробке после EXP. Срок годности относится к последнему дню этого месяца. Не храните в холодильнике или морозильной камере. После первого открытия осторожно закройте пакет. После вскрытия пакета пластыри необходимо использовать в течение 14 дней. Не используйте это лекарство, если вы заметили, что пакет поврежден. В таком случае пластырь может высохнуть и поэтому плохо держится.
Как удалить Версатис
Используемые пластыри все еще содержат активный ингредиент, который может быть опасен для окружающих. Сложите старые пластыри пополам липкой стороной внутрь и выбросьте их, чтобы они не были доступны для детей.
Не выбрасывайте лекарства в сточные воды или бытовые отходы. Спросите своего фармацевта, как утилизировать лекарства, которые вы больше не используете. Это поможет защитить окружающую среду.
Состав и лекарственная форма
Что содержит Версатис
- действующее вещество - лидокаин
- каждый пластырь размером 10 см x 14 см содержит 700 мг (5% масс.) лидокаина.
- другие компоненты пластыря (вспомогательные вещества): глицерин, жидкокристаллический сорбит, кармеллоза натрия, пропиленгликоль (E1520), мочевина, тяжелый каолин, винная кислота, желатин, поливиниловый спирт, глицинат алюминия, динатрий эдетат, метилпарагидроксибензоат (E218) , пропилпарагидроксибензоат (E216), полиакриловая кислота, полиакрилат натрия, очищенная вода.
Опорный слой и клеевой слой: полиэтилентерефталат (ПЭТ).
Описание внешнего вида Versatis и что содержится в упаковке
Лекарственные пластыри имеют длину 14 см и ширину 10 см. Они белые, из мягкого материала, с надписью «лидокаин 5%». Пластыри упакованы в закрывающиеся пакеты по 5 пластырей в каждом.
Каждая упаковка содержит 5, 10, 20, 25 или 30 пластырей, упакованных в 1, 2, 4, 5 или 6 пакетов соответственно.
Не все упаковки имеются в продаже.
Листовка с исходным кодом: AIFA (Итальянское агентство по лекарственным средствам). Контент опубликован в январе 2016 года. Представленная информация может быть устаревшей.
Чтобы иметь доступ к самой последней версии, рекомендуется зайти на сайт AIFA (Итальянское агентство по лекарственным средствам). Заявление об ограничении ответственности и полезная информация.
01.0 НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
VERSATIS 5% ЛЕКАРСТВЕННЫЙ ПАТЧ
02.0 КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ
Каждый пластырь размером 10 см x 14 см содержит 700 мг (5% масс.) Лидокаина (50 мг лидокаина / грамм адгезивной основы).
Вспомогательные вещества с известным эффектом:
Метилпарагидроксибензоат 14 мг
Пропилпарагидроксибензоат 7 мг
Пропиленгликоль 700 мг
Полный список вспомогательных веществ см. В разделе 6.1.
03.0 ФАРМАЦЕВТИЧЕСКАЯ ФОРМА
Лечебный пластырь
Белый гидрогелевый пластырь, содержащий клейкий материал, нанесенный на нетканую основу из полиэтилентерефталата с тисненой надписью «Лидокаин 5%» и покрыт защитной пленкой из полиэтилентерефталата.
04.0 КЛИНИЧЕСКАЯ ИНФОРМАЦИЯ
04.1 Терапевтические показания
Versatis показан для симптоматического лечения нейропатической боли, связанной с перенесенной инфекцией Herpes Zoster (постгерпетическая невралгия, NPH), у взрослых.
04.2 Дозировка и способ применения
Взрослые и пожилые
На болезненный участок необходимо накрыть пластырь, наносимый один раз в день не более чем на 12 часов в течение 24 часов. Следует применять только пластыри, необходимые для эффективного лечения. При необходимости пластырь можно разрезать ножницами на более мелкие части перед снятием защитной пленки. В общей сложности одновременно следует накладывать не более трех патчей.
Пластырь следует наносить на неповрежденную, сухую и не раздраженную кожу (после заживления герпетических образований).
Каждый пластырь нельзя применять более 12 часов. Свободный перерыв от следующего применения должен составлять не менее 12 ч. Пластырь можно накладывать днем или ночью.
Пластырь следует наносить на кожу сразу после извлечения его из мешочка и снятия защитной пленки с поверхности гидрогеля. Волосы и волосы в области нанесения необходимо подстригать ножницами (не сбривать).
Через 2-4 недели лечение следует пересмотреть. Если после этого периода терапевтического ответа на Versatis не было (во время применения пластыря и / или периода без пластыря, лечение следует прекратить, так как в этой ситуации потенциальные риски могут превысить пользу (см. Разделы 4.4 и 5.1). Длительное использование Versatis в клинических испытаниях показало, что количество используемых пластырей со временем уменьшается. Следовательно, лечение следует пересматривать через регулярные промежутки времени, чтобы решить, нужно ли количество пластырей, необходимых для покрытия болезненной области. можно уменьшить или можно увеличить свободный интервал между нанесением пластыря.
Почечная недостаточность
У пациентов с почечной недостаточностью легкой или средней степени тяжести коррекции дозировки не требуется. Версатис следует применять с осторожностью у пациентов с тяжелой почечной недостаточностью (см. Раздел 4.4).
Печеночная недостаточность
У пациентов с легким или умеренным нарушением функции печени коррекции дозировки не требуется. Версатис следует применять с осторожностью у пациентов с тяжелой печеночной недостаточностью (см. Раздел 4.4).
Педиатрическая популяция
Безопасность и эффективность Versatis у пациентов младше 18 лет не установлены. Нет данных.
04.3 Противопоказания
Повышенная чувствительность к действующему веществу или любому из вспомогательных веществ, перечисленных в разделе 6.1. Пластырь также противопоказан пациентам с известной гиперчувствительностью к другим местным анестетикам амидного типа, таким как бупивакаин, этидокаин, мепивакаин и прилокаин.
Пластырь нельзя наносить на воспаленную или поврежденную кожу, например, на активные очаги опоясывающего лишая, атопический дерматит, раны.
04.4 Особые предупреждения и соответствующие меры предосторожности при использовании
Пластырь нельзя наносить на слизистые оболочки. Следует избегать попадания пластыря в глаза.
Пластырь содержит пропиленгликоль, который может вызвать раздражение кожи. Он также содержит метилпарагидроксибензоат и пропилпарагидроксибензоат, которые могут вызывать аллергические реакции (даже с задержкой).
Пластырь следует с осторожностью применять пациентам с тяжелым поражением сердца, почек или печени.
Было обнаружено, что один из метаболитов лидокаина, 2,6-ксилидин, обладает генотоксическим и канцерогенным действием у крыс (см. Раздел 5.3). Показано, что вторичные метаболиты обладают мутагенным действием. Клиническое значение этого открытия неизвестно. Следовательно, длительное лечение Versatis оправдано только реальной терапевтической пользой для пациента (см. Раздел 4.2).
04.5 Взаимодействие с другими лекарственными средствами и другие формы взаимодействия
На данный момент исследований взаимодействия нет. В клинических испытаниях пластыря не сообщалось о клинически значимых взаимодействиях.
Поскольку максимальные концентрации лидокаина в плазме, наблюдаемые в клинических исследованиях с пластырем, были низкими (см. Раздел 5.2), клинически значимые фармакокинетические взаимодействия маловероятны.
Хотя обычно абсорбция лидокаина через кожу низкая, пластырь следует использовать с осторожностью у пациентов, получающих антиаритмические средства I класса (например, токаинид, мексилетин) или другие местные анестетики, поскольку нельзя исключить риск системного дополнительного эффекта.
04.6 Беременность и кормление грудью
Беременность
Лидокаин проходит через плацентарный барьер. Однако данных о применении лидокаина беременными женщинами недостаточно.
Исследования на животных не указывают на тератогенный потенциал лидокаина. (см. пункт 5.3).
Потенциальный риск для людей неизвестен, поэтому Версатис не следует использовать во время беременности, если нет четких указаний.
Грудное вскармливание
Лидокаин выделяется с грудным молоком. Однако в отношении пластыря нет клинических исследований у кормящих женщин. Поскольку метаболизм лидокаина относительно быстрый и почти полностью происходит в печени, предполагается, что только очень небольшое количество лидокаина может выделяться с грудным молоком.
Плодородие
Клинических данных о фертильности нет. Исследования на животных не показали влияния на женскую фертильность.
04.7 Влияние на способность управлять автомобилем и работать с механизмами
Исследования влияния на способность управлять автомобилем или работать с механизмами не проводились. Поскольку системная абсорбция минимальна (раздел 5.2), влияние на способность управлять автомобилем или работать с механизмами маловероятно.
04.8 Побочные эффекты
О следующих нежелательных эффектах сообщают в порядке убывания их серьезности в каждой частотной группе.
Примерно у 16% пациентов, получающих лечение, могут возникать побочные реакции. Это местные реакции, обусловленные особенностями препарата.
Наиболее частыми побочными реакциями были реакции в месте нанесения (например, ощущение жжения, дерматит, эритема, зуд, сыпь, раздражение кожи и волдыри).
В таблице ниже перечислены побочные реакции, о которых сообщили пациенты, которые использовали пластырь в исследованиях постгерпетической невралгии. Они перечислены по классам и частоте в различных устройствах. Их частота определяется как: очень часто ≥ 1/10; общий ≥ 1/100 до
У пациентов, которые использовали пластырь в постмаркетинговых условиях, наблюдались следующие реакции.
Все побочные реакции, как правило, были легкой или умеренной интенсивности. Менее 5% из них привели к прекращению лечения.
При правильном использовании пластыря системные побочные реакции маловероятны, поскольку системная концентрация лидокаина очень низкая (см. Раздел 5.2). Системные побочные реакции на лидокаин аналогичны тем, которые наблюдаются при применении других амидов, используемых в качестве местных анестетиков (см. Раздел 4.9).
Сообщение о предполагаемых побочных реакциях
Сообщение о предполагаемых побочных реакциях, возникающих после получения разрешения на лекарственный препарат, важно, поскольку оно позволяет осуществлять непрерывный мониторинг баланса пользы / риска лекарственного средства. Медицинских работников просят сообщать о любых предполагаемых побочных реакциях через национальную систему отчетности ". Итальянское агентство по лекарственным средствам Сайт: http://www.agenziafarmaco.gov.it/it/responsabili
04.9 Передозировка
Передозировка пластырем маловероятна, но нельзя исключить, что неправильное использование пластыря, такое как одновременное использование большого количества пластырей, в течение более длительного периода применения или использования на поврежденной коже, может привести к более высокому, чем обычно, плазме. уровни лидокаина. Возможные признаки системной токсичности аналогичны тем, которые наблюдаются после введения лидокаина в качестве местного анестетика, и могут включать следующие признаки и симптомы: головокружение, рвоту, сонливость, судороги, мидриаз, брадикардию, аритмию и шок.
Кроме того, известные взаимодействия между системными концентрациями лидокаина с бета-блокаторами, ингибиторами CYP3A4 (например, производными имидазола, макролидами) и антиаритмическими препаратами могут стать актуальными в случае передозировки.
При подозрении на передозировку пластырь следует удалить и при необходимости принять поддерживающие меры. Противоядия от лидокаина нет.
05.0 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
05.1 Фармакодинамические свойства
Фармакотерапевтическая группа: местные анестетики, амиды.
Код УВД: N01BB02
Механизм действия
Versatis обладает двойным механизмом действия: фармакологической активностью лидокаина и механическим действием гидрогелевого пластыря, защищающего гиперчувствительную область.
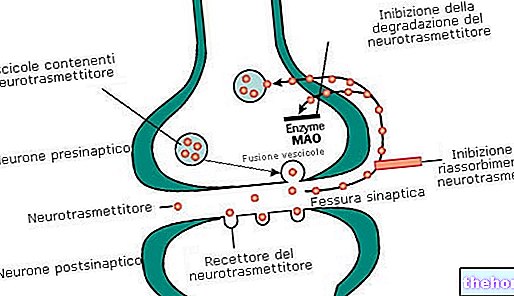
Лидокаин, содержащийся в пластырях Versatis, непрерывно распространяется по коже, оказывая местное обезболивающее. Механизм действия связан со стабилизацией мембран нейронов, которая, как полагают, определяет один понижающее регулирование натриевых каналов и, следовательно, уменьшение боли.
Клиническая эффективность
Обезболивание при НПХ затруднено. Имеются данные об эффективности Versatis в облегчении симптомов аллодинамического компонента НПХ в некоторых случаях (см. Раздел 4.2).
Эффективность Versatis была продемонстрирована в исследованиях постгерпетической невралгии.
Для оценки эффективности пластырей, содержащих 5% лидокаин, были проведены два основных контролируемых исследования.
В первом исследовании пациенты были набраны из уже известной популяции "ответчикЭто было перекрестное исследование, которое включало 14 дней лечения пластырями, содержащими 5% лидокаин, с последующим приемом плацебо или наоборот. Основная цель заключалась в том, чтобы "время выходить", то есть время, когда пациенты вышли из исследования, потому что уменьшение боли было на 2 балла ниже, чем их обычная реакция по 6-балльной шкале (от ухудшения до полного снятия боли). Из 32 набранных пациентов 30 завершили исследование. В "время выходить" среднее значение для плацебо составляло 4 дня, а для активного препарата - 14 дней (p
Во втором исследовании 265 пациентов с постгерпетической невралгией были набраны для 8-недельного открытого курса лечения 5% -ным пластырем с лидокаином. В этом неконтролируемом исследовании примерно 50% пациентов ответили на лечение снижением по крайней мере на четыре балла по 6-балльной шкале (от ухудшения до полного облегчения). В общей сложности 71 пациент был рандомизирован для получения плацебо или пластырей с 5% лидокаином в течение 2-14 дней. Первичная конечная точка была определена как отсутствие эффективности в течение 2 дней подряд, поскольку уменьшение боли было на два пункта ниже, чем нормальный ответ по шестибалльной шкале (от ухудшения до полной ремиссии), что привело к прекращению лечения. Прекращение лечения произошло из-за неэффективности у 9 из 36 пациентов, получавших препарат, и у 16 из 35 пациентов, получавших плацебо.
Последующий анализ второго исследования показал, что первоначальный ответ не зависел от продолжительности ранее существовавшего состояния НПХ.Однако тот факт, что пациенты с более длительным НПХ (> 12 месяцев) получают наибольшую пользу от активного лечения, подтверждается выводом о том, что эта группа пациентов чаще выбывала из исследования из-за неэффективности при переходе на лечение плацебо во время фазы двойного слепого исследования. .
В открытом контролируемом исследовании Versatis показал «сопоставимую эффективность с прегабалином у 98 пациентов с PHN с благоприятным профилем безопасности».
05.2 «Фармакокинетические свойства.
Абсорбция
Когда пластырь с 5% лидокаином используется в пределах рекомендованной максимальной дозы (3 пластыря одновременно накладываются в течение 12 часов), примерно 3 ± 2% от общей нанесенной дозы лидокаина доступно для системного применения как для однократного, так и для многократного введения.
Популяционный кинетический анализ, проведенный во время исследований клинической эффективности у пациентов с НПХ, продемонстрировал среднюю максимальную концентрацию лидокаина 45 нг / мл после одновременного применения 3 пластырей, 12 часов в день, повторенных в течение одного года. Это значение согласуется с данными фармакокинетических исследований. у пациентов с НПХ (52 нг / мл) и у здоровых добровольцев (85 нг / мл и 125 нг / мл).
Не было тенденции к накоплению лидокаина и его метаболитов MEGX, GX и 2,6 ксилидина; концентрации при устойчивое состояние они достигаются в первые 4 дня.
Кинетический анализ популяции показал, что системное воздействие показывает пропорционально меньшее увеличение, чем количество накладываемых одновременно пластырей, когда их количество увеличивается с 1 до 3.
Распределение
После внутривенного введения лидокаина здоровым добровольцам объем распределения составил 1,3 ± 0,4 л / кг (среднее значение ± стандартное отклонение, n = 15). Объем распределения не зависит от возраста, он уменьшается у пациентов с застойной болезнью сердца и увеличивается у пациентов с заболеванием печени. При концентрациях в плазме, определяемых наложением пластыря, примерно 70% лидокаина связывается с белками плазмы.Лидокаин проникает через плацентарный и гематоэнцефалический барьер, вероятно, путем пассивной диффузии.
Биотрансформация
Лидокаин быстро метаболизируется в печени до ряда метаболитов. Основным метаболическим путем лидокаина является N-деалкилирование до моноэтилглицинксилидида (MEGX) и глицинксилидида (GX), оба из которых менее активны, чем лидокаин, и доступны в низких концентрациях. Эти метаболиты гидролизуются до 2,6-ксилидина, который путем конъюгации превращается в 4-гидрокси-2,6-ксилидин.
Фармакологическая активность метаболита 2,6-ксилидина неизвестна, но он показывает канцерогенный потенциал у крыс (см. Раздел 5.3). Популяционный кинетический анализ выявил среднюю максимальную концентрацию 2,6-ксилидина 9 нг / мл после ежедневного повторения. заявки до 1 года. Это открытие подтверждено фармакокинетическим исследованием фазы I. Данные о метаболизме лидокаина в коже отсутствуют.
Устранение
Лидокаин и его метаболиты выводятся почками. Более 85% дозы выводится с мочой в виде метаболитов или активного вещества. Менее 10% дозы лидокаина выводится в неизмененном виде. Основной метаболит с мочой представляет собой конъюгат 4-гидрокси-2, 6-ксилидин, который составляет примерно 70-80% дозы, выводимой с мочой. У людей 2,6-ксилидин выводится с мочой в концентрациях менее 1% от дозы. Средний период полувыведения лидокаина после применения пластыря у здоровых добровольцев составляет 7,6 часа. Выведение лидокаина и его метаболитов может задерживаться в случае сердечной, почечной или печеночной недостаточности.
05.3 Доклинические данные по безопасности
Эффекты в доклинических исследованиях общей токсичности наблюдались только при дозах, которые, как считается, значительно превышают максимально достижимое воздействие на человека, что указывает на низкую клиническую значимость.
Лидокаина гидрохлорид не был генотоксичным в исследованиях. in vitro или in vivo. Его метаболит, образующийся при гидролизе, 2,6-ксилидин, показал генотоксическую активность в нескольких тестах, особенно после метаболической активации.
Исследования канцерогенности лидокаина не проводились. Исследования, проведенные для метаболита 2,6-ксилидина, смешанного с рационом самцов и самок крыс, показали связанную с лечением цитотоксичность: также наблюдались гиперплазия обонятельного эпителия носа, карциномы и аденомы в носовых полостях. на уровне печени и подкожно. Поскольку риск для человека неясен, следует избегать длительного лечения лидокаином.
Лидокаин не влиял на общую репродуктивную способность, фертильность самок или эмбрионально-плодное развитие / тератогенез у крыс, подвергшихся воздействию концентраций в плазме, в 50 раз превышающих наблюдаемые у пациентов. Исследования на животных относительно мужской фертильности, родов или послеродового развития не завершены.
06.0 ФАРМАЦЕВТИЧЕСКАЯ ИНФОРМАЦИЯ
06.1 Вспомогательные вещества
Самоклеящийся слой
Глицерин, жидкокристаллический сорбит, кармеллоза натрия, пропиленгликоль (E1520), мочевина, тяжелый каолин, винная кислота, желатин, поливиниловый спирт, глицинат алюминия, динатрий эдетат, метилпарагидроксибензоат (E218), пропилпарагидроксибензоат (E216), полиакриловая кислота, полиакриловая кислота полиакрилат, вода очищенная.
Служба поддержки
Полиэтилентерефталат (ПЭТ)
Фильм
Полиэтилентерефталат
06.2 Несовместимость
Не имеет значения.
06.3 Срок действия
3 года.
После вскрытия пакета пластырь необходимо использовать в течение 14 дней.
06.4 Особые меры предосторожности при хранении
Не охлаждайте и не замораживайте. После первого открытия держите пакет закрытым.
06.5 Характер непосредственной упаковки и содержимого упаковки
Закрывающиеся пакеты из метаакрилового сополимера бумага / полиэтилен / алюминий / этиленовая кислота, содержащие 5 пластырей.
Каждая упаковка содержит 5, 10, 20, 25 или 30 пластырей.
Не все размеры упаковки могут быть проданы.
06.6 Инструкции по эксплуатации и обращению
После использования пластырь по-прежнему содержит активный ингредиент. После его удаления пластырь следует сложить пополам клеевым слоем внутрь, чтобы самоклеящийся слой не открывался, и его следует выбросить.
Неиспользованный или выброшенный пластырь следует утилизировать в соответствии с местными правилами.
07.0 ДЕРЖАТЕЛЬ РАЗРЕШЕНИЯ НА МАРКЕТИНГ
ВЛАДЕЛЬЦА AIC: GRÜNENTHAL ITALIA S.r.l. via Carlo Bo 11 20143 Милан
08.0 НОМЕР РАЗРЕШЕНИЯ НА МАРКЕТИНГ
10 лечебных пластырей 5% AIC n. 040335022
30 лечебных пластырей 5% AIC n. 040335059
09.0 ДАТА ПЕРВОГО РАЗРЕШЕНИЯ ИЛИ ПРОДЛЕНИЯ РАЗРЕШЕНИЯ
Дата первой регистрации: март 2012 г.
Дата последнего обновления: 5.01.2012
10.0 ДАТА ПЕРЕСМОТРА ТЕКСТА
30 мая 2015 г.