Элементный анализ белков дает следующие средние значения: 55% углерода, 7% водорода и 16% азота; очевидно, что белки отличаются друг от друга, но их средний элементный состав мало отличается от значений, указанных выше. .
Конституционально белки представляют собой макромолекулы, образованные из природных α-аминокислот; аминокислоты соединяются посредством амидной связи, которая устанавливается в результате реакции между аминогруппой α-аминокислоты и карбоксилом другой α-аминокислоты.
Эта связь (-CO-NH-) также называется пептидной связью, поскольку она связывает пептиды (аминокислоты в комбинации):
полученный дипептид состоит из двух аминокислот. Поскольку дипептид содержит свободную аминогруппу на одном конце (NH2) и карбоксил на другом (COOH), он может реагировать с одной или несколькими аминокислотами и удлинять цепь как справа, так и слева, с той же реакцией. видно выше.
Последовательность реакций (которые, кстати, на самом деле не так просты) может продолжаться бесконечно: до тех пор, пока не появится полимер, называемый полипептид или белок. Различие между пептидами и белками связано с молекулярной массой: обычно для молекулярных масс выше 10 000 мы говорим о белках.
Связывание аминокислот вместе для получения даже небольших белков является сложной задачей, хотя недавно был разработан автоматический метод получения белков из аминокислот, который дает отличные результаты.
Таким образом, простейший белок состоит из двух аминокислот: по международному соглашению упорядоченная нумерация аминокислот в структуре белка начинается с аминокислоты со свободной α-аминогруппой.
кодирование этого белка), который сталкивается с немалыми химическими трудностями.
Посредством деградации по Эдману удалось определить упорядоченную последовательность аминокислот: белок реагирует с фенилизотиоцианатом (FITC); первоначально дублет азота α-амино атакует фенилизотиоцианат, образующий производное тиокарбамила; впоследствии полученный продукт циклизуется с образованием производного фенилтиогидантоина, которое является флуоресцентным.
Эдман изобрел машину, называемую секвенатором, которая автоматически регулирует параметры (время, реагенты, pH и т. Д.) Деградации и обеспечивает первичную структуру белков (за это он получил Нобелевскую премию).
Первичная структура недостаточна для полной интерпретации свойств белковых молекул; Считается, что эти свойства существенно зависят от пространственной конфигурации, которую белковые молекулы склонны принимать, складываясь различными способами: то есть, принимая то, что было определено как вторичная структура белков.
Вторичная структура белков мерцает, то есть имеет свойство разрушаться при нагревании; затем белки сами себя денатурируют, теряя многие из своих характерных свойств. Помимо нагревания выше 70 ° C, денатурация также может быть вызвана облучением или действием реагентов (например, сильных кислот).
Денатурация белков из-за теплового эффекта наблюдается, например, при нагревании яичного белка: видно, что он теряет студенистый вид и превращается в нерастворимое белое вещество. Однако денатурация белков приводит к разрушению их вторичной структуры, но оставляет их первичную структуру неизменной (конкатенация различных аминокислот).
Белки принимают третичную структуру, когда их цепь, хотя и гибкая, несмотря на изгиб вторичной структуры, складывается таким образом, что возникает искаженная трехмерная структура в форме твердого тела. За третичную структуру отвечают, прежде всего, дисульфидные связи, которые могут быть установлены между цистеином -SH, разбросанным по молекуле.
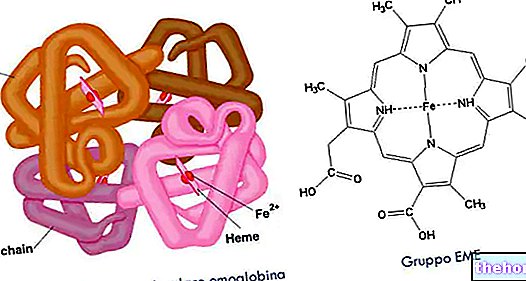
С другой стороны, четвертичная структура принадлежит только белкам, состоящим из двух или более субъединиц. Гемоглобин, например, состоит из двух пар белков (то есть во всех четырех белковых цепях), расположенных в вершинах тетраэдра так, чтобы образовалась сферическая структура; четыре белковые цепи удерживаются вместе ионными силами и нековалентные связи.
Другим примером четвертичной структуры является структура инсулина, которая, по-видимому, состоит из шести белковых субъединиц, расположенных парами в вершинах треугольника, в центре которого находятся два атома цинка.
Волокнистые белки
Это белки с определенной жесткостью и имеющие гораздо более длинную ось, чем другие; волокнистый белок, присутствующий в природе в больших количествах, является коллагеном (или коллагеном).
Волокнистый белок может иметь различные вторичные структуры: α-спираль, β-лист и, в случае коллагена, тройную спираль; α-спираль является наиболее стабильной структурой, за ней следует β-лист, а наименее стабильной из трех является тройная спираль.
Правильно если вслед за основным каркасом (ориентированным снизу вверх) выполняется движение, подобное завинчиванию правого винта; в то время как спираль из левая рука если движение аналогично завинчиванию левого винта. В правой α-спирали заместители -R аминокислот перпендикулярны основной оси белка и обращены наружу, а в левой - стороны a-спирали, заместители -R обращены внутрь. Правосторонние а-спирали более стабильны, чем левые, потому что между vati -R c "меньше взаимодействия и меньше стерических препятствий. Все а-спирали, обнаруженные в белках, правовращающие.
Структура α-спирали стабилизируется водородными связями (водородными мостиками), которые образуются между карбоксильной группой (-C = O) каждой аминокислоты и аминогруппой (-NH), обнаруженной на четыре остатка позже в линейная последовательность.
Примером белка, имеющего структуру α-спирали, является кератин волос.
За счет удлинения структуры α-спирали осуществляется переход от α-спирали к β-листу; также тепло или механическое напряжение позволяют перейти от α-спирали к β-листовой структуре.
Обычно в белке структуры β-листов близки друг к другу, потому что между частями самого белка могут быть установлены межцепочечные водородные связи.
В волокнистых белках большая часть белковой структуры организована в виде α-спирали или β-листа.
Глобулярные белки
Они имеют почти сферическую пространственную структуру (из-за многочисленных изменений направления полипептидной цепи); некоторые части бытия можно проследить до структуры α-спирали или β-листа, а другие части, напротив, не могут быть отнесены к этим формам: расположение не случайное, а организованное и повторяющееся.
Упомянутые до сих пор белки представляют собой вещества полностью гомогенного строения: то есть чистые последовательности объединенных аминокислот; такие белки говорят просто; Есть белки, состоящие из белковой части и небелковой части (группа простаты), называемых белками сопрягать.
, в ногтях, в роговице и хрусталике глаза, между интерстициальными пространствами некоторых органов (например, печени) и так далее.
Его структура дает ему особые механические возможности; он обладает большой механической прочностью, связанной с высокой эластичностью (например, в сухожилиях) или высокой жесткостью (например, в костях), в зависимости от выполняемой функции.
Одним из самых любопытных свойств коллагена является его конституционная простота: он состоит из примерно 30% пролина и примерно 30% глицина; остальные 18 аминокислот должны разделять только оставшиеся 40% структуры белка. Аминокислотная последовательность коллагена удивительно регулярна: из каждых трех остатков третьим является глицин.
Пролин - это циклическая аминокислота, в которой группа R связывается с α-аминогруппой азота, что придает ей определенную жесткость.
Конечная структура представляет собой повторяющуюся цепочку, имеющую форму «спирали»; внутри коллагеновой цепи водородные связи отсутствуют. Коллаген - это «левая спираль с шагом (длина, соответствующая одному витку спирали) больше, чем« α-спираль; спираль коллагена настолько рыхлая, что три белковые цепи могут обернуться вокруг друг друга, образуя » одинарная веревка: структура тройной спирали.
Однако тройная спираль коллагена менее стабильна, чем структура α-спирали и β-пластинки.
Давайте теперь посмотрим на механизм, с помощью которого производится коллаген; рассмотрим, например, разрыв кровеносного сосуда: этот разрыв сопровождается множеством сигналов с целью закрытия сосуда и образования тромба.
Для коагуляции требуется не менее тридцати специализированных ферментов. После образования сгустка необходимо продолжить восстановление ткани; клетки, расположенные близко к ране, также производят коллаген. Для этого сначала индуцируется экспрессия гена, то есть организмы, которые, исходя из информации о гене, способны продуцировать белок (генетическая информация транскрибируется на мРНК, которая покидает ядро и достигает рибосом в цитоплазма, где генетическая информация транслируется в белок). Затем коллаген синтезируется в рибосомах (он выглядит как левая спираль, состоящая примерно из 1200 аминокислот и имеющая молекулярную массу примерно 150 000 дн), а затем накапливается в просветах, где он становится субстратом для ферментов, способных выполнять посттрансляционные модификации (модификации языка, переведенные как «мРНК»); в коллагене эти модификации заключаются в гидроксилировании некоторых боковых цепей, особенно пролина и лизина.
Недостаток ферментов, вызывающих эти изменения, вызывает цингу: это заболевание, которое изначально вызывает разрыв кровеносных сосудов, ломку зубов, что может сопровождаться межкишечными кровотечениями и смертью; это может быть вызвано постоянным употреблением продуктов с длительным сроком хранения.
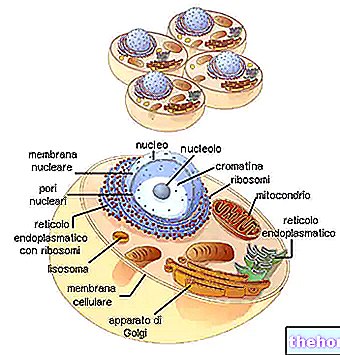
Впоследствии из-за действия других ферментов происходят другие модификации, которые заключаются в гликозидировании гидроксильных групп пролина и лизина (сахар связывается с кислородом ОН); эти ферменты находятся в областях, отличных от просвета, поэтому белок, претерпевая модификации, мигрирует внутри эндоплазматического ретикулума и попадает в мешочки (пузырьки), которые закрываются сами на себя и отделяются от ретикулума: внутри них он содержит гликозидированный протеин. -коллагеновый мономер; последний достигает аппарата Гольджи, где определенные ферменты распознают цистеин, присутствующий в карбоксиконцевой части гликозидированного проколлагена, и заставляют различные цепи сближаться друг с другом и образовывать дисульфидные мостики: таким образом, три цепи гликозидированный проколлаген получается связанным вместе, и это является отправной точкой, из которой три цепи, взаимопроникающие, затем спонтанно образуют тройную спираль.Три цепи гликозидированного проколлагена, связанные вместе, достигают, затем везикулу, которая, задыхаясь, отделяется от аппарата Гольджи, транспортируя три цепи к периферии клетки, где через предохранитель ион с плазматической мембраной, триметр изгоняется из клетки.
Во внеклеточном пространстве есть особые ферменты, проколлагеновые пептидазы, которые удаляют из видов, изгнанных из клетки, три фрагмента (по одному для каждой спирали) из 300 аминокислот на 1 дюйм, из концевой карбоксильной части и три фрагмента. фрагменты (по одному на каждую спираль) примерно из 100 аминокислот каждый, от аминоконцевой части: остается тройная спираль, состоящая примерно из 800 аминокислот на спираль, известная как тропоколлаген.
Тропоколлаген имеет вид довольно жесткого стержня; различные тримеры связываются ковалентными связями, образуя более крупные структуры: микрофибриллы. В микрофибриллах различные тримеры расположены в шахматном порядке; многие микрофибриллы составляют пучки тропоколлагена.
В костях, между коллагеновыми волокнами, есть интерстициальные пространства, в которых откладываются сульфаты и фосфаты кальция и магния: эти соли также покрывают все волокна; это делает кости жесткими.
В сухожилиях интерстициальные пространства менее богаты кристаллами, чем в костях, а белки меньше, чем в тропоколлагене: это придает сухожилиям эластичность.
Остеопороз - это заболевание, вызванное недостатком кальция и магния, из-за которого невозможно зафиксировать соли в интерстициальных областях волокон тропоколлагена.