Активные ингредиенты: Вилдаглиптин.
Галвус в таблетках по 50 мг
Показания Почему используется Галвус? Для чего это?
Действующее вещество Галвуса, вилдаглиптин, относится к группе лекарств, называемых «пероральные противодиабетические средства».
Галвус используется для лечения взрослых пациентов с сахарным диабетом 2 типа. Он используется, когда диабет нельзя контролировать с помощью одной диеты и физических упражнений. Он помогает контролировать уровень сахара в крови. Ваш врач назначит галвус отдельно или вместе. Другие противодиабетические лекарства вы уже принимаете, если не было доказано, что они достаточно эффективны для контроля диабета.
Диабет 2 типа развивается, когда организм не вырабатывает достаточно инсулина или если инсулин, который вырабатывает организм, не работает должным образом. Он также может развиться, когда организм вырабатывает слишком много глюкагона.
Инсулин - это вещество, которое помогает снизить уровень сахара в крови, особенно после еды. Глюкагон - это вещество, которое запускает производство сахара в печени, вызывая повышение уровня сахара в крови. Поджелудочная железа вырабатывает оба этих вещества.
Как работает Галвус
Галвус заставляет поджелудочную железу производить больше инсулина и меньше глюкагона. Это помогает контролировать уровень сахара в крови. Было показано, что это лекарство снижает уровень сахара в крови. Это поможет предотвратить осложнения диабета. Даже если вы начнете принимать лекарства от диабета сейчас, важно продолжать соблюдать рекомендованную диету и / или заниматься физическими упражнениями.
Противопоказания Когда нельзя применять Галвус
Не принимайте Галвус:
- если у вас аллергия на вилдаглиптин или какие-либо другие ингредиенты этого лекарства (перечислены в разделе 6). Если вы считаете, что у вас может быть аллергия на вилдаглиптин или какие-либо другие ингредиенты Galvus, не принимайте это лекарство и обратитесь к врачу.
Меры предосторожности при применении Что следует знать перед приемом Галвуса
Перед приемом Галвуса проконсультируйтесь со своим врачом, фармацевтом или диабетической медсестрой.
- если у вас диабет 1 типа (ваше тело не вырабатывает инсулин) или если у вас есть заболевание, называемое диабетическим кетоацидозом.
- если вы принимаете антидиабетическое лекарство, известное как сульфонилмочевина (если вы принимаете его вместе с Galvus, ваш врач может уменьшить дозу сульфонилмочевины, чтобы избежать низкого уровня глюкозы в крови [гипогликемии]).
- если у вас умеренное или тяжелое заболевание почек (вам потребуется меньшая доза Галвуса).
- если вы на диализе
- если у вас заболевание печени
- если вы страдаете сердечной недостаточностью
- если у вас есть или когда-либо было заболевание поджелудочной железы
Если вы ранее принимали вилдаглиптин, но вам пришлось прекратить его прием из-за заболевания печени, вам не следует принимать это лекарство.
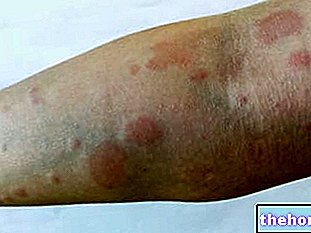
Поражения кожи - частое осложнение диабета. Желательно соблюдать рекомендации врача или медсестры по уходу за кожей и стопами, а также обращать особое внимание на образование волдырей или язв во время приема Галвуса. Если это произойдет, вам следует незамедлительно проконсультироваться с врачом.
Перед началом лечения Галвусом будет проведено обследование для оценки функционирования печени, которое будет повторяться каждые три месяца в течение первого года лечения и периодически в дальнейшем. Это необходимо для того, чтобы как можно скорее обнаружить признаки повышенного содержания печеночных ферментов.
Дети и подростки
Не рекомендуется применение Галвуса детям и подросткам до 18 лет.
Взаимодействие Какие лекарства или продукты могут изменить действие Galvus
Сообщите своему врачу или фармацевту, если вы принимаете, недавно принимали или собираетесь принимать какие-либо другие лекарства.
Ваш врач может изменить дозу Галвуса, если вы принимаете другие лекарства, такие как:
- тиазиды или другие диуретики (также называемые таблетками для мочеиспускания) - кортикостероиды (обычно используются для лечения воспаления)
- лекарства для щитовидной железы
- некоторые лекарства, влияющие на нервную систему.
Предупреждения Важно знать, что:
Беременность и кормление грудью
Если вы беременны или кормите грудью, подозреваете, что беременны или планируете беременность, проконсультируйтесь с врачом или фармацевтом, прежде чем принимать это лекарство.
Вы не должны использовать Галвус во время беременности. Неизвестно, попадает ли Galvus в грудное молоко. Вы не должны использовать Galvus, если вы кормите грудью или планируете кормить грудью.
Вождение и использование машин
Если вы чувствуете головокружение при приеме Галвуса, не садитесь за руль и не пользуйтесь механизмами.
Галвус содержит лактозу
Галвус содержит лактозу (молочный сахар). Если врач сказал вам, что у вас непереносимость некоторых сахаров, обратитесь к врачу, прежде чем принимать это лекарство.
Доза, способ и время приема Как применять Галвус: Дозировка
Всегда принимайте это лекарство точно так, как вам сказал врач. В случае сомнений проконсультируйтесь с врачом или фармацевтом.
Сколько принимать и когда
Количество Galvus, которое необходимо принять, варьируется в зависимости от индивидуальных условий. Ваш врач скажет вам, сколько именно таблеток Галвуса нужно принять. Максимальная суточная доза - 100 мг.
Обычная доза Галвуса составляет:
- 50 мг в день в виде однократной дозы утром, если вы принимаете Галвус с другим лекарством, называемым сульфонилмочевиной.
- 100 мг в день по 50 мг утром и 50 мг вечером, если вы принимаете только Галвус с другим лекарством, называемым метформин или глитазон, с комбинацией метформина и сульфонилмочевины или с инсулином.
- 50 мг в день утром, если у вас умеренное или тяжелое заболевание почек или вы находитесь на диализе.
Как принимать Галвус
- Таблетки проглотить, запивая водой.
Как долго принимать Галвус
- Принимайте Галвус каждый день столько, сколько рекомендует врач. Возможно, вам придется продолжать это лечение в течение длительного времени.
- Врач будет регулярно проверять ваше состояние, чтобы убедиться, что лечение дает желаемый эффект.
Если вы забыли принять Галвус
Если вы забыли принять дозу этого лекарства, примите ее, как только вспомните. Затем примите следующую дозу в обычное время. Если уже почти пора принять следующую дозу, пропустите пропущенную дозу. Не принимайте двойную дозу, чтобы восполнить пропущенную таблетку.
Если вы перестанете принимать Галвус
Не прекращайте прием Галвуса, если ваш врач не скажет вам об этом. Если вы не уверены, как долго вы будете принимать это лекарство, спросите своего врача.
Передозировка Что делать, если вы приняли слишком много Галвуса
Если вы приняли слишком много таблеток Галвуса или ваше лекарство принял кто-то другой, немедленно обратитесь к врачу. Может потребоваться медицинская помощь. Если вам нужно обратиться к врачу или в больницу, возьмите упаковку с собой.
Побочные эффекты Каковы побочные эффекты Галвуса
Как и все лекарства, это лекарство может вызывать побочные эффекты, хотя они возникают не у всех.
Некоторые симптомы требуют немедленной медицинской помощи:
Вы должны прекратить прием Галвуса и немедленно обратиться к врачу при возникновении любого из следующих побочных эффектов:
- Ангионевротический отек (редко: может наблюдаться у 1 из 1000 человек): симптомы включают отек лица, языка или горла, затрудненное глотание, затрудненное дыхание, внезапную сыпь или крапивницу, что может указывать на реакцию, называемую «ангионевротический отек».
- Заболевание печени (гепатит) (редко): симптомы включают пожелтение кожи и глаз, тошноту, потерю аппетита или темную мочу, что может указывать на заболевание печени (гепатит).
- Воспаление поджелудочной железы (панкреатит) (частота неизвестна). Симптомы включают сильную и постоянную боль в животе (в области живота), которая может распространяться на спину, а также тошноту и рвоту.
Другие побочные эффекты
У некоторых пациентов при приеме галвуса и метформина наблюдались следующие побочные эффекты:
- Общие (им может быть подвержено до 1 человека из 10): тремор, головная боль, головокружение, тошнота, низкий уровень глюкозы в крови.
- Нечасто (им может быть подвержено до 1 человека из 100): усталость.
Некоторые пациенты испытали следующие побочные эффекты при приеме Галвуса и сульфонилмочевины:
- Часто: тремор, головная боль, головокружение, слабость, низкий уровень глюкозы в крови.
- Нечасто: запор.
- Очень редко (им может быть подвержено до 1 человека из 10000): боль в горле, насморк.
Некоторые пациенты испытывали следующие побочные эффекты при приеме Галвуса и глитазона:
- Часто: увеличение веса, отек рук, щиколоток или стоп (отек).
- Нечасто: головная боль, слабость, низкий уровень глюкозы в крови.
Некоторые пациенты испытывали следующие побочные эффекты при приеме только Галвуса:
- Часто: головокружение.
- Нечасто: головная боль, запор, отек рук, лодыжек или стоп (отек), боль в суставах, низкий уровень глюкозы в крови.
- Очень редко: боль в горле, насморк, лихорадка.
Некоторые пациенты испытывали следующие побочные эффекты при приеме галвуса, метформина и сульфонилмочевины:
- Часто: головокружение, тремор, слабость, низкий уровень глюкозы в крови, повышенное потоотделение.
Некоторые пациенты испытывали следующие побочные эффекты при приеме Галвуса и инсулина (с метформином или без него):
- Часто: головная боль, озноб, тошнота (плохое самочувствие), низкий уровень глюкозы в крови, изжога.
- Нечасто: диарея, метеоризм.
Во время маркетинга этого лекарства также сообщалось о следующих побочных эффектах:
- Частота неизвестна (невозможно оценить по имеющимся данным): зудящая сыпь, воспаление поджелудочной железы, локальное шелушение кожи или волдырей, мышечные боли.
Сообщение о побочных эффектах
Если у вас появятся какие-либо побочные эффекты, поговорите со своим врачом, фармацевтом или медсестрой, занимающейся диабетом. Это включает в себя любые возможные побочные эффекты, не перечисленные в этой брошюре. Вы также можете сообщить о побочных эффектах напрямую через национальную систему отчетности, указанную в Приложении V. Сообщая о побочных эффектах вы можете помочь предоставить дополнительную информацию о безопасности этого лекарства.
Срок действия и удержание
- Храните это лекарство в недоступном для детей месте.
- Не используйте это лекарство после истечения срока годности, указанного на блистере и коробке после «EXP» / «EXP». Срок годности относится к последнему дню этого месяца.
- Хранить в оригинальной упаковке, беречь от влаги.
- Не используйте упаковку Galvus, если она повреждена или имеет признаки взлома.
Expiry "> Другие взаимодействия
Что содержит Галвус
- Действующее вещество - вилдаглиптин. Каждая таблетка содержит 50 мг вилдаглиптина.
- Другими ингредиентами являются безводная лактоза, микрокристаллическая целлюлоза, натрийгликолят крахмала (тип A) и стеарат магния.
Описание внешнего вида Галвуса и содержимое упаковки
Таблетки Galvus 50 мг круглые, плоские, от белого до слегка желтоватого цвета, с надписью "NVR" на одной стороне и "FB" на другой.
Таблетки Galvus 50 мг доступны в упаковках, содержащих 7, 14, 28, 30, 56, 60, 90, 112, 180 или 336 таблеток, и в групповых упаковках, содержащих 3 картонные коробки, каждая из которых содержит 112 таблеток.
Не все размеры упаковки могут продаваться в вашей стране.
Листовка с исходным кодом: AIFA (Итальянское агентство по лекарственным средствам). Контент опубликован в январе 2016 года. Представленная информация может быть устаревшей.
Чтобы иметь доступ к самой последней версии, рекомендуется зайти на сайт AIFA (Итальянское агентство по лекарственным средствам). Заявление об ограничении ответственности и полезная информация.
01.0 НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА -
GALVUS 50 мг ТАБЛЕТКИ
02.0 КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ -
Каждая таблетка содержит 50 мг вилдаглиптина.
Наполнитель с известным эффектом: каждая таблетка содержит 47,82 мг лактозы (безводной).
Полный список вспомогательных веществ см. В разделе 6.1.
03.0 ФАРМАЦЕВТИЧЕСКАЯ ФОРМА -
Таблетка.
Круглая (диаметр 8 мм), от белого до слегка желтоватого цвета, плоская таблетка со скошенными краями.
Буквы «NVR» выбиты с одной стороны, «FB» - с другой.
04.0 КЛИНИЧЕСКАЯ ИНФОРМАЦИЯ -
04.1 Терапевтические показания -
Вилдаглиптин показан для лечения сахарного диабета 2 типа у взрослых:
В монотерапии
- у пациентов, недостаточно контролируемых только диетой и физическими упражнениями, и которым терапия метформином нецелесообразна из-за противопоказаний или непереносимости.
В двойной пероральной терапии в сочетании с:
- метформин у пациентов с недостаточным гликемическим контролем, несмотря на введение максимально переносимой дозы только метформина,
- сульфонилмочевина, у пациентов с недостаточным гликемическим контролем, несмотря на введение максимально переносимой дозы сульфонилмочевины, и для которых терапия метформином не подходит из-за противопоказаний или непереносимости,
- тиазолидиндион у пациентов с недостаточным гликемическим контролем и у которых уместно применение тиазолидиндиона.
В тройной пероральной терапии в сочетании с:
- сульфонилмочевина и метформин, когда диета и физические упражнения, связанные с двойной терапией этими препаратами, не обеспечивают адекватного гликемического контроля.
Вилдаглиптин также показан для использования в комбинации с инсулином (с метформином или без него), когда диета и физические упражнения в сочетании со стабильной дозой инсулина не обеспечивают адекватного гликемического контроля.
04.2 Дозировка и способ применения -
Дозировка
Взрослые
При использовании отдельно, в комбинации с метформином, в комбинации с тиазолидиндионом, в комбинации с метформином и сульфонилмочевиной или в комбинации с инсулином (с метформином или без него) рекомендуемая суточная доза вилдаглиптина составляет 100 мг за одну дозу. 50 мг утром и 50 мг вечером.
При использовании в двойной терапии в сочетании с сульфонилмочевиной рекомендуемая доза вилдаглиптина составляет 50 мг один раз в день утром. В этой популяции пациентов вилдаглиптин в дозе 100 мг в сутки был не более эффективен, чем вилдаглиптин в дозе 50 мг один раз в сутки.
При использовании в комбинации с сульфонилмочевиной более низкая доза сульфонилмочевины может снизить риск гипогликемии.
Дозы выше 100 мг не рекомендуются.
Если пропущена доза Галвуса, ее следует принять, как только пациент вспомнит об этом.
Не следует принимать двойную дозу в тот же день.
Безопасность и эффективность вилдаглиптина в качестве тройной пероральной терапии в сочетании с метформином и тиазолидиндионом не установлены.
Дополнительная информация для конкретных групп пациентов
Пожилые (≥ 65 лет)
У пожилых пациентов коррекция дозы не требуется (см. Также разделы 5.1 и 5.2).
Нарушение функции почек
У пациентов с почечной недостаточностью легкой степени тяжести коррекции дозы не требуется (оформление креатинин ≥ 50 мл / мин). Для пациентов с умеренной или тяжелой почечной недостаточностью или терминальной стадией почечной недостаточности (ТПН) рекомендуемая доза Галвуса составляет 50 мг один раз в день (см. Также разделы 4.4, 5.1 и 5.2).
Нарушение функции печени
Галвус не следует применять пациентам с нарушением функции печени, включая пациентов, у которых уровень аланинаминотрансферазы (АЛТ) или аспартатаминотрансферазы (АСТ) превышает верхний предел нормы (ВГН) в 3 раза до лечения (см. Также разделы 4.4 и 5.2).
Педиатрическая популяция
Применение Галвуса не рекомендуется детям и подросткам (
Способ применения
Пероральное употребление
Галвус можно принимать с пищей или без нее (см. Также раздел 5.2).
04.3 Противопоказания -
Повышенная чувствительность к действующему веществу или любому из вспомогательных веществ, перечисленных в разделе 6.1.
04.4 Особые предупреждения и соответствующие меры предосторожности при использовании -
Общий
Галвус не заменяет инсулин у инсулинозависимых пациентов. Галвус не следует применять пациентам с диабетом 1 типа или для лечения диабетического кетоацидоза.
Нарушение функции почек
Опыт лечения гемодиализных пациентов с ТПН ограничен, поэтому этим пациентам следует применять Галвус с осторожностью (см. Также разделы 4.2, 5.1 и 5.2).
Нарушение функции печени
Галвус не следует использовать у пациентов с нарушением функции печени, включая пациентов с уровнем АЛТ или АСТ> 3x ULN до лечения (см. Также разделы 4.2 и 5.2).
Мониторинг ферментов печени
Сообщалось о редких случаях нарушения функции печени (включая гепатит). В этих случаях у пациентов, как правило, не было симптомов без клинических последствий, а показатели функции печени нормализовались после прекращения лечения. Перед началом лечения Галвусом следует провести функциональные пробы печени, чтобы узнать исходное значение для пациента. Во время лечения Галвусом следует проверять функцию печени каждые три месяца в течение первого года лечения и периодически в дальнейшем. Пациенты, у которых развивается повышенный уровень трансаминаз, должны быть проверены с помощью второй оценки функции печени для подтверждения результатов, а затем продолжены частыми функциональными тестами печени до тех пор, пока отклонения не вернутся к норме. Если повышение уровня АСТ или АЛТ в 3 раза превышает верхний предел нормы или выше, рекомендуется прекратить терапию Галвусом. Пациентам, у которых развивается желтуха или другие признаки нарушения функции печени, следует прекратить лечение Галвусом.
После прекращения лечения Галвусом и нормализации показателей функции печени лечение Галвусом не следует возобновлять.
Сердечная недостаточность
Клиническое исследование вилдаглиптина у пациентов I-III функциональных классов Нью-Йоркской кардиологической ассоциации (NYHA) показало, что лечение вилдаглиптином не было связано с изменениями функции левого желудочка или ухудшением ранее существовавшей застойной сердечной недостаточности (ЗСН) по сравнению с плацебо. Клинические данные Опыт лечения пациентов с функциональным классом III по NYHA, получавших вилдаглиптин, все еще ограничен, а результаты неубедительны (см. раздел 5.1).
Нет опыта использования вилдаглиптина в клинических испытаниях у пациентов с IV функциональным классом по NYHA, поэтому его применение у таких пациентов не рекомендуется.
Кожные заболевания
В доклинических токсикологических исследованиях сообщалось о поражениях кожи, включая волдыри и язвы, на конечностях обезьян (см. Раздел 5.3). Хотя в клинических испытаниях не наблюдалось «увеличения частоты кожных поражений», опыт у пациентов с кожными осложнениями диабета был ограничен. Кроме того, были постмаркетинговые сообщения о буллезных и эксфолиативных поражениях кожи. Поэтому в соответствии с обычным уходом за больным диабетом рекомендуется наблюдение за любыми кожными заболеваниями, такими как волдыри и язвы.
Острый панкреатит
Использование вилдаглиптина связано с риском развития острого панкреатита. Пациенты должны быть проинформированы о характерных симптомах острого панкреатита.
При подозрении на панкреатит прием вилдаглиптина следует прекратить; Если подтвержден острый панкреатит, прием вилдаглиптина не следует возобновлять. Следует соблюдать осторожность пациентам с острым панкреатитом в анамнезе.
Гипогликемия
Известно, что сульфонилмочевины вызывают гипогликемию. Пациенты, получающие вилдаглиптин в сочетании с сульфонилмочевиной, могут иметь риск гипогликемии. Таким образом, более низкая доза сульфонилмочевины может снизить риск гипогликемии.
Вспомогательные вещества
Таблетки содержат лактозу. Пациентам с редкими наследственными проблемами непереносимости галактозы, дефицитом лактазы Лаппа или мальабсорбцией глюкозы-галактозы не следует принимать это лекарство.
04.5 Взаимодействие с другими лекарственными средствами и другие формы взаимодействия -
Вилдаглиптин имеет низкий потенциал взаимодействия при сочетании с другими лекарственными средствами. Поскольку вилдаглиптин не является субстратом фермента цитохрома P (CYP) 450 и не ингибирует и не индуцирует ферменты CYP 450, взаимодействие с активными веществами, которые являются субстратами, ингибиторами или индукторами этих ферментов, маловероятно.
Комбинация с пиоглитазоном, метформином и глибенкламидом
Результаты исследований, проведенных с этими пероральными противодиабетическими средствами, не выявили клинически значимых фармакокинетических взаимодействий.
Дигоксин (субстрат p-гликопротеина), варфарин (субстрат CYP2C9)
Клинические исследования, проведенные со здоровыми людьми, не выявили клинически значимых фармакокинетических взаимодействий. Однако это свидетельство не было подтверждено в контрольной популяции.
Комбинация с амлодипином, рамиприлом, валсартаном или симвастатином
Были проведены исследования лекарственного взаимодействия амлодипина, рамиприла, валсартана и симвастатина на здоровых людях. В этих исследованиях не наблюдалось клинически значимых фармакокинетических взаимодействий после одновременного приема с вилдаглиптином.
Как и в случае применения других пероральных противодиабетических средств, гипогликемический эффект вилдаглиптина может быть уменьшен некоторыми активными веществами, включая тиазиды, кортикостероиды, препараты для лечения щитовидной железы и симпатомиметики.
04.6 Беременность и кормление грудью -
Беременность
Нет адекватных данных об использовании вилдаглиптина у беременных женщин. Исследования на животных показали репродуктивную токсичность в высоких дозах (см. Раздел 5.3). Потенциальный риск для людей неизвестен. Из-за отсутствия данных о людях, Галвус не следует применять во время беременность.
Время кормления
Неизвестно, выделяется ли вилдаглиптин с грудным молоком. Исследования на животных показали экскрецию вилдаглиптина с молоком. Галвус не следует применять в период лактации.
Плодородие
Исследования влияния Galvus на фертильность человека не проводились (см. Раздел 5.3).
04.7 Влияние на способность управлять автомобилем и работать с механизмами -
Исследования способности управлять автомобилем и работать с механизмами не проводились. Пациентам, у которых головокружение является побочной реакцией, следует избегать вождения или использования механизмов.
04.8 Побочные эффекты -
Резюме профиля безопасности
Данные по безопасности были получены от 3784 пациентов, получавших ежедневные дозы вилдаглиптина 50 мг (один раз в день) или 100 мг (50 мг два раза в день или 100 мг один раз в день) в контролируемых исследованиях продолжительностью не менее 12 недель. Из этих пациентов 2264 получали только вилдаглиптин и 1520 получали вилдаглиптин в комбинации с другим лекарством. 2682 пациента получали вилдаглиптин в дозе 100 мг в сутки (50 мг два раза в сутки или 100 мг один раз в сутки), а 1102 пациента получали вилдаглиптин в дозе 50 мг один раз в сутки.
Большинство побочных реакций в этих клинических испытаниях были легкими и преходящими по своей природе и не требовали прекращения терапии. Не было никакой связи между побочными реакциями и возрастом, этнической принадлежностью, продолжительностью воздействия или суточной дозой.
Сообщалось о редких случаях нарушения функции печени (включая гепатит). В этих случаях у пациентов, как правило, не было симптомов без клинических последствий, а показатели функции печени нормализовались после прекращения лечения. По данным исследований контролируемой монотерапии или дополнительной терапии продолжительностью до 24 недель, частота повышения АЛТ или АСТ ≥ 3-кратного верхнего предела нормы (классифицируется как присутствующая как минимум в 2 последовательных контрольных исследованиях или при последнем посещении во время лечения) составлял 0,2%, 0,3% и 0,2% для вилдаглиптина 50 мг один раз в день, вилдаглиптина 50 мг два раза в день и всех препаратов сравнения, соответственно. Эти повышения трансаминаз обычно были бессимптомными, непрогрессирующими по своей природе и не были связаны с холестазом или желтухой.
Сообщалось о редких случаях ангионевротического отека при применении вилдаглиптина с частотой, аналогичной контрольной группе. В большинстве случаев сообщалось о применении вилдаглиптина в сочетании с ингибитором фермента ангиотензина (ингибитор АПФ). Большинство явлений были средней степени тяжести и разрешились на фоне лечения вилдаглиптином.
Таблица побочных реакций
Нежелательные реакции, о которых сообщалось у пациентов, получавших Галвус в двойных слепых исследованиях в качестве монотерапии и дополнительной терапии, перечислены ниже для каждого показания с разбивкой по классам органов и абсолютной частоте. Частоты определены как очень общие (≥1 / 10), обычные (≥1 / 100,
Сочетание с метформином
Таблица 1 Нежелательные реакции, зарегистрированные у пациентов, получавших галвус в дозе 100 мг в день в комбинации с метформином в двойных слепых исследованиях (N = 208)
Описание избранных побочных реакций
В контролируемых клинических испытаниях, проведенных с комбинацией вилдаглиптина 100 мг в день + метформин, не сообщалось об отмене препарата из-за побочных реакций ни в группе вилдаглиптина 100 мг в день + метформин, ни в группе плацебо + метформин. В клинических исследованиях частота гипогликемии составляла часто встречается у пациентов, получавших вилдаглиптин в дозе 100 мг в день в комбинации с метформином (1%), и нечасто у пациентов, получавших плацебо + метформин (0,4%). В группе вилдаглиптина не было зарегистрировано серьезных гипогликемических событий.
В клинических исследованиях вес не изменился по сравнению с исходным уровнем при добавлении 100 мг вилдаглиптина к метформину (+0,2 кг и -1,0 кг для вилдаглиптина и плацебо соответственно).
Клинические исследования продолжительностью до 2 лет не показали никаких дополнительных сигналов безопасности или непредвиденных рисков при сочетании вилдаглиптина с метформином.
Сочетание с сульфонилмочевиной
Таблица 2 Нежелательные реакции, зарегистрированные у пациентов, получавших 50 мг галвуса в комбинации с сульфонилмочевиной в двойных слепых исследованиях (N = 170)
Описание избранных побочных реакций
В контролируемых клинических испытаниях, проведенных с комбинацией вилдаглиптин 50 мг + сульфонилмочевина, общая частота отмены из-за побочных реакций составила 0,6% в группе вилдаглиптина 50 мг + сульфонилмочевина по сравнению с 0% в группе, получавшей плацебо + сульфонилмочевину.
В клинических исследованиях при добавлении вилдаглиптина в дозе 50 мг один раз в день к глимепириду частота гипогликемии составляла 1,2% по сравнению с 0,6% в группе плацебо + глимепирид. В группах с вилдаглиптином серьезных гипогликемических событий не сообщалось.
В клинических исследованиях вес не изменился по сравнению с исходным уровнем при добавлении вилдаглиптина 50 мг в день к глимепириду (-0,1 кг и -0,4 кг для вилдаглиптина и плацебо, соответственно).
Ассоциация с тиазолидиндионом
Таблица 3 Побочные реакции, зарегистрированные у пациентов, получавших галвус в дозе 100 мг в день в комбинации с тиазолидиндионом в двойных слепых исследованиях (N = 158)
Описание избранных побочных реакций
В контролируемых клинических испытаниях, проведенных с комбинацией вилдаглиптина 100 мг в день + тиазолидиндион, как в группе вилдаглиптина 100 мг в день + тиазолидиндион, так и в группе плацебо + тиазолидиндион, не сообщалось об отмене препарата из-за побочных реакций. В клинических исследованиях частота гипогликемии была нечасто у пациентов, получавших вилдаглиптин + пиоглитазон (0,6%), тогда как это было обычным явлением у пациентов, получавших плацебо + пиоглитазон (1,9%). В группе вилдаглиптина не было зарегистрировано серьезных гипогликемических событий. В дополнительных исследованиях с пиоглитазоном абсолютная прибавка веса при приеме плацебо и галвуса 100 мг в день составляла 1,4 и 2,7 кг соответственно.
Частота возникновения периферических отеков при добавлении вилдаглиптина в дозе 100 мг в сутки к фоновой терапии с максимальной дозой пиоглитазона (45 мг один раз в сутки) составила 7,0% по сравнению с 2,5% для одного пиоглитазона.
Монотерапия
Таблица 4 Нежелательные реакции, зарегистрированные у пациентов, получавших галвус в дозе 100 мг в день в качестве монотерапии, в двойных слепых исследованиях (N = 1855)
Описание избранных побочных реакций
Кроме того, в контролируемых клинических испытаниях, проведенных с применением только вилдаглиптина, общая частота случаев отмены из-за побочных реакций не была выше у пациентов, получавших вилдаглиптин в дозе 100 мг в день (0,3%), по сравнению с пациентами, получавшими плацебо (0,6%) или компаратором ( 0,5%).
В сравнительных контролируемых исследованиях монотерапии гипогликемия наблюдалась редко и регистрировалась у 0,4% (7 из 1855) пациентов, получавших вилдаглиптин в дозе 100 мг в день, по сравнению с 0,2% (2 из 1082) пациентов в группах активного сравнения или плацебо, без Сообщается о серьезных или серьезных событиях.
В клинических исследованиях вес не изменился по сравнению с исходным уровнем при введении вилдаглиптина в дозе 100 мг в день в качестве монотерапии (-0,3 кг и -1,3 кг для вилдаглиптина и плацебо, соответственно). Не было выявлено дополнительных сигналов безопасности или неожиданных рисков при применении только вилдаглиптина.
Сочетание с метформином и сульфонилмочевиной
Таблица 5 Нежелательные реакции, зарегистрированные у пациентов, получавших Галвус 50 мг два раза в день в сочетании с метформином и сульфонилмочевиной (N = 157)
Описание избранных побочных реакций
Не было случаев отмены из-за побочных реакций в группе лечения вилдаглиптин + метформин + глимепирид по сравнению с 0,6% в группе лечения плацебо + метформин + глимепирид.
Частота гипогликемии была обычной в обеих группах лечения (5,1% для группы вилдаглиптин + метформин + глимепирид по сравнению с 1,9% для группы плацебо + метформин + глимепирид).
Сообщалось об одном тяжелом гипогликемическом событии в группе вилдаглиптина.
В конце исследования влияние на среднюю массу тела было нейтральным (+0,6 кг в группе вилдаглиптина и -0,1 кг в группе плацебо).
Связь с инсулином
Таблица 6 Побочные реакции, зарегистрированные у пациентов, получавших галвус в дозе 100 мг в день в комбинации с инсулином (с метформином или без него) в двойных слепых исследованиях (N = 371)
Описание избранных побочных реакций
В контролируемых клинических испытаниях комбинации вилдаглиптина 50 мг два раза в день с инсулином, с сопутствующим метформином или без него, общая частота отмены из-за побочных реакций составила 0,3% в группе лечения вилдаглиптином, а в группе плацебо отмены не было.
Частота гипогликемии была одинаковой в обеих группах лечения (14,0% в группе вилдаглиптина против 16,4% в группе плацебо). У двух пациентов в группе вилдаглиптина и у 6 пациентов в группе плацебо возникли серьезные гипогликемические события.
В конце исследования влияние на среднюю массу тела было нейтральным (+0,6 кг от исходного уровня в группе вилдаглиптина и без изменения веса в группе плацебо).
Постмаркетинговый опыт
Таблица 7 Постмаркетинговые побочные реакции
Сообщение о предполагаемых побочных реакциях
Отчетность о предполагаемых побочных реакциях, возникающих после получения разрешения на лекарственный препарат, важна, поскольку позволяет осуществлять непрерывный мониторинг баланса пользы и риска лекарственного средства. Медицинских работников просят сообщать о любых предполагаемых побочных реакциях через национальную систему отчетности.
04.9 Передозировка -
Информация о передозировке вилдаглиптином ограничена.
Симптомы
Информация о вероятных симптомах передозировки была получена в результате исследования переносимости повышения дозы у здоровых субъектов, получавших Galvus в течение 10 дней. При приеме 400 мг было три случая мышечной боли и отдельные случаи легкой и преходящей парестезии, лихорадки, отека и временного повышения уровня липазы. При дозе 600 мг у одного пациента развились отеки в ступнях и руках и повысились уровни креатинфосфокиназы (КФК), аспартатаминотрансферазы (АСТ), креативного белка (СРБ) и миоглобина. У трех других субъектов развился отек стопы, в двух случаях - парестезия. Все симптомы и лабораторные отклонения исчезли без лечения после отмены исследуемого препарата.
Уход
В случае передозировки рекомендуется поддерживающее лечение. Вилдаглиптин нельзя удалить гемодиализом. Однако основной метаболит, образующийся при гидролизе (LAY 151), может быть удален путем гемодиализа.
05.0 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА -
05.1 «Фармакодинамические свойства -
Фармакотерапевтическая группа: Лекарства, применяемые при диабете, ингибиторы дипептидилпептидазы 4 (DPP-4), код АТХ: A10BH02.
Вилдаглиптин относится к классу препаратов модулятора островков поджелудочной железы и является мощным и селективным ингибитором DPP-4.
Механизм действия
Введение вилдаглиптина приводит к быстрому и полному ингибированию активности DPP-4, что приводит к увеличению эндогенных уровней GLP-1 (глюкагоноподобный пептид-1) и GIP (глюкозозависимый инсулинотропный полипептид) натощак и после приема пищи.
Фармакодинамические эффекты
Увеличивая эндогенные уровни инкретинов, вилдаглиптин увеличивает чувствительность бета-клеток к глюкозе, что приводит к улучшению глюкозозависимой секреции инсулина. Лечение вилдаглиптином в дозе 50–100 мг в день у пациентов с сахарным диабетом 2 типа значительно улучшилось i. маркер функция бета-клеток, включая HOMA-b (оценка модели гомеостаза -b), отношение проинсулина к инсулину и меры реагирования бета-клеток в тесте на переносимость еды с частым отбором проб. У субъектов, не страдающих диабетом (нормальный уровень глюкозы в крови), вилдаглиптин не стимулирует секрецию инсулина и не снижает уровень глюкозы.
Увеличивая уровень эндогенного GLP-1, вилдаглиптин также увеличивает чувствительность альфа-клеток к глюкозе, что приводит к адекватной секреции глюкагона для количества глюкозы.
Увеличение соотношения инсулин / глюкагон при гипергликемии, вызванное повышением уровня инкретина, вызывает снижение продукции глюкозы в печени натощак и после приема пищи, что приводит к снижению уровня глюкозы в крови.
Известный эффект повышения уровня GLP-1, который замедляет опорожнение желудка, не наблюдается при лечении вилдаглиптином.
Клиническая эффективность и безопасность
Более 15 000 пациентов с сахарным диабетом 2 типа участвовали в двойных слепых плацебо-контролируемых клинических испытаниях с продолжительностью лечения до более 2 лет. В этих исследованиях вилдаглиптин вводили более 9000 пациентов в суточных дозах 50 мг один раз в день, 50 мг два раза в день или 100 мг один раз в день. Более 5000 пациентов мужского пола и более 4000 женщин получали вилдаглиптин по 50 мг один раз в сутки или 100 мг в сутки. Возраст более 1900 пациентов, получавших вилдаглиптин в дозе 50 мг один раз в сутки или 100 мг в сутки, составлял ≥ 65 лет. В этих исследованиях вилдаглиптин назначали в виде монотерапии пациентам с диабетом 2 типа, ранее не получавшим лекарств, или в комбинации у пациентов, недостаточно контролируемых другими противодиабетическими препаратами. продукты.
В целом вилдаглиптин улучшал гликемический контроль при применении отдельно или в сочетании с метформином, сульфонилмочевиной и тиазолидиндионом, о чем свидетельствует клинически значимое снижение уровня HbA1c от исходного уровня.конечная точка исследование (см. Таблицу 8).
В клинических исследованиях величина снижения HbA1c при применении вилдаглиптина была выше у пациентов с более высокими исходными значениями HbA1c.
В 52-недельном двойном слепом контролируемом исследовании вилдаглиптин (50 мг дважды в день) снижал исходный уровень HbA1c на -1% по сравнению с -1,6%, достигнутым для метформина (титрованный до 2 г / день). Статистическая не меньшая эффективность не была получена Пациенты При лечении вилдаглиптином частота нежелательных реакций со стороны желудочно-кишечного тракта была значительно ниже, чем при лечении метформином.
В 24-недельном двойном слепом контролируемом исследовании вилдаглиптин (50 мг два раза в день) сравнивали с розиглитазоном (8 мг один раз в день). У пациентов со средним исходным уровнем HbA1c 8,7% среднее снижение составило -1,20% для вилдаглиптина и -1,48% для розиглитазона. Пациенты, получавшие розиглитазон, в среднем прибавили в весе (+1,6 кг), в то время как пациенты, получавшие вилдаглиптин, не прибавили в весе (-0,3 кг). Частота возникновения периферических отеков была ниже в группе вилдаглиптина, чем в группе розиглитазона (2,1% против 4,1% соответственно).
В двухлетнем клиническом исследовании вилдаглиптин (50 мг два раза в день) сравнивали с гликлазидом (до 320 мг / день). Через два года среднее снижение HbA1c составило -0,5% для вилдаглиптина и -0,6% для гликазида по сравнению со средним исходным уровнем HbA1c, равным 8,6%. Статистической неполноценности достигнуто не было. Вилдаглиптин был связан с меньшим количеством гипогликемических событий (0,7%), чем гликазид (1,7%).
В 24-недельном клиническом исследовании вилдаглиптин (50 мг два раза в день) сравнивали с пиоглитазоном (30 мг один раз в день) у пациентов, которым неадекватно контролировался метформин (средняя суточная доза: 2020 мг). По сравнению с исходным уровнем HbA1c, равным 8,4%, среднее снижение составило -0,9% для вилдаглиптина в комбинации с метформином и -1,0% для пиоглитазона в комбинации с метформином. У пациентов, получавших пиоглитазон в комбинации с метформином, среднее увеличение веса составило +1,9 кг. наблюдалось по сравнению с +0,3 кг, наблюдаемым у тех, кто получал вилдаглиптин в сочетании с метформином.
В двухлетнем клиническом исследовании вилдаглиптин (50 мг два раза в день) сравнивали с глимепиридом (до 6 мг / день - средняя доза за 2 года: 4,6 мг) у пациентов, получавших метформин (средняя дневная доза: 1894 мг). Через 1 год среднее снижение HbA1c составило -0,4% при использовании вилдаглиптина в комбинации с метформином и -0,5% при использовании глимепирида в сочетании с метформином, по сравнению со средним исходным уровнем HbA1c, равным 7,3%. Изменение массы тела составило -0,2 кг при приеме вилдаглиптина по сравнению с +1,6 кг при приеме глимепирида. Частота гипогликемии была значительно ниже в группе вилдаглиптина (1,7%), чем в группе глимепирида (16,2%). В конечной точке исследования (2 года) в обеих группах лечения было обнаружено, что HbA1c был аналогичен исходным значениям. сохранялись изменения массы тела и различия в гипогликемии.
В 52-недельном исследовании вилдаглиптин (50 мг два раза в день) сравнивали с гликлазидом (средняя суточная доза: 229,5 мг) у пациентов, у которых метформин не контролировался должным образом (исходная доза метформина 1928 мг / день). Через 1 год среднее снижение HbA1c составило -0,81% для вилдаглиптина в комбинации с метформином (средний исходный HbA1c 8,4%) и -0,85% для гликлазида в комбинации с метформином (средний исходный HbA1c 8,5%)); Статистическая не меньшая эффективность была достигнута (95% ДИ: -0,11 - 0,20). Изменение массы тела составило +0,1 кг при приеме вилдаглиптина по сравнению с увеличением массы тела на +1,4 кг при приеме гликлазида.
Эффективность фиксированной комбинации вилдаглиптина и метформина (постепенно титруемой до дозы 50 мг / 500 мг два раза в день или 50 мг / 1000 мг два раза в день) в качестве терапии оценивалась в 24-недельном исследовании. деново).
HbA1c снижался на -1,82% при приеме вилдаглиптина / метформина 50 мг / 1000 мг дважды в сутки, на -1,61% при приеме вилдаглиптина / метформина 50 мг / 500 мг два раза в сутки, на -1,36% при приеме метформина 1000 мг два раза в сутки и -1,09 % с вилдаглиптином 50 мг два раза в день, начиная со среднего исходного уровня HbA1c 8,6%. ≥10,0% было более выраженным.
Было проведено 24-недельное двойное слепое рандомизированное многоцентровое плацебо-контролируемое исследование для оценки лечебного эффекта вилдаглиптина 50 мг один раз в сутки по сравнению с плацебо у 515 пациентов с диабетом 2 типа и почечной недостаточностью. Умеренная (N = 294) или тяжелая (N = 221). 68,8% и 80,5% пациентов с умеренной и тяжелой почечной недостаточностью, соответственно, получали инсулин (средняя суточная доза 56 единиц и 51,6 единицы соответственно) на исходном уровне. У пациентов с умеренной почечной недостаточностью вилдаглиптин значительно снижал HbA1c по сравнению с плацебо (разница -0,53%) от среднего исходного уровня 7,9%. У пациентов с тяжелой почечной недостаточностью вилдаглиптин значительно снижал HbA1c по сравнению с плацебо (разница -0,56%). ), начиная со среднего исходного уровня 7,7%.
24-недельное рандомизированное двойное слепое плацебо-контролируемое исследование было проведено с участием 318 пациентов для оценки эффективности и безопасности вилдаглиптина (50 мг два раза в день) в сочетании с метформином (≥1500 мг в сутки) и глимепиридом (≥4 мг). ежедневно). Вилдаглиптин в сочетании с метформином и глимепиридом значительно снижал HbA1c по сравнению с плацебо.
Среднее снижение HbA1c с поправкой на плацебо по сравнению со средним исходным значением 8,8% составило -0,76%.
24-недельное рандомизированное двойное слепое плацебо-контролируемое исследование было проведено с участием 449 пациентов для оценки эффективности и безопасности вилдаглиптина (50 мг два раза в день) в сочетании со стабильной дозой базального или предварительно смешанного инсулина (средняя суточная доза 41). ед.), с одновременным приемом метформина (N = 276) или без одновременного приема метформина (N = 173). Вилдаглиптин в сочетании с инсулином значительно снижал HbA1c по сравнению с плацебо. В общей популяции среднее снижение HbA1c с поправкой на плацебо по сравнению со средним исходным уровнем HbA1c, равным 8,8%, составило -0,72%. В подгруппах, получавших инсулин с сопутствующим метформином или без него, среднее снижение HbA1c с поправкой на плацебо составило -0,63% и -0,84% соответственно. Частота гипогликемии в общей популяции составила 8,4% и 7,2% в группах вилдаглиптина и плацебо, соответственно.У пациентов, получавших вилдаглиптин, не наблюдалось увеличения веса (+0,2 кг), в то время как у пациентов, получавших плацебо, наблюдалось снижение веса (-0,7 кг).
В другом 24-недельном исследовании с участием пациентов с более поздними стадиями диабета 2 типа, недостаточно контролируемых инсулином (короткая и более длительная продолжительность действия, средняя доза инсулина 80 МЕ / день), среднее снижение HbA1c при приеме вилдаглиптина (50 мг дважды в день) добавление к инсулину было статистически и значительно больше, чем с плацебо + инсулин (0,5% против 0,2%). Частота гипогликемии была ниже в группе вилдаглиптина, чем в группе плацебо (22,9% против 29,6%).
52-недельное многоцентровое рандомизированное двойное слепое исследование было проведено у пациентов с диабетом 2 типа и застойной сердечной недостаточностью (функциональный класс I-III по NYHA) для оценки эффективности вилдаглиптина в дозе 50 мг два раза в день (N = 128) по сравнению с плацебо. (N = 126) по фракции выброса левого желудочка (ФВЛЖ). Вилдаглиптин не связан с изменением функции левого желудочка или ухудшением ранее существовавшей ЗСН. Выявленные сердечно-сосудистые события в целом сбалансированы. У пациентов с сердечной недостаточностью III класса по NYHA, получавших лечение у пациентов с вилдаглиптином было больше сердечных событий, чем у пациентов, получавших плацебо.Однако имелись смещения в исходном уровне сердечно-сосудистого риска в пользу плацебо, а количество событий было низким, что не позволяло сделать однозначные выводы. Вилдаглиптин значительно снижал HbA1c по сравнению с плацебо (разница 0,6%) по сравнению со средним исходным уровнем 7,8% на 16 неделе. В подгруппе NYHA класса III снижение HbA1c было меньше (разница 0,3%), но этот вывод ограничен из-за небольшое количество пациентов (N = 44). Частота гипогликемии в общей популяции составила 4,7% и 5,6% в группах вилдаглиптина и плацебо соответственно.
Сердечно-сосудистый риск
Был проведен метаанализ 25 клинических испытаний фазы III продолжительностью более 2 лет, посвященных сердечно-сосудистым событиям, получившим независимые и проспективные оценки. Этот анализ показал, что лечение вилдаглиптином не было связано с повышенным риском сердечно-сосудистых заболеваний по сравнению со сравнениями. Составная конечная точка доказанных сердечно-сосудистых и цереброваскулярных (CCV) событий [острый коронарный синдром (ACS), транзиторная ишемическая атака (с признаками сердечного приступа на изображениях), инсульт или смерть CCV] была аналогичной для вилдаглиптина по сравнению с комбинацией сравнения активный и плацебо [отношение риска Mantel-Haenszel 0,84 (95% доверительный интервал 0,63–1,12)]. В общей сложности 99 из 8 956 пациентов в группе вилдаглиптина сообщили о событии по сравнению с 91 из 6061 пациента в группе сравнения.
Таблица 8 Ключевые результаты эффективности вилдаглиптина в плацебо-контролируемой монотерапии и дополнительных исследованиях (первичная эффективность в популяции ITT - намерение лечить)
Педиатрическая популяция
Европейское агентство по лекарственным средствам отказалось от обязательства предоставлять результаты исследований вилдаглиптина во всех подгруппах педиатрической популяции с сахарным диабетом 2 типа (информацию о педиатрическом применении см. В разделе 4.2).
05.2 «Фармакокинетические свойства -
Абсорбция
После перорального приема натощак вилдаглиптин быстро всасывается, при этом пиковые концентрации в плазме достигаются через 1,7 часа. Пища немного задерживает (2,5 часа) время достижения пиковой концентрации в плазме, но не изменяет общую экспозицию (AUC). Введение вилдаглиптина с пищей приводит к снижению Cmax (19%). L Однако степень изменения не клинически значимо, поэтому Галвус можно принимать независимо от еды. Абсолютная биодоступность составляет 85%.
Распределение
Связывание вилдаглиптина с белками плазмы низкое (9,3%), и вилдаглиптин равномерно распределяется между плазмой и эритроцитами. После внутривенного введения средний объем распределения вилдаглиптина алло устойчивое состояние (Vss) составляет 71 литр, что предполагает внесосудистое распределение.
Биотрансформация
У людей метаболизм является основным путем выведения вилдаглиптина, на него приходится 69% дозы. Основной метаболит (LAY 151) фармакологически неактивен и является продуктом гидролиза цианогруппы и составляет 57% от дозы. от глюкуронида (BQS867) и продуктов гидролиза амида (4% от дозы). Данные in vitro на микросомах почек человека предполагают, что почки могут быть одним из основных участников гидролиза вилдаглиптина до его основного неактивного метаболита, LAY 151. DPP-4 частично участвует в гидролизе вилдаглиптина согласно исследованию in vivo проводили на крысах без DPP-4. Вилдаглиптин не метаболизируется в количественной степени ферментами CYP 450. Следовательно, не ожидается, что на метаболический клиренс вилдаглиптина будет влиять одновременный прием лекарственных средств-ингибиторов и / или индукторов CYP 450. Исследования in vitro продемонстрировали, что вилдаглиптин не ингибирует / не индуцирует ферменты CYP 450. Следовательно, вилдаглиптин вряд ли влияет на метаболический клиренс лекарственных средств, метаболизируемых CYP 1A2, CYP 2C8, CYP 2C9, CYP 2C19, CYP 2D6, CYP 2E1 или CYP 3A4 / 5, при одновременном применении.
Устранение
После перорального приема [14C] вилдаглиптина примерно 85% дозы выводится с мочой и 15% дозы выводится с фекалиями. После перорального приема почечная экскреция неизмененного вилдаглиптина составляет 23% от дозы. У здоровых субъектов после внутривенного введения оформление общие плазменные и почечные значения вилдаглиптина составляют 41 и 13 л / час соответственно. После внутривенного введения средний период полувыведения составляет примерно 2 ч. После перорального приема период полувыведения составляет примерно 3 часа.
Линейность / нелинейность
В диапазоне терапевтических доз Cmax вилдаглиптина и площадь под кривой зависимости концентрации в плазме от времени (AUC) увеличиваются приблизительно пропорционально дозе.
Конкретные группы пациентов
Секс
Не наблюдалось клинически значимых различий в фармакокинетике вилдаглиптина между здоровыми мужчинами и женщинами в «широком диапазоне возраста и индекса массы тела (ИМТ). На ингибирование DPP-4 вилдаглиптином не влияет» пол.
Пожилые граждане
У здоровых пожилых людей (≥ 70 лет) общая экспозиция вилдаглиптина (100 мг один раз в день) увеличивалась на 32%, при этом пиковая концентрация в плазме увеличивалась на 18% по сравнению со здоровыми молодыми людьми (18 Однако эти изменения не учитываются. клинически значимо. Ингибирование DPP-4 вилдаглиптином не зависит от возраста.
Нарушение функции печени
Влияние печеночной недостаточности на фармакокинетику вилдаглиптина изучалось у пациентов с легким, умеренным и тяжелым нарушением функции печени по шкале Чайлд-Пью (в диапазоне от 6 для легкой степени до 12 для тяжелой) по сравнению со здоровыми субъектами. При легкой и средней степени печеночной недостаточности экспозиция вилдаглиптина после однократного приема снижается (на 20% и 8% соответственно), в то время как для пациентов с тяжелой печеночной недостаточностью экспозиция вилдаглиптина увеличивается на 22%. Максимальное изменение (уменьшение или увеличение ) при экспозиции вилдаглиптина ≥30%, что не считается клинически значимым. Не было корреляции между тяжестью заболевания печени и изменениями экспозиции вилдаглиптина.
Нарушение функции почек
Открытое исследование с применением нескольких доз было проведено для оценки фармакокинетики более низкой терапевтической дозы вилдаглиптина (50 мг один раз в сутки) у пациентов с различной степенью хронической почечной недостаточности, определяемой клиренсом креатинина (легкая: от 50 до
Вилдаглиптин был удален гемодиализом в ограниченной степени (3% в течение 3-4-часового сеанса гемодиализа, начинающегося через 4 часа после введения дозы).
Этнические группы
Ограниченные данные позволяют предположить, что расовая принадлежность не оказывает существенного влияния на фармакокинетику вилдаглиптина.
05.3 Доклинические данные по безопасности -
Задержка проведения внутрисердечного импульса наблюдалась у собак при неэффективной дозе 15 мг / кг (в 7 раз превышающей воздействие на человека на основе Cmax).
Накопление пенистых альвеолярных макрофагов в легких наблюдалось у крыс и мышей. Доза без эффекта составляла 25 мг / кг (5-кратное воздействие на человека на основе AUC) для крыс и 750 мг / кг (142-кратное воздействие на человека) для мышей. У собак наблюдались желудочно-кишечные симптомы, особенно мягкий стул, слизистый стул, диарея и, при более высоких дозах, кровь в стуле. Уровень отсутствия эффекта не установлен.
В обычных исследованиях генотоксичности in vitro А также in vivo вилдаглиптин не оказывал мутагенного действия. У крыс исследование фертильности и раннего эмбрионального развития не показало, что вилдаглиптин вызывает нарушение фертильности, репродуктивной способности или раннего эмбрионального развития. Эмбрио-плодную токсичность оценивали на крысах и кроликах. У крыс наблюдалась повышенная частота плавающих ребер в сочетании со снижением параметров массы тела матери, при этом доза без эффекта составила 75 мг / кг (в 10 раз больше, чем воздействие на человека). У кроликов снизилась масса плода и произошли изменения скелета. свидетельствующие о задержке развития, наблюдались только при наличии тяжелой материнской токсичности при дозе без эффекта 50 мг / кг (в 9 раз больше, чем воздействие на человека). Исследование пре- и постнатального развития было проведено на крысах. только в сочетании с материнской токсичностью при ≥ 150 мг / кг, включая временное снижение массы тела и снижение двигательной активности в поколении F1.
Двухлетнее исследование канцерогенности на крысах было проведено с пероральными дозами до 900 мг / кг (примерно в 200 раз больше, чем воздействие на человека при максимальной рекомендованной дозе). Не наблюдалось увеличения заболеваемости опухолями, связанными с вилдаглиптином. Еще одно двухлетнее исследование канцерогенности было проведено на мышах при пероральных дозах до 1000 мг / кг. Наблюдалось увеличение заболеваемости аденокарциномами молочной железы. Гемангиосаркомы без эффективных доз 500 мг / кг (в 59 раз больше, чем у человека) и 100 мг / кг (в 16 раз больше, чем у человека), соответственно. Повышенная заболеваемость этими опухолями у мышей не считалась значительным риском для людей из-за отсутствия генотоксичности вилдаглиптина и его основного метаболита, развития опухолей у одного вида и всех остальных. Высокий коэффициент системного воздействия, при котором наблюдались опухоли. .
В 13-недельном токсикологическом исследовании на обезьянах циномолгус о поражениях кожи сообщалось при дозах ≥ 5 мг / кг / день. Поражения постоянно локализовались на конечностях (руки, ступни, уши и хвост). При дозе 5 мг / кг / день (приблизительно эквивалентной AUC человека после воздействия дозы 100 мг) наблюдались только везикулы. Они регрессировали, несмотря на продолжающееся лечение, и не были связаны с гистопатологическими отклонениями. При дозах ≥ 20 мг / кг / день (примерно в 3 раза выше AUC у людей после воздействия дозы 100 мг) отмечалось шелушение и шелушение кожи, струпья и язвы на хвосте с соответствующими гистопатологическими изменениями. Некротические поражения хвоста наблюдались при дозах ≥ 80 мг / кг / день.
В течение 4-недельного периода восстановления кожные поражения не регрессировали у обезьян, получавших 160 мг / кг / день.
06.0 ФАРМАЦЕВТИЧЕСКАЯ ИНФОРМАЦИЯ -
06.1 Вспомогательные вещества -
Безводная лактоза
Микрокристаллическая целлюлоза
Гликолят крахмала натрия (тип А)
Стеарат магния
06.2 Несовместимость »-
Не имеет значения.
06.3 Срок действия »-
3 года
06.4 Особые меры предосторожности при хранении -
Хранить в оригинальной упаковке, беречь от влаги.
06.5 Тип непосредственной упаковки и содержимое упаковки -
Алюминий / алюминий в блистерной упаковке (PA / Al / PVC // Al)
Доступен в упаковках по 7, 14, 28, 30, 56, 60, 90, 112, 180 или 336 таблеток и в групповых упаковках по 336 (3 упаковки по 112) таблеток.
Не все размеры упаковки могут быть проданы.
06.6 Инструкции по эксплуатации и обращению -
Никаких особых инструкций.
07.0 ДЕРЖАТЕЛЬ «МАРКЕТИНГОВОГО РАЗРЕШЕНИЯ» -
Новартис Еврофарм Лимитед
Бизнес-парк Фримли
Camberley GU16 7SR
Соединенное Королевство
08.0 НОМЕР РАЗРЕШЕНИЯ НА МАРКЕТИНГ -
EU / 1/07/414 / 001-010
EU / 1/07/414/018
038144010
038144022
038144034
038144046
038144059
038144061
038144073
038144085
038144097
038144109
038144186
09.0 ДАТА ПЕРВОГО РАЗРЕШЕНИЯ ИЛИ ПРОДЛЕНИЯ РАЗРЕШЕНИЯ -
Дата первого разрешения: 26 сентября 2007 г.
Дата последнего обновления: 26 сентября 2012 г.
10.0 ДАТА ПЕРЕСМОТРА ТЕКСТА -
D.CCE, апрель 2015 г.