Активные ингредиенты: трастузумаб.
Герцептин 150 мг порошок для концентрата для приготовления раствора для инфузий
Вкладыши Герцептин доступны для размеров упаковки:- Герцептин 150 мг порошок для концентрата для приготовления раствора для инфузий
- Герцептин 600 мг раствор для инъекций во флаконе
- Герцептин 600 мг раствор для инъекций через устройство для введения
Почему используется Герцептин? Для чего это?
Герцептин содержит активное вещество трастузумаб, которое представляет собой моноклональное антитело. Моноклональные антитела связываются со специфическими белками или антигенами. Трастузумаб предназначен для избирательного связывания с антигеном, называемым рецептором 2 эпидермального фактора роста человека (HER2). HER2 присутствует в больших количествах на поверхности некоторых раковых клеток, стимулируя их рост. Когда герцептин связывается с HER2, он останавливает рост этих клеток и заставляет их умирать.
Ваш врач может назначить Герцептин для лечения рака груди и желудка, если:
- У вас ранний рак груди с высоким уровнем белка HER2.
- У вас метастатический рак груди (рак груди, который распространился далеко от первичного рака) с высоким уровнем HER2. Герцептин может быть назначен в сочетании с химиотерапевтическими препаратами паклитакселом или доцетакселом в качестве первого лечения метастатического рака молочной железы или может быть назначен отдельно, если другие методы лечения оказались неэффективными. Он также используется в сочетании с лекарствами, называемыми ингибиторами ароматазы, для лечения пациентов с высоким уровнем HER2 и метастатическим раком груди, положительным по рецепторам гормонов (рак, чувствительный к присутствию женских половых гормонов).
- У вас метастатический рак желудка с высоким уровнем HER2 в сочетании с другими противораковыми препаратами капецитабином или 5-фторурацилом и цисплатином.
Противопоказания Когда нельзя применять Герцептин
Не применяйте Герцептин, если:
- у вас аллергия на трастузумаб, мышиные (мышиные) белки или любой другой ингредиент.
- у вас серьезные проблемы с дыханием в покое из-за рака или если вам требуется кислородное лечение.
Меры предосторожности при применении Что следует знать перед приемом Герцептина
Ваш врач будет внимательно следить за вашим лечением.
Сердечные проверки
Лечение Герцептином отдельно или с таксаном может повлиять на ваше сердце, особенно если вы уже принимали антрациклин (таксаны и антрациклины - два других типа лекарств, используемых для лечения рака). Поэтому в первую очередь проверяется функция вашего сердца. (каждые три месяца) и после (до двух-пяти лет) лечения Герцептином. Если вы испытываете признаки сердечной недостаточности (т. е. сердце не перекачивает кровь должным образом), возможно, вам придется прекратить прием Герцептина.
Перед приемом Герцептина проконсультируйтесь со своим врачом, фармацевтом или медсестрой, если:
- имели сердечную недостаточность, ишемическую болезнь сердца, заболевание сердечного клапана (шумы в сердце), высокое кровяное давление, принимали или в настоящее время принимают какие-либо лекарства для лечения высокого кровяного давления.
- принимали или в настоящее время принимают лекарство под названием доксорубицин или эпирубицин (лекарства, используемые для лечения рака). Эти препараты (или любой другой антрациклин) могут повредить сердечную мышцу и увеличить риск сердечных проблем при приеме Герцептина.
- вы страдаете одышкой, особенно если вы в настоящее время принимаете таксан. Герцептин может вызвать затруднение дыхания, особенно при первом приеме. Это может быть более серьезным, если вы уже страдаете одышкой. Очень редко пациенты с тяжелыми проблемами дыхания до лечения умирали при приеме Герцептина.
- когда-либо получали другие виды лечения рака.
Если вы получаете лечение Герцептином в сочетании с любыми другими лекарствами, используемыми для лечения рака, такими как паклитаксел, доцетаксел, ингибитор ароматазы, капецитабин, 5-фторурацил или цисплатин, вам также следует прочитать листок-вкладыш для этих лекарств.
Дети и подростки
Герцептин не рекомендуется детям младше 18 лет.
Взаимодействия Какие лекарства или продукты могут изменить действие Герцептина
Сообщите своему врачу, фармацевту или медсестре, если вы принимаете, недавно принимали или собираетесь принимать какие-либо другие лекарства.
Выведение Герцептина из организма может занять до 7 месяцев. Поэтому вам следует сообщить своему врачу, фармацевту или медсестре, что вы принимали Герцептин, если вы начали принимать какие-либо новые лекарства в течение 7 месяцев после прекращения терапии.
Предупреждения Важно знать, что:
Беременность
- Если вы беременны, думаете, что беременны или планируете забеременеть, сообщите об этом своему врачу, фармацевту или медсестре, прежде чем принимать это лекарство.
- Вы должны использовать эффективную контрацепцию во время лечения Герцептином и в течение как минимум 7 месяцев после прекращения лечения.
- Ваш врач обсудит с вами риски и преимущества приема Герцептина во время беременности. В редких случаях у беременных женщин, принимающих Герцептин, наблюдалось уменьшение (амниотической) жидкости, окружающей развивающегося ребенка в утробе матери. Это состояние могло быть вредным для ребенка в утробе матери и было связано с неполным созреванием легких, что привело к смерти плода.
Время кормления
Не кормите грудью во время приема Герцептина и в течение 7 месяцев после приема последней дозы Герцептина, поскольку Герцептин может перейти к ребенку с грудным молоком. Прежде чем принимать какие-либо лекарства, проконсультируйтесь с врачом или фармацевтом.
Вождение и использование машин
Неизвестно, повлияет ли Герцептин на вашу способность управлять автомобилем или механизмами. Однако, если вы испытываете такие симптомы, как озноб или жар, вам не следует водить машину или работать с механизмами, пока эти симптомы не исчезнут.
Дозировка и способ применения Как применять Герцептин: Дозировка
Перед началом лечения ваш врач определит количество HER2 в вашей опухоли. Только пациенты с повышенным уровнем HER2 будут лечиться Герцептином. Герцептин должен назначаться только врачом или медсестрой. Ваш врач назначит вам подходящую дозу и график лечения. Доза Герцептина зависит от веса вашего тела.
Есть два разных типа (составов) Герцептина:
- один вводится инфузией в вену (внутривенная инфузия)
- другой вводится путем инъекции под кожу (подкожная инъекция).
Важно проверять этикетку продукта, чтобы убедиться, что вводится правильный рецепт, прописанный вашим врачом. Внутривенный препарат Герцептина не предназначен для подкожного введения и должен вводиться только внутривенной инъекцией.
Внутривенный препарат Герцептина вводится в виде «внутривенной инфузии (« капельного вливания ») непосредственно в ваши вены. Первая доза вашего лечения вводится в течение 90-минутного периода, и во время приема вы будете находиться под наблюдением медицинского работника, если у вас возникнут какие-либо заболевания. побочный эффект. Если первая доза переносится хорошо, последующие дозы можно вводить в течение 30 минут (см. раздел 2 «Предупреждения и меры предосторожности»). Количество получаемых инфузий будет зависеть от вашей реакции на лечение. Ваш врач примет решение. обсудить это с ней.
Пациентам с ранним раком груди, метастатическим раком груди и метастатическим раком желудка Герцептин вводят каждые 3 недели. Герцептин также можно назначать один раз в неделю для лечения метастатического рака груди.
Чтобы избежать ошибок при приеме лекарств, важно проверять этикетки на флаконах, чтобы убедиться, что лекарство, которое готовится и вводится, представляет собой Герцептин (трастузумаб), а не трастузумаб эмтанзин.
Передозировка Что делать, если вы приняли слишком много Герцептина
Нет никаких известных эффектов, которые можно отнести к передозировке Герцептина.
Если вы перестанете принимать Герцептин
Не прекращайте прием этого препарата, не посоветовавшись предварительно с врачом. Все дозы следует принимать в нужное время каждую неделю или каждые три недели (в зависимости от вашего графика приема). Это помогает препарату действовать наилучшим образом.
Выведение Герцептина из организма может занять до 7 месяцев. Таким образом, ваш врач может решить продолжить наблюдение за функцией вашего сердца даже после завершения лечения.
Если у вас есть дополнительные вопросы по применению этого лекарства, обратитесь к врачу, фармацевту или медсестре.
Побочные эффекты Каковы побочные эффекты Герцептина
Как и все лекарства, Герцептин может вызывать побочные эффекты, но не у всех. Некоторые из этих побочных эффектов могут быть серьезными и могут потребовать госпитализации.
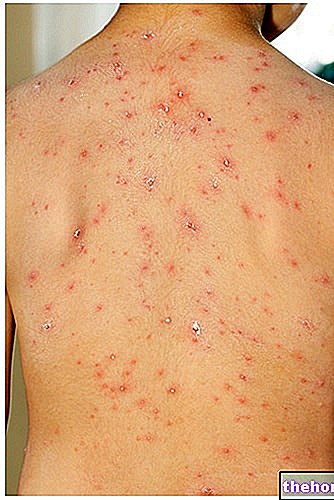
Во время инфузии Герцептина могут возникать такие реакции, как озноб, лихорадка и другие гриппоподобные симптомы. Эти эффекты очень распространены (им может быть подвержено более 1 человека из 10). К другим связанным с инфузией симптомам относятся: тошнота, рвота, боль, увеличение мышц. напряжение и тремор, головная боль, головокружение, затрудненное дыхание, хрипы, высокое или низкое кровяное давление, нарушения сердечного ритма (учащенное сердцебиение, учащенное или нерегулярное сердцебиение), отек лица или губ, кожная сыпь и ощущение усталости. Некоторые из этих симптомов могут быть серьезными, и некоторые пациенты умерли (см. Раздел 2 «Предупреждения и меры предосторожности»).
Эти эффекты в основном проявляются при первой внутривенной инфузии («капание» в вену) и в течение первых нескольких часов после начала инфузии. Обычно они временные. Медицинский работник будет наблюдать за вами во время инфузии и в течение как минимум шести часов после начала первой инфузии и в течение двух часов после начала других инфузий. Если вы почувствуете реакцию, инфузия будет замедлена или остановлена, и вам могут дать лечение для противодействия нежелательным эффектам. Настой можно продолжить после улучшения симптомов.
Иногда симптомы проявляются более чем через шесть часов после начала инфузии. Если это случилось с вами, немедленно обратитесь к врачу. Иногда симптомы могут улучшиться, а позже ухудшиться.
Другие побочные эффекты могут возникать в любое время во время лечения Герцептином, а не только в связи с инфузией. Иногда во время лечения, а иногда и после его окончания могут возникать проблемы с сердцем. Они могут быть серьезными. Они включают ослабление крови. Сердечная мышца, которая может приводят к сердечной недостаточности, воспалению (отечность, покраснение, жар и боль) оболочки сердца и нарушениям сердечного ритма. Это может привести к появлению таких симптомов, как:
- одышка (даже ночью),
- кашель,
- задержка жидкости (отек) в ногах или руках,
- сердцебиение (быстрое или нерегулярное сердцебиение).
Ваш врач будет регулярно контролировать ваше сердце во время лечения, но вы должны немедленно сообщить своему врачу, если заметите какой-либо из вышеперечисленных симптомов.
Если у вас возникнут какие-либо из вышеперечисленных симптомов после завершения лечения Герцептином, вам следует обратиться к врачу и сообщить ему / ей о вашем предыдущем лечении Герцептином.
Очень частые побочные эффекты Герцептина (им может быть подвержено более 1 человека из 10):
- инфекции
- понос
- запор
- ожоги груди (диспепсия)
- слабость
- кожная сыпь
- грудная боль
- боль в животе
- боль в суставах
- низкий уровень эритроцитов и лейкоцитов (которые помогают бороться с инфекциями), иногда связанный с лихорадкой
- мышечная боль
- конъюнктивит
- чрезмерное раздирание
- носовое кровотечение
- насморк
- выпадение волос
- тремор
- приливы
- головокружение
- проблемы с ногтями
- потеря веса
- потеря аппетита
- неспособность заснуть (бессонница)
- Измененный вкус
- Низкое количество тромбоцитов
- Онемение или покалывание пальцев рук и ног
- Покраснение, отек или волдыри во рту и / или горле
- Боль, отек, покраснение или онемение рук и / или ног
Общие побочные эффекты Герцептина (им может быть подвержено до 1 человека из 10):
- аллергические реакции
- сухость во рту и коже
- инфекции горла
- сухие глаза
- инфекции мочевого пузыря и кожи
- потливость
- Опоясывающий лишай
- усталость и недомогание
- воспаление пазух
- был обеспокоен
- воспаление поджелудочной железы или печени
- депрессия
- заболевания почек
- изменения в мышлении
- повышенный мышечный тонус или напряжение (гипертония)
- астма
- боль в руках и / или ногах
- легочные заболевания
- зудящая сыпь
- боль в спине
- сонливость
- боль в шее
- синяки
- боль в костях
- геморрой
- прыщи
- зуд
- судороги ног
Необычные побочные эффекты Герцептина могут наблюдаться у 1 из 100 человек:
- глухота
- сыпь с волдырями
Редкие побочные эффекты Герцептина: им может быть подвержено до 1 человека из 1000:
- слабость
- желтуха
- воспаление / рубцевание легких
Другие побочные эффекты, о которых сообщалось при применении Герцептина: частоту невозможно оценить на основании имеющихся данных:
- аномалии или изменения свертывания крови
- анафилактические реакции
- высокий уровень калия
- отек мозга
- отек или кровотечение за глазами
- отек сердечной оболочки
- медленное сердцебиение
- шок
- нарушение сердечного ритма
- респираторный дистресс
- нарушение дыхания
- острое скопление жидкости в легких
- острое сужение дыхательных путей
- аномальное снижение уровня кислорода в крови
- отек горла
- затрудненное дыхание в положении лежа
- повреждение / недостаточность печени
- отек лица, губ и горла
- почечная недостаточность ненормальное снижение уровня жидкости вокруг ребенка в матке
- недостаточность развития легких в матке
- аномальное развитие почек в матке
Некоторые из возникающих побочных эффектов могут быть связаны с раком груди. Если вы принимаете Герцептин в сочетании с химиотерапией, некоторые из этих побочных эффектов также могут быть связаны с химиотерапией.
Если у вас возникнут какие-либо побочные эффекты, сообщите об этом своему врачу, фармацевту или медсестре.
Сообщение о побочных эффектах
Если у вас появятся какие-либо побочные эффекты, поговорите со своим врачом, фармацевтом или медсестрой. Это включает в себя любые возможные побочные эффекты, не указанные в этой брошюре. Вы также можете сообщить о побочных эффектах напрямую через национальную систему отчетности, перечисленную в Приложении V. Побочные эффекты, которым вы можете помочь предоставьте дополнительную информацию о безопасности этого лекарства.
Срок действия и удержание
Храните это лекарство в недоступном для детей месте.
Не используйте это лекарство после истечения срока годности, указанного на этикетке коробки и флакона после EXP. Срок годности относится к последнему дню этого месяца.
Хранить в холодильнике (2-8 ° C).
Инфузионные растворы следует использовать сразу после разведения. Не используйте Герцептин, если вы заметили какие-либо частицы или изменения цвета до приема.
Лекарства нельзя выбрасывать в канализацию или бытовые отходы. Узнайте у фармацевта, как утилизировать лекарства, которые вы больше не используете. Это поможет защитить окружающую среду.
Состав и лекарственная форма
Что содержит Герцептин
- Действующее вещество - трастузумаб.Каждый флакон содержит 150 мг трастузумаба, который необходимо растворить в 7,2 мл воды для инъекций. Полученный раствор содержит примерно 21 мг / мл трастузумаба.
- Другие ингредиенты: гидрохлорид L-гистидина, L-гистидин, α-дигидрат, α-трегалоза, полисорбат 20.
Как выглядит Герцептин и что содержится в упаковке
Герцептин представляет собой порошок для концентрата раствора для инфузий, который поставляется в стеклянном флаконе, закрытом резиновой пробкой, который содержит 150 мг трастузумаба. Порошок представляет собой лиофилизированные гранулы от белого до светло-желтого цвета. Каждая упаковка содержит 1 флакон порошка.
Листовка с исходным кодом: AIFA (Итальянское агентство по лекарственным средствам). Контент опубликован в январе 2016 года. Представленная информация может быть устаревшей.
Чтобы иметь доступ к самой последней версии, рекомендуется зайти на сайт AIFA (Итальянское агентство по лекарственным средствам). Заявление об ограничении ответственности и полезная информация.
01.0 НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
ГЕРЦЕПТИН 150 МГ ПОРОШОК ДЛЯ КОНЦЕНТРАТА ДЛЯ РАСТВОРА ДЛЯ ИНФУЗИИ
02.0 КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ
Один флакон содержит 150 мг трастузумаба, гуманизированного моноклонального антитела IgG1, продуцируемого культурой клеток млекопитающих (клетки яичников китайского хомячка) в суспензии, очищенного с помощью аффинной хроматографии и ионного обмена, со специфическими процедурами инактивации и удаления вирусов.
Восстановленный раствор Герцептина содержит трастузумаб 21 мг / мл.
Полный список вспомогательных веществ (см. Раздел 6.1).
03.0 ФАРМАЦЕВТИЧЕСКАЯ ФОРМА
Порошок для концентрата для приготовления раствора для инфузий.
Лиофилизированный порошок от белого до светло-желтого цвета.
04.0 КЛИНИЧЕСКАЯ ИНФОРМАЦИЯ
04.1 Терапевтические показания
Рак молочной железы
Метастатический рак груди
Герцептин показан для лечения взрослых пациентов с HER2-положительным метастатическим раком молочной железы (MBC):
• в качестве монотерапии для лечения пациентов, получивших не менее двух режимов химиотерапии по поводу метастатического заболевания. Ранее назначенная химиотерапия должна содержать по крайней мере один антрациклин и один таксан, если только пациент не подходит для такого лечения. Пациенты с положительным рецептором гормонов также должны не реагировать на гормональную терапию, если только пациент не подходит для такого лечения.
• в комбинации с паклитакселом для лечения пациентов, которые не получали химиотерапию по поводу метастатического заболевания и которым не показано лечение антрациклинами.
• в комбинации с доцетакселом для лечения пациентов, которые не получали химиотерапию по поводу метастатического заболевания.
• в комбинации с ингибитором ароматазы при лечении пациентов в постменопаузе с гормонально-положительным МВС, ранее не получавших трастузумаб.
Рак груди на ранней стадии
Герцептин показан для лечения взрослых пациентов с HER2-положительным ранним раком молочной железы (EBC):
• после операции, химиотерапии (неоадъювантной или адъювантной) и лучевой терапии (если применимо) (см. Раздел 5.1)
• после адъювантной химиотерапии доксорубицином и циклофосфамидом в комбинации с паклитакселом или доцетакселом.
• в сочетании с адъювантной химиотерапией доцетакселом и карбоплатином.
• в сочетании с неоадъювантной химиотерапией с последующей адъювантной терапией герцептином, при местнораспространенном заболевании (включая воспалительную форму) или при опухолях> 2 см в диаметре (см. Разделы 4.4 и 5.1).
Герцептин следует использовать только у пациентов с метастатическим раком груди или раком на ранней стадии, опухоли которых демонстрируют сверхэкспрессию HER2 или амплификацию гена HER2, как определено с помощью точного и утвержденного теста (см. Разделы 4.4 и 5.1).
Метастатический рак желудка
Герцептин в комбинации с капецитабином или 5-фторурацилом и цисплатином показан для лечения взрослых пациентов с метастатической аденокарциномой желудка или гастроэзофагеального перехода с положительным результатом HER2, которые ранее не получали противоопухолевую терапию по поводу метастатического заболевания.
Герцептин следует назначать только пациентам с метастатическим раком желудка (MGC), опухоли которых имеют сверхэкспрессию HER2, определяемую как результат IHC2 + и подтвержденную результатами SISH или FISH, или определяемую как результат IHC3 +. Необходимо использовать точные и проверенные методы определения (см. Разделы 4.4 и 5.1).
04.2 Дозировка и способ применения
Измерение экспрессии HER2 является обязательным до начала терапии (см. Разделы 4.4 и 5.1). Лечение герцептином должно начинаться только врачом, имеющим опыт проведения цитотоксической химиотерапии (см. Раздел 4.4), и назначаться только медицинским работником. .
Важно проверить маркировку лекарства, чтобы убедиться, что пациенту вводится правильный препарат (фиксированная доза для внутривенного или подкожного введения). Препарат для внутривенного введения Герцептина не предназначен для подкожного введения и должен вводиться только внутривенно.
В исследовании MO22982 изучалось переключение с лечения внутривенным введением Герцептина на лечение подкожной формой Герцептина и наоборот, вводимое каждые три недели (каждые 3 недели) (см. Раздел 4.8).
Чтобы избежать ошибок при приеме лекарств, важно проверять этикетки на флаконах, чтобы убедиться, что лекарство, которое вы готовите и вводите, является герцептином (трастузумаб), а не кадсилой (трастузумаб эмтанзин).
Дозировка
Метастатический рак груди
Администрация каждые три недели
Рекомендуемая начальная ударная доза составляет 8 мг / кг массы тела. Рекомендуемая поддерживающая доза с трехнедельными интервалами составляет 6 мг / кг массы тела, начиная с трех недель после ударной дозы.
Еженедельное администрирование
Рекомендуемая начальная ударная доза Герцептина составляет 4 мг / кг массы тела. Рекомендуемая еженедельная поддерживающая доза Герцептина составляет 2 мг / кг массы тела, начиная через неделю после ударной дозы.
Применение в комбинации с паклитакселом или доцетакселом
В основных исследованиях (H0648g, M77001) паклитаксел или доцетаксел вводили на следующий день после первой дозы Герцептина (дозы см. В Сводке характеристик продукта (SmPC) паклитаксела или доцетаксела) и сразу после последующих доз Герцептина, если предыдущая Доза Герцептина переносилась хорошо.
Применение в сочетании с ингибитором ароматазы
В базовом исследовании (BO16216) Герцептин и анастрозол вводили с первого дня. Не было ограничений по времени введения Герцептина и анастрозола (дозы см. В SmPC для анастрозола или других ингибиторов ароматазы).
Рак груди на ранней стадии
Администрация каждые три недели и еженедельно
Рекомендуемая начальная ударная доза Герцептина при приеме 3 раза в неделю составляет 8 мг / кг массы тела. Рекомендуемая поддерживающая доза Герцептина с трехнедельным интервалом составляет 6 мг / кг массы тела, начиная с трех недель после ударной дозы.
При еженедельном приеме (начальная ударная доза 4 мг / кг с последующим приемом 2 мг / кг один раз в неделю) одновременно с паклитакселом после химиотерапии доксорубицином и циклофосфамидом.
См. Раздел 5.1 о дозе комбинированной химиотерапии.
Метастатический рак желудка
Администрация каждые три недели
Рекомендуемая начальная ударная доза составляет 8 мг / кг массы тела. Рекомендуемая поддерживающая доза с трехнедельными интервалами составляет 6 мг / кг массы тела, начиная с трех недель после ударной дозы.
Метастатический и ранний рак груди и метастатический рак желудка
Продолжительность лечения
Пациентам с метастатическим раком груди или метастатическим раком желудка следует принимать Герцептин до прогрессирования заболевания. Пациентам с ранним раком молочной железы следует принимать Герцептин в течение 1 года или до рецидива, в зависимости от того, что наступит раньше. Продолжительное лечение EBC более одного года не рекомендуется (см. Раздел 5.1).
Снижение дозировки
В ходе клинических испытаний снижения дозы Герцептина не производилось. Пациенты могут продолжать терапию Герцептином в периоды обратимой миелосупрессии, вызванной химиотерапией, но в этот период следует тщательно контролировать наличие осложнений, связанных с нейтропенией. Обратитесь к SmPC паклитаксела, доцетаксела или ингибитора ароматазы, чтобы уменьшить или отложить дозировку.
Если процент фракции выброса левого желудочка (ФВЛЖ) снижается на ≥ 10 пунктов от исходного уровня и падает ниже 50%, дозирование следует приостановить, а оценку ФВЛЖ повторить в течение примерно 3 недель. Если ФВЛЖ не улучшается или снижается в дальнейшем, или если развивается симптоматическая застойная сердечная недостаточность (ЗСН), следует серьезно подумать о прекращении приема Герцептина, если только польза для отдельного пациента не перевешивает риски. Все эти пациенты должны пройти обследование у кардиолога и наблюдаться с течением времени.
Пропущенные дозы
Если пациент пропустил прием Герцептина в течение недели или меньше, как можно скорее следует ввести обычную поддерживающую дозу Герцептина (еженедельно: 2 мг / кг, каждые 3 недели: 6 мг / кг). Не ждите следующего запланированного цикла. Последующие поддерживающие дозы Герцептина следует вводить через 7 или 21 день в зависимости от соответствующего режима дозирования: еженедельно или каждые три недели.
Если пациент пропустил прием Герцептина более недели, новую ударную дозу Герцептина следует ввести примерно через 90 минут (еженедельная доза: 4 мг / кг, каждые 3 недели доза: 8 мг / кг), как только возможный. Последующие поддерживающие дозы Герцептина (еженедельное введение: 2 мг / кг, введение каждые 3 недели: 6 мг / кг соответственно) следует вводить через 7 или 21 день в зависимости от соответствующего режима дозирования: еженедельно или каждые три недели.
Конкретные группы населения
Фармакокинетические исследования у пожилых людей и у субъектов с нарушением функции почек или печени не проводились. В популяционном фармакокинетическом анализе не было обнаружено, что возраст и почечная недостаточность влияют на доступность трастузумаба.
Педиатрическая популяция
Нет показаний для специального применения Герцептина в педиатрической популяции.
Способ применения
Ударную дозу Герцептина следует вводить в виде 90-минутной внутривенной инфузии. Не вводить в виде внутривенной инъекции или внутривенного болюса. Внутривенное вливание Герцептина должно осуществляться медицинскими работниками, обученными лечению анафилаксии, и при наличии оборудования для оказания неотложной помощи. Пациентов следует наблюдать в течение не менее шести часов после начала первой инфузии и в течение двух часов после начала последующих инфузий на предмет выявления таких симптомов, как лихорадка и озноб или другие симптомы, связанные с инфузией (см. Разделы 4.4 и 4.8. Эти симптомы могут можно контролировать, остановив инфузию или снизив скорость. Вливание можно возобновить после исчезновения симптомов.
Если начальная ударная доза переносится хорошо, последующие дозы можно вводить в виде 30-минутной инфузии.
Инструкции по восстановлению внутривенного препарата Герцептина перед введением см. В разделе 6.6.
04.3 Противопоказания
• Известная гиперчувствительность к трастузумабу, белкам мыши или любому из вспомогательных веществ, перечисленных в разделе 6.1.
• Пациенты с тяжелой одышкой в покое из-за осложнений злокачественных новообразований на поздней стадии или пациенты, которым требуется дополнительная кислородная терапия.
04.4 Особые предупреждения и соответствующие меры предосторожности при использовании
Чтобы улучшить отслеживаемость биологических препаратов, коммерческое название и номер партии вводимого продукта должны быть четко записаны (или объявлены) в медицинской карте пациента.
Тест на HER2 должен проводиться в специализированной лаборатории, которая может гарантировать адекватную валидацию аналитических процедур (см. Раздел 5.1).
В настоящее время нет данных клинических испытаний по повторному лечению пациентов, ранее получавших Герцептин в качестве адъювантной терапии.
Сердечная дисфункция
Общее рассмотрение
Пациенты, принимающие Герцептин, имеют повышенный риск развития ХСН (Класс II-IV согласно Нью-Йоркская кардиологическая ассоциация [NYHA]) или бессимптомная сердечная дисфункция. Эти явления наблюдались у пациентов, получавших только Герцептин или комбинированную терапию паклитакселом или доцетакселом, особенно после химиотерапии антрациклинами (доксорубицин или эпирубицин). Они были от умеренной до тяжелой по интенсивности и были связаны со смертью (см. Параграф 4.8). Кроме того, следует соблюдать особую осторожность при лечении пациентов с повышенным сердечным риском, например гипертония, подтвержденная ишемическая болезнь сердца, ХСН, фракция выброса левого желудочка (ФВЛЖ) пожилой возраст.
Все кандидаты на лечение Герцептином, но особенно пациенты, ранее получавшие лечение антрациклином и циклофосфамидом (АЦ), должны пройти базовую оценку сердечного статуса, включая анамнез и физикальное обследование, электрокардиограмму (ЭКГ), эхокардиограмму и / или многократное сканирование (MUGA). или МРТ. Мониторинг может помочь выявить пациентов, у которых развивается сердечная дисфункция. Оценку сердечной функции, проводимую как первоначальную, следует повторять каждые 3 месяца во время лечения и каждые 6 месяцев после прекращения лечения в течение 24 месяцев после последнего приема Герцептина.
На основании популяционного фармакокинетического анализа всех доступных данных (см. Раздел 5.2) трастузумаб может оставаться в кровотоке до 7 месяцев после прекращения приема Герцептина. Пациенты, получающие антрациклины после прекращения лечения Герцептином, могут иметь повышенный риск сердечной дисфункции. По возможности врачи должны избегать терапии антрациклинами в течение 7 месяцев после прекращения приема Герцептина. Если используются антрациклины, следует тщательно контролировать сердечную функцию пациента.
Пациентам, у которых после первоначального скрининга возникли кардиологические проблемы, следует рассмотреть возможность формального кардиологического обследования. Во время лечения у всех пациентов следует контролировать сердечную функцию (например, каждые 12 недель). Мониторинг может помочь в выявлении пациентов, у которых развивается сердечная дисфункция. Пациентам, у которых развивается бессимптомная сердечная дисфункция, может быть полезно более частое наблюдение (например, каждые 6-8 недель). В случае пациентов, которые сообщают о продолжающемся снижении функции левого желудочка, но остаются бессимптомными, врач должен рассмотреть возможность прекращения терапии, если не наблюдается клинической пользы от терапии Герцептином.
Безопасность продолжения или возобновления приема Герцептина у пациентов с сердечной дисфункцией не изучалась в проспективных исследованиях. Если ФВЛЖ снижается на ≥ 10 баллов по сравнению с исходным уровнем и падает ниже 50%, дозирование следует приостановить и снова оценить ФВЛЖ в течение примерно 3 недель. при отсутствии улучшения или дальнейшего снижения или развития симптоматической ЗСН следует серьезно рассмотреть возможность прекращения приема Герцептина, если только польза для отдельного пациента не перевешивает риски. Эти пациенты должны быть обследованы кардиологом и наблюдаться с течением времени.
Если во время терапии Герцептином возникает симптоматическая сердечная недостаточность, ее следует лечить стандартными лекарственными препаратами для лечения ХСН. Большинство пациентов, у которых развилась ХСН или бессимптомная сердечная дисфункция в основных исследованиях, улучшились при стандартном лечении ингибитором ангиотензинпревращающего фермента (АПФ) или блокатором рецепторов ангиотензина (БРА) и бета-блокатором Большинство пациентов с сердечными симптомами и доказательствами клинической пользы, связанной с Герцептином лечение продолжили терапию без дальнейших сердечных клинических проявлений.
Метастатический рак груди
Герцептин не следует назначать одновременно с антрациклинами в контексте MBC.
Пациенты с MBC, которые ранее получали антрациклины, также подвержены риску сердечной дисфункции при лечении Герцептином, хотя этот риск ниже, чем при одновременном применении Герцептина и антрациклинов.
Рак груди на ранней стадии
У пациентов с EBC кардиологическое обследование, проводимое как первоначальное, следует повторять каждые 3 месяца во время лечения и каждые 6 месяцев после прекращения лечения, вплоть до 24 месяцев после последнего введения Герцептина. Дополнительный мониторинг рекомендуется у пациентов, получающих химиотерапию на основе антрациклинов, и его следует проводить ежегодно в течение 5 лет после последнего введения Герцептина или дольше, если наблюдается продолжающееся снижение ФВЛЖ.
Пациенты с инфарктом миокарда (ИМ) в анамнезе, стенокардией, требующей лечения, предыдущей или текущей ЗСН (класс II-IV по NYHA), кардиомиопатией ФВЛЖ, сердечной аритмией, требующей лечения, клинически значимым пороком клапанов сердца, контролируемой артериальной гипертензией (контролируемая гипертензия) надлежащим стандартным лечением) и гемодинамически значимый перикардиальный выпот были исключены из основных исследований адъювантного и неоадъювантного лечения EBC с применением Герцептина. Таким образом, этим пациентам нельзя рекомендовать лечение.
Адъювантное лечение
Герцептин не следует назначать одновременно с антрациклинами в контексте адъювантной терапии.
Повышенная частота симптоматических и бессимптомных сердечных событий наблюдалась у пациентов с ранним раком молочной железы, когда Герцептин вводился после химиотерапии на основе антрациклинов, по сравнению с режимом доцетаксела и неантрациклинового карбоплатина, и был более выраженным, когда Герцептин вводился одновременно с таксанами. чем при последовательном введении таксанов. Независимо от используемого режима, большинство симптоматических сердечных событий произошло в течение первых 18 месяцев. В одном из 3 основных исследований, в которых следовать за в среднем 5,5 лет (BCIRG006) устойчивое увеличение совокупной частоты симптоматических сердечных событий или ФВЛЖ наблюдалось у пациентов, получавших Герцептин одновременно с таксаном после терапии антрациклином, до 2,37% по сравнению с примерно 1,1% в двух сравнениях. руки (антрациклин плюс циклофосфамид, затем таксан и таксан, карбоплатин и герцептин).
Четыре крупных исследования, проведенных в условиях адъювантной химиотерапии, выявили факторы сердечного риска, в том числе: пожилой возраст (> 50 лет), низкий ФВЛЖ (антигипертензивные препараты. У пациентов, получавших Герцептин после завершения адъювантной химиотерапии, риск сердечной дисфункции был связан с: более высокая кумулятивная доза антрациклинов, вводимая до начала терапии Герцептином, и индекс массы тела (ИМТ)> 25 кг / м2.
Неоадъювантно-адъювантное лечение
Пациентам с EBC, которые являются кандидатами на неоадъювантное лечение, Герцептин следует назначать одновременно с антрациклинами только пациентам, ранее не получавшим химиотерапию, и только по схемам с низкими дозами антрациклина, то есть максимальным кумулятивным дозам доксорубицина 180 мг / м2 или эпирубицина 360 мг / м2.
Если пациенты лечились одновременно с полным курсом низких доз антрациклинов и герцептина в неоадъювантном режиме, после операции не следует проводить дальнейшую цитотоксическую химиотерапию. В других ситуациях решение о необходимости дополнительной цитотоксической химиотерапии должно приниматься с учетом индивидуальных факторов.
На сегодняшний день опыт одновременного приема трастузумаба с низкими дозами антрациклиновых схем ограничен двумя исследованиями (MO16432 и BO22227).
В опорном исследовании MO16432 Герцептин вводили одновременно с неоадъювантной химиотерапией, включающей три курса доксорубицина (кумулятивная доза 180 мг / м2).
Частота симптоматической сердечной дисфункции составила 1,7% в группе, принимавшей герцептин.
Основное исследование BO22227 было разработано, чтобы продемонстрировать не меньшую эффективность лечения препаратом Герцептина для подкожного введения по сравнению с препаратом Герцептин для внутривенного введения на основе общих первичных конечных точек ФК и эффективности (Цикл 8 трастузумаба перед введением дозы и частота ПКО при окончательном хирургическом вмешательстве, соответственно. ) (см. раздел 5.1 ОЛПК Герцептина для подкожного введения). В базовом исследовании BO22227 Герцептин вводили одновременно с неоадъювантной химиотерапией, включающей четыре курса эпирубицина (кумулятивная доза 300 мг / м2); при среднем сроке наблюдения 40 месяцев частота застойной сердечной недостаточности составила 0,0% в группе внутривенного введения герцептина.
Клинический опыт у пациентов старше 65 лет ограничен.
Реакции, связанные с инфузией, и гиперчувствительность
Сообщалось о серьезных побочных реакциях, связанных с инфузией Герцептина, включая одышку, гипотензию, хрипы, гипертензию, бронхоспазм, наджелудочковую тахиаритмию, снижение сатурации кислорода, анафилаксию, респираторный дистресс, крапивницу и ангионевротический отек (см. Раздел 4.8). Премедикация может использоваться для снижения риска таких событий. Большинство этих событий происходит во время или в течение 2,5 часов после начала первой инфузии. Если есть реакция на инфузию, инфузию Герцептина следует прекратить или замедлить скорость инфузии, а за пациентом следует наблюдать до исчезновения всех наблюдаемых симптомов (см. Раздел 4.2. Эти симптомы можно лечить обезболивающими / жаропонижающими средствами, такими как меперидин или парацетамол, или антигистаминами, такими как дифенгидрамин. Большинство пациентов испытали исчезновение симптомов. Симптомы и впоследствии получили дальнейшие инфузии герцептина. Серьезные реакции успешно лечились с помощью поддерживающая терапия, такая как кислород, бета-агонисты и кортикостероиды. В редких случаях эти реакции были связаны с клиническим течением, заканчивающимся летальным исходом. Пациенты, у которых наблюдается одышка в состоянии покоя из-за осложнений запущенных опухолей и сопутствующих заболеваний, могут с большим риском Выше - смертельная реакция на настой. Поэтому таких пациентов нельзя лечить Герцептином (см. Раздел 4.3).
Сообщалось также о начальных улучшениях с последующим клиническим ухудшением и отсроченными реакциями с быстрым клиническим ухудшением. Смерть наступила в течение нескольких часов и до одной недели после инфузии. В очень редких случаях у пациентов наблюдались реакции на инфузию и легочные симптомы более чем через шесть часов после начала инфузии Герцептина. Пациенты должны быть предупреждены о возможности таких отсроченное начало, и в этом случае следует проинструктировать связаться со своим врачом.
Легочные события
Сообщалось о тяжелых легочных осложнениях при применении Герцептина в постмаркетинговых условиях (см. Раздел 4.8). Эти события иногда заканчивались летальным исходом. Сообщалось также о случаях интерстициального заболевания легких, включая легочные инфильтраты, острый респираторный дистресс-синдром, пневмонию., Легкое воспаление, плевральный выпот, респираторный дистресс, острый отек легких и дыхательная недостаточность. Факторы риска, связанные с интерстициальным заболеванием легких, включают предшествующую или сопутствующую терапию другими противоопухолевыми препаратами, такими как таксаны, гемцитабин, винорелбин и лучевая терапия, для которых такая связь уже известна . Эти события могут возникать в контексте инфузионной реакции или иметь отсроченное начало. Пациенты, у которых наблюдается одышка в покое из-за осложнений, связанных с запущенными опухолями и сопутствующими заболеваниями, могут иметь более высокий риск развития событий. Поэтому nti не следует лечить Герцептином (см. раздел 4.3). Следует соблюдать осторожность при воспалении легких, особенно у пациентов, одновременно принимающих таксаны.
04.5 Взаимодействие с другими лекарственными средствами и другие формы взаимодействия
Официальных исследований взаимодействия наркотиков не проводилось. В клинических исследованиях не наблюдалось клинически значимых взаимодействий между Герцептином и лекарственными средствами, принимаемыми одновременно.
Влияние трастузумаба на фармакокинетику других противоопухолевых средств
Фармакокинетические данные исследований BO15935 и M77004 у женщин с HER2-положительным метастатическим раком молочной железы показали, что воздействие паклитаксела и доксорубицина (и их основных метаболитов 6-α-гидроксил-паклитаксела, POH и доксорубицинола, DOL) не изменялось присутствием трастузумаба. (Внутривенная ударная доза 8 мг / кг или 4 м / кг с последующим введением 6 мг / кг каждые 3 недели или 2 мг / кг каждые 1 недели внутривенно, соответственно).
Однако трастузумаб может увеличивать общую экспозицию метаболита доксорубицина (7-дезокси-13 дигидродоксорубицинон, D7D). Биоактивность D7D и клинический эффект увеличения этого метаболита не ясны.
Данные исследования JP16003, одноразового приема Герцептина (ударная доза 4 мг / кг внутривенно и 2 мг / кг внутривенно еженедельно) и доцетаксела (60 мг / м2 внутривенно), проведенного у японских женщин с HER2-положительным метастатическим раком молочной железы, предполагают наличие сопутствующего Введение Герцептина не влияло на фармакокинетику однократной дозы доцетаксела. JP19959 - это часть исследования BO18255 (ToGA), проведенного на японских пациентах мужского и женского пола с распространенным раком желудка для изучения фармакокинетического профиля капецитабина и цисплатина, вводимых с герцептином или без него. Результаты этого подисследования предполагают, что воздействие биоактивных метаболитов (например, 5-ФУ) капецитабина не изменилось при одновременном применении монотерапии цисплатином или цисплатином с герцептином. Однако сам капецитабин показал более высокие концентрации и более длительный период полувыведения в сочетании с Герцептином. Данные также предполагают, что фармакокинетика цисплатина не изменилась при одновременном применении капецитабина или капецитабина в сочетании с герцептином.
Фармакокинетические данные исследования H4613g / GO01305 у пациентов с метастатическим или местнораспространенным неоперабельным HER2-положительным раком молочной железы предполагают, что трастузумаб не влияет на фармакокинетику карбоплатина.
Влияние противоопухолевых препаратов на фармакокинетику трастузумаба
Сравнение смоделированных концентраций трастузумаба в сыворотке после монотерапии Герцептином (нагрузочная доза 4 мг / кг / 2 мг / кг каждые 1 нед внутривенно) и концентраций в сыворотке, наблюдаемых у японских женщин с HER2-положительным метастатическим раком молочной железы (исследование JP16003), показало, что одновременное введение доцетаксела не имело эффекта. по фармакокинетике трастузумаба.
Сравнение фармакокинетических данных двух исследований фазы II (BO15935 и M77004) и одного исследования фазы III (H0648g), в которых пациенты получали сопутствующее лечение герцептином и паклитакселом, и двух исследований фазы II, в которых герцептин вводили в качестве монотерапии (W016229 и MO16982) у женщин с HER2-положительным метастатическим раком молочной железы указывает на то, что индивидуальные и средние минимальные концентрации трастузумаба в сыворотке различаются внутри и между исследованиями, но неясно влияние одновременного приема паклитаксела на фармакокинетику трастузумаба. Сравнение фармакокинетических данных трастузумаба из исследования M77004, в котором женщины с HER2-положительным метастатическим раком молочной железы получали сопутствующее лечение Герцептином, паклитакселом и доксорубицином, и фармакокинетические данные трастузумаба в исследованиях, в которых Герцептин вводился отдельно (H0649g) или в комбинации с антрациклином. плюс циклофосфамид или паклитаксел (исследование H0648g) показали, что доксорубицин и паклитаксел не влияют на фармакокинетику трастузумаба.
Фармакокинетические данные исследования H4613g / GO01305 свидетельствуют о том, что карбоплатин не влияет на фармакокинетику трастузумаба.
Одновременное применение анастрозола не повлияло на фармакокинетику трастузумаба.
04.6 Беременность и кормление грудью
Женщины детородного возраста
Женщины детородного возраста должны быть предупреждены о необходимости использования эффективных средств контрацепции во время лечения Герцептином и в течение 7 месяцев после окончания лечения (см. Раздел 5.2).
Беременность
Исследования репродукции проводились на обезьянах. циномолгус в дозах до 25 раз превышающей еженедельную поддерживающую дозу для человека 2 мг / кг внутривенного препарата Герцептина и не выявило признаков нарушения фертильности или повреждения плода. Перенос трастузумаба через плаценту наблюдался в период развития. Ранний плод (20-50 дни беременности ) и на поздних сроках (120-150 дни гестации). Неизвестно, может ли Герцептин повлиять на репродуктивную способность. Поскольку исследования репродукции животных не всегда позволяют прогнозировать эффекты у мужчин, Герцептин следует избегать во время беременности, за исключением потенциальных преимуществ для матери. перевешивают потенциальные риски для плода.
Постмаркетинговые сообщения о нарушении развития и / или функции почек в сочетании с маловодием, некоторые из которых связаны с фатальной гипоплазией легких у плода, у беременных, получавших Герцептин. В случае беременности женщину следует проинформировать о возможности причинения вреда плоду. Тщательный контроль со стороны многопрофильной бригады желателен, если беременная женщина лечится Герцептином или если беременность наступает во время лечения Герцептином или в течение 7 месяцев после приема последней дозы лекарства.
Время кормления
Исследование на обезьянах Циномолгус Было показано, что во время кормления грудью при дозах, в 25 раз превышающих еженедельную поддерживающую дозу для человека 2 мг / кг внутривенного препарата Герцептина, трастузумаб секретируется с молоком. Присутствие трастузумаба в сыворотке крови новорожденных обезьян не было связано с какими-либо побочными эффектами на рост или развитие от рождения до 1-месячного возраста. Неизвестно, секретируется ли трастузумаб с грудным молоком человека. Поскольку человеческий IgG1 секретируется с грудным молоком человека и потенциальный риск причинения вреда новорожденному неизвестен, женщинам не следует кормить грудью во время терапии Герцептином и в течение 7 месяцев после приема последней дозы.
Плодородие
Данных о рождаемости нет.
04.7 Влияние на способность управлять автомобилем и работать с механизмами
Герцептин не оказывает или оказывает незначительное влияние на способность управлять автомобилем и механизмами. Однако пациентам, у которых развиваются симптомы, связанные с инфузией (см. Раздел 4.4), следует рекомендовать не водить машину и не работать с механизмами до исчезновения симптомов.
04.8 Побочные эффекты
Резюме профиля безопасности
К наиболее серьезным и / или частым побочным реакциям, зарегистрированным на сегодняшний день при применении Герцептина (внутривенный и подкожный), относятся сердечная дисфункция, инфузионные реакции, гематотоксичность (особенно нейтропения), инфекции и легочные побочные реакции.
Табличный список побочных реакций
В этом разделе были использованы следующие категории частот: очень часто (≥1 / 10), часто (≥1 / 100,
В таблице 1 представлены побочные реакции, о которых сообщалось при использовании внутривенного Герцептина отдельно или в комбинации с химиотерапией в основных клинических испытаниях и в постмаркетинговых условиях.
Все включенные термины относятся к самому высокому проценту, наблюдаемому в основных клинических исследованиях.
Таблица 1: Нежелательные эффекты, о которых сообщалось при внутривенной монотерапии Герцептином или в комбинации с химиотерапией в основных клинических исследованиях (N = 8386) и в постмаркетинговый период
+ Указывает на нежелательные реакции, связанные с летальным исходом.
1 Указывает на побочные реакции, о которых сообщается в основном в связи с реакциями, связанными с инфузией. Для них нет конкретных процентных значений.
* Наблюдается при комбинированной терапии после лечения антрациклинами в сочетании с таксанами.
Описание конкретных побочных реакций
Сердечная дисфункция
Застойная сердечная недостаточность (класс II-IV по NYHA) является частой побочной реакцией, связанной с применением Герцептина, и может привести к летальному исходу (см. Раздел 4.4). У пациентов, получавших Герцептин, наблюдались признаки и симптомы сердечной дисфункции, такие как одышка, ортопноэ, усиленный кашель, отек легких, галоп s3, снижение фракции выброса желудочков (см. Раздел 4.4).
В 3 основных клинических испытаниях с применением Герцептина в качестве адъюванта в сочетании с химиотерапией частота сердечной дисфункции 3/4 степени (особенно симптоматическая застойная сердечная недостаточность) была одинаковой у пациентов, получавших только химиотерапию (например, тех, кто не принимал Герцептин), и у пациентов. прием Герцептина последовательно после таксана (0,3-0,4%). Самый высокий процент наблюдался у пациентов, получавших Герцептин одновременно с таксаном (2,0%). Опыт одновременного приема Герцептина и низких доз антрациклинов в условиях неоадъювантной терапии ограничен (см. раздел 4.4).
Когда герцептин был назначен после завершения адъювантной химиотерапии, сердечная недостаточность III-IV классов по NYHA наблюдалась у 0,6% пациентов в группе лечения в течение одного года после среднего периода наблюдения в 12 месяцев. В исследовании BO16348 после среднего периода наблюдения в 8 лет частота тяжелой ХСН (класс III и IV по NYHA) в группе герцептина, получавшей 1 год, составила 0,8%, а частота дисфункции левого желудочка была умеренно симптоматической и бессимптомной - 4,6%. .
Тяжелая обратимость ХСН (определяемая как последовательность как минимум двух последовательных ФВ ЛЖ ≥50% после события) наблюдалась у 71,4% пациентов, получавших Герцептин. Обратимость была продемонстрирована у 79,5% пациентов. 17% событий, связанных с сердечной дисфункцией, произошло после завершения лечения Герцептином.
В основных исследованиях лечения метастатического заболевания с помощью внутривенного препарата Герцептина частота сердечной дисфункции варьировала от 9% до 12%, когда препарат вводился в комбинации с паклитакселом, по сравнению с 1-4% для одного паклитаксела. При монотерапии этот показатель составлял 6–9%. Самый высокий уровень сердечной дисфункции отмечался у пациентов, получавших Герцептин одновременно с антрациклинами / циклофосфамидом (27%), и был значительно выше, чем у пациентов, принимавших только антрациклины / циклофосфамид (7-10%). В последующем клиническом исследовании с проспективным мониторингом сердечной функции было обнаружено, что частота симптоматической застойной сердечной недостаточности составила 2,2% у пациентов, получавших герцептин и доцетаксел, по сравнению с 0% у пациентов, получавших монотерапию доцетакселом. Часть пациентов (79%) ), у которых в ходе этих клинических испытаний развилась сердечная дисфункция, улучшилось состояние после получения стандартного лечения застойной сердечной недостаточности.
Инфузионные реакции, реакции аллергического типа и гиперчувствительность.
Подсчитано, что примерно 40% пациентов, получавших Герцептин, будут испытывать ту или иную форму инфузионной реакции. Однако большинство инфузионных реакций имеют выраженность от легкой до умеренной (балльная система NCI-CTC) и, как правило, возникают на ранних этапах лечения, т. Е. Во время инфузии. , два и три, с меньшей частотой в последующих инфузиях. К таким реакциям относятся озноб, лихорадка, одышка, гипотензия, хрипы, бронхоспазм, тахикардия, снижение сатурации кислорода, респираторный дистресс, сыпь, тошнота, рвота и головная боль (см. Раздел 4.4). Скорость инфузионных реакций всех степеней варьировалась в разных исследованиях в зависимости от показаний, метода сбора данных и назначения трастузумаба одновременно с химиотерапией или монотерапией.
Тяжелые анафилактические реакции, требующие немедленного дополнительного вмешательства, обычно могут возникать как во время первой, так и второй инфузии Герцептина (см. Раздел 4.4) и были связаны с летальным исходом.
В единичных случаях наблюдались анафилактоидные реакции.
Гематотоксичность
Очень часто наблюдаются фебрильная нейтропения и лейкопения. Обычно развивающиеся побочные реакции включали: анемию, тромбоцитопению и нейтропению. Частота эпизодов гипопротромбинемии неизвестна. Риск нейтропении может немного увеличиваться при назначении трастузумаба с доцетакселом после терапии антрациклинами.
Легочные события
Тяжелые легочные побочные реакции возникают в связи с применением Герцептина и были связаны с летальным исходом. К ним относятся, помимо прочего, легочные инфильтраты, острый респираторный дистресс-синдром, пневмония, воспаление легких, плевральный выпот, респираторный дистресс, острый отек легких и дыхательная недостаточность (см. раздел 4.4).
Подробная информация о мерах по минимизации риска, соответствующих Европейскому плану управления рисками, представлена в разделе «Особые предупреждения и меры предосторожности» (раздел 4.4).
Иммуногенность
В условиях неоадъювантно-адъювантного лечения EBC у 8,1% (24/296) пациентов, получавших герцептин внутривенно, развились антитела против трастузумаба (независимо от наличия антител на исходном уровне). Нейтрализующие антитела к трастузумабу были обнаружены в образцах после исходного уровня у 2 из 24 пациентов, получавших герцептин внутривенно.
Клиническая значимость этих антител неизвестна; однако фармакокинетика, эффективность (определяемая полным патологическим ответом [pCR]) и безопасность внутривенного герцептина, определяемая возникновением реакций, связанных с введением (ARR), по-видимому, не были нарушены этими антителами.
Нет данных об иммуногенности Герцептина при раке желудка.
Переход от лечения препаратом Герцептин для внутривенного введения к лечению подкожной формой Герцептина и наоборот
В исследовании MO22982 изучали переход от лечения препаратом Герцептин для внутривенного введения к лечению препаратом Герцептин для подкожного введения с основной целью оценить предпочтение пациентом внутривенного или подкожного введения трастузумаба. В ходе исследования были проанализированы 2 когорты (одна из которых получала препарат для подкожного введения, а другая - препарат для подкожного введения через устройство доставки) с использованием перекрестного дизайна с двумя плечами, в результате чего 488 пациентов были рандомизированы для двух различных последовательностей лечения Герцептином, назначенных каждые три. недель (в / в [циклы 1-4] → п / к [циклы 5-8] или п / к [циклы 1-4] → в / в [циклы 5-8]). Субъекты, ранее не получавшие терапию Герцептином IV (20,3%) или ранее подвергавшиеся воздействию Герцептина IV ( 79,7%). Для последовательности IV → sc (комбинированные группы препаратов для подкожного флакона и препарата для подкожного введения) показатели, связанные с нежелательными явлениями (всех степеней), были соответственно описаны до переключения (циклы 1-4) и после переключения ( циклы 5-8) как 53,8% против 56,4%; для последовательности sc → ev (объединенные когорты scin флакон и п / к через устройство доставки), частота нежелательных явлений (всех степеней) была описана до и после переключения как 65,4% по сравнению с 48,7%.
До перехода (циклы 1-4) частота появления серьезных нежелательных явлений, нежелательных явлений 3 степени и прекращения лечения из-за нежелательных явлений была низкой (
Сообщение о предполагаемых побочных реакциях
Сообщение о предполагаемых побочных реакциях, возникающих после получения разрешения на лекарственный препарат, важно, поскольку оно позволяет осуществлять непрерывный мониторинг баланса пользы / риска лекарственного средства. Медицинских работников просят сообщать о любых предполагаемых побочных реакциях через национальную систему отчетности. "Адрес www. agenziafarmaco.gov.it/it/responsabili.
04.9 Передозировка
В клинических исследованиях на людях не сообщалось о случаях передозировки. Однократные дозы Герцептина, превышающие 10 мг / кг, в клинических исследованиях не применялись. До этого уровня дозы переносились хорошо.
05.0 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
05.1 Фармакодинамические свойства
Фармакотерапевтическая группа: Противоопухолевые препараты, моноклональные антитела, код АТХ: L01XC03.
Трастузумаб представляет собой рекомбинантное гуманизированное моноклональное антитело IgG1 против рецептора 2 фактора роста эпителия человека (HER2). Сверхэкспрессия HER2 наблюдается в 20-30% случаев первичного рака молочной железы. Исследования показателей положительности HER2 при раке желудка (GC), обнаруживаемом с помощью иммуногистохимии (IHC) и гибридизации на месте флуоресцентный (FISH) или гибридный на месте хромогенные (CISH) показали, что существует «широкая вариабельность положительности HER2 в диапазоне от 6,8% до 34,0% для IHC и от 7,1% до 42,6% для FISH». Исследования показали, что пациенты с раком груди с гиперэкспрессией HER2 имеют более короткую выживаемость без признаков заболевания, чем пациенты с раком без гиперэкспрессии HER2. Внеклеточный домен рецептора (ECD, p105) может попадать в кровоток и измеряться в образцах сыворотки.
Механизм действия
Трастузумаб связывается с «высоким сродством и специфичностью с субдоменом IV, перимембранной областью внеклеточного домена HER2. Связывание трастузумаба с HER2 ингибирует лиганд-независимую передачу сигналов HER2 и предотвращает протеолитическое расщепление его внеклеточного домена, что является механизмом активации HER2. Следовательно, трастузумаб продемонстрировал как in vitro что у животных, чтобы иметь возможность ингибировать пролиферацию опухолевых клеток человека, которые сверхэкспрессируют HER2. Кроме того, трастузумаб является мощным медиатором клеточно-опосредованной антителозависимой цитотоксичности (ADCC). В пробирке Было показано, что опосредованная трастузумабом ADCC преимущественно воздействует на опухолевые клетки, сверхэкспрессирующие HER2, по сравнению с опухолевыми клетками, не обладающими сверхэкспрессией HER2.
Обнаружение сверхэкспрессии HER2 или амплификации гена HER2
Обнаружение сверхэкспрессии HER2 или амплификации гена HER2 при раке груди
Герцептин следует использовать только у онкологических больных со сверхэкспрессией HER2 или амплификацией гена HER2, как это определено точным и проверенным тестом. Сверхэкспрессию HER2 следует обнаруживать с помощью иммуногистохимического (ИГХ) исследования фиксированных срезов опухоли (см. Раздел 4.4). Амплификацию гена HER2 следует обнаруживать путем гибридизации. на месте флуоресценцией (FISH) или гибридизацией на месте хромогенный (CISH) фиксированных срезов опухоли. Пациенты, демонстрирующие выраженную сверхэкспрессию HER2 с указанием показателя IHC 3+ или положительного результата FISH или CISH, являются кандидатами на лечение Герцептином.
Чтобы гарантировать точные и воспроизводимые результаты, тесты должны проводиться в специализированных лабораториях, способных гарантировать валидацию аналитических процедур.
Рекомендуемая система для оценки моделей маркировки IHC показана в таблице 2:
Таблица 2 Рекомендуемая система для оценки паттернов ИГХ-мечения при раке груди
В целом, тест FISH считается положительным, если отношение количества копий гена HER2 на опухолевую клетку к количеству копий хромосомы 17 больше или равно 2, или если имеется более 4 копий гена HER2 на опухолевую клетку. Ген HER2 опухолевой клетки, если хромосома 17 не используется в качестве эталона.
В целом, тест CISH считается положительным, если в более чем 50% раковых клеток имеется более 5 копий гена HER2 на ядро.
Полные инструкции по выполнению и интерпретации тестов см. В листовках, прилагаемых к утвержденным тестовым пакетам FISH и CISH. Могут также применяться официальные рекомендации по тестированию HER2.
Для любого другого метода, который может использоваться для оценки экспрессии белка или гена HER2, анализы должны выполняться только в лабораториях, которые обеспечивают оптимальную эффективность валидированных методов. Такие методы должны быть ясными, точными и достаточно точными, чтобы продемонстрировать сверхэкспрессию HER2, и должны уметь отличать умеренную (уровень 2+) от высокой (уровень 3+) избыточную экспрессию HER2.
Обнаружение сверхэкспрессии HER2 или амплификации гена HER2 при раке желудка
Для определения сверхэкспрессии HER2 или амплификации гена HER2 следует использовать только точный и подтвержденный тест. IHC рекомендуется в качестве первого теста, а в случаях, когда также требуется оценка амплификации гена HER2, следует использовать метод гибридизации с ионами серебра in situ (SISH) или метод FISH. Однако рекомендуется использовать технологию SISH для параллельной оценки гистологии и морфологии опухоли. Чтобы обеспечить валидацию процедур оценки и получение точных и воспроизводимых результатов, тест HER2 должен проводиться в лаборатории с обученным персоналом. Полные инструкции по проведению теста и интерпретации результатов можно найти в информационном листе о продукте, прилагаемом к тестам, используемым для оценки HER2.
В исследовании ToGA (BO18255) пациенты с опухолями IHC3 + или FISH были определены как HER2-положительные и поэтому были включены в исследование. Основываясь на результатах клинических исследований, положительные эффекты были ограничены пациентами с более высоким уровнем сверхэкспрессии белка HER2, определяемым как 3+ с ИГХ или 2+ с ИГХ и положительным результатом FISH.
В сравнительном исследовании методологии (исследование D008548) наблюдалась высокая степень согласия (> 95%) между методами SISH и FISH для определения амплификации гена HER2 у пациентов с раком желудка.
Сверхэкспрессию HER2 необходимо определять с помощью иммуногистохимического исследования (ИГХ) фиксированных срезов опухоли. Амплификацию гена HER2 необходимо определять путем гибридизации. на местес использованием SISH или FISH на фиксированных срезах опухоли.
Рекомендуемая система для оценки моделей маркировки IHC показана в таблице 3:
Таблица 3 Рекомендуемая система для оценки паттернов оценки IHC при раке желудка
В общем, тесты SISH или FISH считаются положительными, если отношение количества копий гена HER2 на опухолевую клетку к количеству копий хромосомы 17 больше или равно 2.
Клиническая эффективность и безопасность
Метастатический рак груди
Герцептин использовался в клинических испытаниях отдельно у пациентов с MBC с опухолями, характеризующимися сверхэкспрессией HER2 и неэффективностью одного или нескольких предыдущих режимов химиотерапии для метастатического заболевания (только Герцептин).
Герцептин также использовался в комбинации с паклитакселом или доцетакселом для лечения метастатического заболевания у пациентов, ранее не получавших химиотерапию.Пациенты, предварительно получавшие адъювантную химиотерапию на основе антрациклинов, получали паклитаксел (175 мг / м2, вводимый в виде 3-часовой инфузии) с герцептином или без него. В опорном исследовании доцетаксела (100 мг / м2 в виде 1-часовой инфузии) с герцептином или без него 60% пациентов ранее получали адъювантную химиотерапию на основе антрациклинов. Пациенты получали Герцептин до прогрессирования заболевания.
Эффективность Герцептина в комбинации с паклитакселом у пациентов, ранее не получавших адъювантную терапию антрациклинами, не изучалась.Однако комбинация Герцептин + доцетаксел была эффективной, независимо от того, получали ли пациенты предшествующую адъювантную терапию антрациклинами или нет.
В методе, используемом для анализа сверхэкспрессии HER2 и определения права пациентов участвовать в основных клинических испытаниях монотерапии Герцептином и Герцептином плюс паклитакселом, использовалось иммуногистохимическое окрашивание HER2 фиксированного материала из опухолей молочной железы с использованием мышиных моноклональных антител CB11 и 4D5. Эти ткани фиксировали в формалине. или фиксатор Буэна. Этот метод анализа, используемый в клинических исследованиях и выполняемый в центральной лаборатории, использовал шкалу от 0 до 3+. Пациенты, классифицированные по окраске 2+ или 3+, были включены, в то время как пациенты с окраской 0 или 1+ были исключены Более 70% включенных в исследование пациентов имели «гиперэкспрессию» 3+. Полученные данные свидетельствуют о том, что положительные эффекты были выше у пациентов с более высоким уровнем сверхэкспрессии HER2 (3+).
Основным аналитическим методом, использованным для определения HER2-положительности в базовом исследовании с доцетакселом, с герцептином или без него, был иммуногистохимический анализ. Меньшая часть пациентов была протестирована с помощью гибридизации. на месте во флуоресценции (FISH). В этом исследовании 87% включенных пациентов характеризовались IHC3 + заболеванием, а 95% - IHC3 + и / или FISH-положительным заболеванием.
Еженедельное введение при метастатическом раке груди
Результаты исследований эффективности монотерапии и комбинированных исследований приведены в таблице 4:
Таблица 4 Результаты исследований эффективности монотерапии и комбинированной терапии
ВДП = время до прогрессирования; "нет данных" указывает, что это не могло быть оценено или что это еще не было достигнуто.
1 Исследование H0649g: Субпопуляции пациентов с IHC3 +
2 Исследование H0648g: Субпопуляции пациентов с IHC3 +
3 Исследование M77001: Популяция, планирующая лечение, результаты через 24 месяца
Комбинированное лечение Герцептином с анастрозолом
Герцептин изучался в сочетании с анастрозолом для лечения первой линии пациентов в постменопаузе с гормональным рецептором HER2, сверхэкспрессирующим MBC (например, рецептор эстрогена (ER) и / или рецептор прогестерона (PR)). Выживаемость без прогрессирования заболевания увеличилась вдвое в группе герцептина в комбинации с анастрозолом по сравнению с группой монотерапии анастрозолом (4,8 месяца против 2,4 месяца). По другим параметрам улучшения, наблюдаемые в комбинированной группе, были: общий ответ (16,5% против 6,7%), клиническая польза (42,7% против 27,9%), время до прогрессирования (4, 8 месяцев против 2,4 месяца). Не было разницы между двумя группами по времени и продолжительности ответа. Средняя общая выживаемость была увеличена на 4,6 месяца для пациентов в комбинированной группе. Разница не была статистически значимой, однако более половины пациентов, включенных в группу, принимавшую только анастрозол, лечились по схеме, содержащей герцептин, после прогрессирования заболевания.
Назначение каждые три недели при метастатическом раке молочной железы
Данные об эффективности, полученные при несравнительных исследованиях монотерапии и комбинированной терапии, сведены в Таблицу 5 ниже:
Таблица 5 Результаты эффективности несравнительных исследований, проведенных как при монотерапии, так и при комбинированной терапии
ВДП = время до прогрессирования; "нет данных" указывает, что это не могло быть оценено или что это еще не было достигнуто.
1. Исследование WO16229: ударная доза 8 мг / кг, затем 6 мг / кг каждые 3 недели.
2. Исследование MO16982: ударная доза 6 мг / кг в неделю 3 раза; с последующим приемом 6 мг / кг каждые 3 недели
3. Исследование BO15935
4. Исследование MO16419
Сайты прогресса
Частота прогрессирования печени была значительно снижена у пациентов, получавших комбинацию герцептин-паклитаксел, по сравнению с одним паклитакселом (21,8% против 45,7%; p = 0,004). У большего числа пациентов, получавших герцептин и паклитаксел, наблюдалось прогрессирование центральной нервной системы по сравнению с пациентами, получавшими только паклитаксел (12,6% против 6,5%; p = 0,377).
Рак молочной железы на ранней стадии (адъювантная установка)
Рак груди на ранней стадии определяется как инвазивный неметастатический первичный рак груди.
Использование Герцептина в контексте адъювантной терапии изучалось в 4 крупных многоцентровых рандомизированных исследованиях:
• Исследование BO16348 было разработано для сравнения лечения Герцептином каждые три недели в течение одного и двух лет с наблюдением только у пациентов с HER2-положительным EBC после операции, стандартной химиотерапии и лучевой терапии (если применимо). Также было проведено сравнение между лечением Герцептином в течение одного года и лечением Герцептином в течение двух лет. Пациентам, которые собирались получать Герцептин, вводили начальную нагрузочную дозу 8 мг / кг, а затем 6 мг / кг каждые три недели в течение одного или двух лет.
• Исследования NSAPB B-31 и NCCTG N9831, включая объединенный анализ, были разработаны для оценки клинической полезности комбинации лечения герцептином и паклитакселом после химиотерапии AC; Кроме того, исследование NCCTG N9831 также оценивало последовательное добавление Герцептина к химиотерапии AC → P у пациентов с HER2-положительным EBC после операции.
• Исследование BCIRG 006 было разработано для оценки связи между лечением герцептином и доцетакселом после химиотерапии AC или доцетакселом и карбоплатином у пациентов с HER2-положительным EBC после операции.
Первоначальный рак молочной железы в исследовании HERA ограничивался операбельной первичной инвазивной аденокарциномой молочной железы с положительными подмышечными лимфатическими узлами или отрицательными подмышечными лимфатическими узлами, если опухоль имела диаметр не менее 1 см.
В объединенном анализе NSAPB B-31 и NCCTG N9831, EBC был ограничен женщинами с операбельным раком груди высокого риска, определенным как HER2-положительный и положительный подмышечный лимфатический узел или положительный HER2-положительный и отрицательный подмышечные лимфатические узлы с характеристиками высокого риска (размер опухоли). > 1 см и ER отрицательный или размер опухоли> 2 см, независимо от гормонального статуса).
В исследовании BCIRG 006, HER2-положительный EBC был ограничен пациентами с положительными или отрицательными узлами с высоким риском, определяемым как отсутствие поражения лимфатических узлов (pN0), и по крайней мере 1 из следующего: размер опухоли более 2 см, рецепторы эстрогена и прогестерон отрицательный, гистологический и / или ядерный класс 2-3 или возраст
В таблице 6 обобщены результаты эффективности исследования BO16348 после среднего периода наблюдения 12 месяцев * и 8 лет **:
Таблица 6 Результаты исследования эффективности из исследования BO16348
* Одногодичная ко-первичная конечная точка DFS по сравнению с наблюдением достигла статистического предела по умолчанию
** Окончательный анализ (включая переход 52% пациентов из группы наблюдения к Герцептину)
*** Существует общее несоответствие выборки из-за небольшого числа пациентов, рандомизированных после даты отсечения для 12-месячного среднего последующего анализа.
Результаты промежуточного анализа эффективности превысили заранее определенный статистический предел протокола для сравнения Герцептина в течение 1 года по сравнению с наблюдением. После среднего периода наблюдения в течение 12 месяцев отношение рисков (HR) для безрецидивной выживаемости (DFS) составило 0,54 (95% ДИ 0,44–0,67), что дает абсолютное преимущество с точки зрения 2-летней безрецидивной выживаемости в 7,6 процентных пункта (85,8% против 78,2%) в пользу группы Герцептина.
После среднего периода наблюдения в 8 лет был проведен окончательный анализ, который показал, что лечение Герцептином в течение одного года было связано со снижением риска на 24% по сравнению с одним наблюдением (ОР = 0,76, ДИ 95% 0,67–0,86). означает абсолютное преимущество с точки зрения 8-летней выживаемости без прогрессирования в 6,4 процентных пункта в пользу лечения Герцептином в течение одного года.
В этом окончательном анализе продление лечения Герцептином на два года не показало каких-либо дополнительных преимуществ по сравнению с лечением в течение 1 года [HR DFS в 2-летней популяции по сравнению с 1-летней группой намеренных лечиться (ITT) = 0,99 (95% ДИ: 0,87–1,13), значение p = 0,90 и ОС HR = 0,98 (0,83–1,15); значение p = 0,78]. Частота бессимптомной дисфункции левого желудочка увеличивалась в группе лечения в течение 2 лет (8,1% против 4,6% в группе лечения). В группе лечения в течение 1 года у большего числа пациентов было по крайней мере одно нежелательное явление 3 или 4 степени в группе лечения в течение 2 лет (20,4%) по сравнению с группой лечения в течение 1 года (16,3%).
В исследованиях NSAPB B-31 и NCCTG N9831 Герцептин вводили в комбинации с паклитакселом после химиотерапии AC.
Доксорубицин и циклофосфамид вводили одновременно следующим образом:
• внутривенное введение доксорубицина, 60 мг / м2, каждые 3 недели в течение 4 циклов.
• внутривенное введение циклофосфамида, 600 мг / м2 в течение 30 минут, каждые 3 недели в течение 4 циклов.
Паклитаксел в комбинации с Герцептином вводили следующим образом:
• внутривенный паклитаксел - 80 мг / м2 в виде непрерывной внутривенной инфузии один раз в неделю в течение 12 недель,
или
• паклитаксел внутривенный - 175 мг / м2 в виде непрерывной внутривенной инфузии, вводимой один раз каждые 3 недели в течение 4 циклов (1 день каждого цикла).
Результаты эффективности объединенного анализа NSAPB B-31 и NCCTG 9831 на момент окончательного анализа DFS * суммированы в таблице 7. Средняя продолжительность наблюдения составила 1,8 года для пациентов в группе AC. → P и 2,0 года для пациентов в группе AC → PH.
Таблица 7 Сводка результатов эффективности объединенного анализа NSABP B-31 и NCCTG 9831 во время окончательного анализа DFS *
А: доксорубицин; С: циклофосфамид; Р: паклитаксел; H: трастузумаб
* При средней продолжительности наблюдения 1,8 года для пациентов в группе AC → P и 2,0 года для пациентов в группе AC → PH.
** Значение p для OS не превышало заранее установленный статистический предел для сравнения AC → PH по сравнению с AC → P.
По отношению к "конечная точка Первичный, DFS, добавление герцептина к химиотерапии паклитакселом привело к снижению риска рецидива заболевания на 52%. Соотношение рисков означает абсолютную пользу с точки зрения выживаемости без признаков заболевания через 3 года, равной 11,8% (87,2% против 75,4%). %) в пользу руки AC → PH (Герцептин).
Во время обновления безопасности, после среднего периода наблюдения 3,5–3,8 года, «анализ DFS подтвердил степень пользы, показанную в окончательном анализе DFS». переход Герцептина в контрольной группе, добавление Герцептина к химиотерапии паклитакселом привело к снижению риска рецидива заболевания на 52%. Добавление Герцептина к химиотерапии паклитакселом также привело к снижению рецидива заболевания на 37%. Риск смерти.
Предварительно запланированный окончательный анализ общей выживаемости на основе комбинированного анализа исследований NSABP B-31 и NCCTG 9831 был проведен на момент 707 смертей (средний период наблюдения 8,3 года в группе AC → PH). По сравнению с тем, что наблюдалось при лечении AC → P, лечение AC → PH привело к статистически значимому улучшению OS (стратифицированный HR = 0,64; 95% ДИ [0,55 - 0,74]; p-значение log-rank
Окончательные результаты OS из объединенного анализа NSABP B-31 и NCCTG 9831 суммированы в Таблице 8 ниже.
Таблица 8 Окончательный анализ общей выживаемости на основе комбинированного анализа NSABP B-31 и NCCTG 9831
А: доксорубицин; С: циклофосфамид; Р: паклитаксел; H: трастузумаб
Анализ DFS был также проведен в окончательном анализе OS, полученном в результате комбинированного анализа NSABP B-31 и NCCTG N9831. Обновленные результаты анализа DFS (стратифицированный HR = 0,61; 95% ДИ [0,54 - 0,69]) показали, что Преимущество DFS аналогично тому, которое наблюдалось в окончательном первичном анализе DFS, несмотря на то, что 24,8% пациентов в группе AC → P переходили на лечение Герцептином. Выживаемость без признаков заболевания составила 77,2% (95% ДИ: 75,4% - 79,1% ) в группе AC → PH оценивается в 8 лет с абсолютным преимуществом 11,8% по сравнению с группой AC → P.
В исследовании BCIRG 006 Герцептин вводили в комбинации с доцетакселом, после химиотерапии AC (AC → DH) или в комбинации с доцетакселом и карбоплатином (DCarbH).
Доцетаксел вводили следующим образом:
• внутривенное введение доцетаксела - 100 мг / м2 в виде 1-часовой внутривенной инфузии каждые 3 недели в течение 4 циклов (2-й день первого цикла доцетаксела, затем 1-й день каждого последующего цикла)
или
• внутривенный доцетаксел - 75 мг / м2 в виде 1-часовой внутривенной инфузии каждые 3 недели в течение 6 циклов (2-й день первого цикла, затем 1-й день каждого последующего цикла)
с последующим:
• карбоплатин - с целевой AUC = 6 мг / мл / мин, вводимый в виде внутривенной инфузии продолжительностью 30-60 минут, повторяемой каждые 3 недели, всего шесть циклов.
Герцептин назначался один раз в неделю в сочетании с химиотерапией, а затем каждые 3 недели в течение 52 недель.
Результаты эффективности BCIRG 006 суммированы в таблицах 9 и 10. Средняя продолжительность наблюдения составила 2,9 года в группе AC → D и 3,0 года в каждой из групп AC → DH и DCarbH.
Таблица 9 Резюме анализов эффективности из исследования BCIRG 006 AC → D против AC → DH
AC → D = доксорубицин в комбинации с циклофосфамидом, за которым следует доцетаксел; AC → DH = доксорубицин в комбинации с циклофосфамидом, за которым следует доцетаксел в комбинации с трастузумабом; ДИ = доверительный интервал.
Таблица 10 Резюме анализов эффективности из исследования BCIRG 006 AC → D против DCarbH
AC → D = доксорубицин в комбинации с циклофосфамидом, за которым следует доцетаксел; DCarbH = доцетаксел, карбоплатин и трастузумаб; ДИ = доверительный интервал
В исследовании BCIRG 006 относительно "конечная точка первичный, DFS, соотношение рисков приводит к абсолютному преимуществу с точки зрения 3-летней безрецидивной выживаемости в 5,8 процентных пункта (86,7% против 80,9%) в пользу группы AC → DH (Герцептин) и 4,6 процентных пункта. (85,5% против 80,9%) в пользу группы DCarbH (Герцептин) по сравнению с AC → D.
В исследовании BCIRG 006 213/1075 пациентов в группе DCarbH (TCH), 221/1074 пациентов в группе AC DH (AC TH) и 217/1073 в группе AC → D (AC T) имели статус производительности по Карновски. ≤90 (80 или 90). Никакого преимущества безрецидивной выживаемости (DFS) не наблюдалось в этой подгруппе пациентов (отношение рисков = 1,16; 95% ДИ [0,73, 1,83] для DCarbH (TCH) по сравнению с группой AC. D (AC T); отношение рисков 0,97; 95% ДИ [0,60, 1,55] для AC DH (AC TH) по сравнению с плечом AC D).
Кроме того, был проведен анализ постфактум исследовательские данные совместного анализа (JA) NSABP B-31 / NCCTG N9831 и клинического исследования BCIRG006, объединяющего DFS и симптоматические сердечные события, как обобщено в таблице 11:
Таблица 11 Анализ постфактум изучение результатов совместного анализа (JA) NSABP B-31 / NCCTG N9831 и клинического исследования BCIRG006, сочетающего DFS и симптоматические сердечные события
А: доксуробицин; С: циклофосфамид; Р: паклитаксел; D: доцетаксел; Карб: карбоплатин; H: трастузумаб
ДИ = доверительный интервал
* На момент окончательного анализа DFS Средняя продолжительность наблюдения составила 1,8 года в группе AC → P и 2,0 года в группе AC → PH.
Рак груди на ранней стадии (контекст неоадъювант-адъювант)
На сегодняшний день нет доступных результатов, сравнивающих эффективность Герцептина, вводимого с химиотерапией в режиме адъюванта, по сравнению с режимом неоадъювант / адъювант.
В контексте неоадъювантно-адъювантного лечения, исследование MO16432, многоцентровое рандомизированное клиническое исследование, было разработано для оценки клинической эффективности одновременного введения Герцептина с неоадъювантной химиотерапией, содержащей как антрациклин, так и таксан, с последующим применением Герцептина в качестве адъюванта вверх. до 1 года лечения. В исследование были включены пациенты с впервые выявленным местнораспространенным (стадия III) или воспалительным EBC. Пациенты с опухолями HER2 + были рандомизированы для получения неоадъювантной химиотерапии одновременно с неоадъювантной адъювантной химиотерапией герцептином или только неоадъювантной химиотерапией.
В исследовании MO16432 Герцептин (ударная доза 8 мг / кг, затем поддерживающая доза 6 мг / кг каждые 3 недели) вводили одновременно с 10 курсами неоадъювантной химиотерапии следующим образом:
• Доксорубицин 60 мг / м2 и паклитаксел 150 мг / м2, вводимые каждые 3 недели в течение 3 циклов,
с последующим
• Паклитаксел 175 мг / м2 вводится каждые 3 недели в течение 4 циклов,
с последующим
• CMF в 1-й и 8-й день каждые 4 недели в течение 3 циклов,
за которым после операции последовали
• дополнительные курсы адъювантного Герцептина (по окончании 1 года терапии).
Результаты исследования МО16432 приведены в таблице 12. Средняя продолжительность наблюдения в группе Герцептина составила 3,8 года.
Таблица 12 Результаты исследования эффективности из исследования MO16432
* определяется как отсутствие инвазивной карциномы в груди и подмышечных лимфатических узлах
Было оценено абсолютное преимущество в 13 процентных пунктов в пользу группы Герцептина с точки зрения 3-летней выживаемости без событий (65% против 52%).
Метастатический рак желудка
Герцептин изучался в рандомизированном открытом исследовании III фазы ToGA (BO18255) в сочетании с химиотерапией по сравнению с одной химиотерапией.
Химиотерапия проводилась следующим образом:
• капецитабин - 1000 мг / м2 перорально два раза в день в течение 14 дней каждые 3 недели в течение 6 циклов (с вечера 1 дня до утра 15 дня каждого цикла)
или
• Внутривенный 5-фторурацил - 800 мг / м2 / день в виде непрерывной внутривенной инфузии в течение 5 дней, каждые 3 недели в течение 6 циклов (дни с 1 по 5 каждого цикла).
Каждый из двух препаратов вводился с:
• цисплатин - 80 мг / м2 каждые 3 недели в течение 6 циклов, вводится в 1 день каждого цикла.
Результаты исследования эффективности BO18225 суммированы в Таблице 13:
Таблица 13 Результаты исследования эффективности BO18225
FP + H: фторпиримидин / цисплатин + герцептин
FP: фторпиримидин / цисплатин
отношение шансов
В исследование были включены пациенты, ранее не лечившиеся по поводу местнораспространенной или рецидивирующей и / или метастатической неоперабельной HER2-положительной аденокарциномы желудка или гастроэзофагеального перехода, не являющиеся кандидатами на лечебное лечение. L "конечная точка первичной была общая выживаемость, определяемая как время от даты рандомизации до даты смерти от любой причины. На момент анализа в общей сложности 349 рандомизированных пациентов умерли: 182 пациента (62,8%) в контрольной группе и 167 пациентов (56,8%) в группе лечения, связанных с основной опухолью.
Апостериорный анализ подгруппы показывает, что положительные эффекты лечения ограничиваются опухолями с более высокими уровнями белка HER2 (IHC 2 + / FISH + или IHC 3+). Средняя общая выживаемость в подгруппе с высокими уровнями сверхэкспрессии HER2 составила 11,8 месяцев против 16 месяцев, ОР 0,65 (95% ДИ 0,51-0,83) и выживаемость без прогрессирования составила 5,5 месяцев по сравнению с 7,6 месяцами, ОР 0,64 (95% ДИ 0,51-0,79) в группе FP по сравнению с группой FP + H, соответственно. общая выживаемость составила 0,75 (95% ДИ 0,51–1,11) в группе IHC2 + / FISH + и 0,58 (95% ДИ 0,41–0,81) в группе IHC3 + / FISH +.
В исследовательском анализе подгрупп, проведенном в исследовании ToGA (BO18255), не было очевидного улучшения общей выживаемости от добавления Герцептина у пациентов с исходным уровнем ECOG PS 2 [HR 0,96 (95% ДИ 0, 51–1,79)], не поддается измерению [ ОР 1,78 (95% ДИ 0,87–3,66)] и местнораспространенное [ОР 1,20 (95% ДИ 0,29–4,97)] заболевание.
Педиатрическая популяция
Европейское агентство по лекарственным средствам сняло обязательство по представлению результатов исследований Герцептина во всех подгруппах педиатрической популяции при раке желудка и груди (информацию о педиатрическом применении см. В разделе 4.2).
05.2 Фармакокинетические свойства
Фармакокинетика трастузумаба была оценена с помощью анализа фармакокинетической модели населения с использованием объединенных данных от 1582 субъектов с HER2-положительным MBC, EBC или распространенным раком желудка (AGC) или другими видами рака, а также здоровых добровольцев в 18 исследованиях фазы I, II и III. в котором Герцептин вводили внутривенно. Для описания профиля концентрация / время использовалась двухкомпонентная модель с параллельным линейным и нелинейным вымыванием из центрального отсека. Из-за нелинейного выведения общий клиренс увеличивался с уменьшением концентрации. Следовательно, невозможно определить постоянный период полувыведения трастузумаба. t1 / 2 уменьшается с уменьшением концентраций в диапазоне доз (см. Таблицу 16). Пациенты с MBC и EBC имели аналогичные значения фармакокинетических параметров [например, клиренс (CL), объем отсека к центральному (Vc), а население предсказало устойчивое воздействие (Cmin, Cmax и AUC)]. Линейный клиренс составлял 0,136 л / день для MBC, 0,112 л / день для EBC и 0,176 л / день для AGC. Значения параметров нелинейного выведения составляли 8,81 мг / день. Для максимальной скорости выведения (Vmax) и 8,92 мкг / мл для константы Михаэлиса-Ментен (Km) для пациентов с MBC, EBC и AGC. Объем центрального отделения составлял 2,62 л для пациентов с MBC и EBC и 3,63 л для пациентов с AGC. Последняя популяционная фармакокинетическая модель определила массу тела, сывороточный аспартатаминотрансферазу и альбумин как статистически ковариантные значимые эффекты, влияющие на экспозицию трастузумаба. Однако величина влияния этих ковариат на экспозицию трастузумаба предполагает маловероятный клинически значимый эффект на концентрацию трастузумаба.
Значения воздействия, предсказанные на основе фармакокинетики населения (медиана с 5-м по 95-й процентиль) и значений фармакокинетических параметров при клинически значимых концентрациях (Cmax и Cmin) для пациентов с MBC, EBC и AGC, получавших одобренные режимы дозирования. q1w (еженедельное дозирование) и q3w (дозирование каждые три недели) показаны в Таблице 14 (Цикл 1), Таблице 15 (устойчивое состояние) и Таблице 16 (фармакокинетические параметры).
Таблица 14 Прогнозируемые фармакокинетические значения воздействия на популяцию в цикле 1 (медиана 5-95-го процентиля) для схем Герцептина IV у пациентов с MBC, EBC и AGC
Таблица 15 Прогнозируемые значения фармакокинетической экспозиции в устойчивом состоянии (5-95-й процентиль) для схем герцептина IV у пациентов с MBC, EBC и AGC
* Cmin, ss - Cmin в установившемся режиме
** Cmax, ss = Cmax в установившемся режиме
*** время при 90% устойчивого состояния
Таблица 16 Прогнозируемые популяцией значения фармакокинетических параметров в устойчивом состоянии для внутривенных схем приема герцептина у пациентов с MBC, EBC и AGC
Вымывание трастузумаба
Период вымывания трастузумаба оценивали после внутривенного введения каждые 1 или 3 недели с использованием популяционной фармакокинетической модели. Результаты этого моделирования показывают, что по крайней мере 95% пациентов достигнут концентрации
Циркулирующий растворимый антиген
Исследовательский анализ ковариант с информацией только для одной подгруппы пациентов показал, что субъекты с более высокими уровнями растворимого антигена HER2-ECD (SHED) имели более быстрый (более низкий Km) нелинейный клиренс (p SGOT / AST; влияние растворимого антигена на клиренс связано с Уровни SGOT / AST.
Нет данных об уровне циркулирующего внеклеточного домена рецептора HER2 (растворимого антигена) в сыворотке крови больных раком желудка.
05.3 Доклинические данные по безопасности
Не было доказательств одноразовой или многократной дозозависимой токсичности в исследованиях продолжительностью до 6 месяцев, а также репродуктивной токсичности в исследованиях тератологии, женской плодовитости или токсичности в последнем периоде гестации / прохождения через плаценту. Герцептин не является генотоксичным. исследование трегалозы, одного из основных вспомогательных веществ препарата, не выявило какой-либо токсичности.
Долгосрочные исследования на животных не проводились для определения канцерогенного потенциала Герцептина или его влияния на мужскую фертильность.
06.0 ФАРМАЦЕВТИЧЕСКАЯ ИНФОРМАЦИЯ
06.1 Вспомогательные вещества
L-гистидина гидрохлорид
L-гистидин
а, дигидрат а-трегалозы
полисорбат 20
06.2 Несовместимость
Этот лекарственный препарат нельзя смешивать или разбавлять с другими лекарственными средствами, кроме упомянутых в разделе 6.6.
Не разбавляйте растворами глюкозы, так как они вызывают агрегацию белка.
06.3 Срок действия
4 года
После разбавления водой для инъекций восстановленный раствор остается физически и химически стабильным в течение 48 часов при температуре от 2 ° C до 8 ° C. Остатки восстановленного раствора необходимо выбросить.
Растворы герцептина для инфузий в поливинилхлоридных, полиэтиленовых или полипропиленовых пакетах, содержащие 9 мг / мл (0,9%) раствора натрия хлорида для инъекций, остаются физически и химически стабильными в течение 24 часов при температуре не выше 30 ° C.
С микробиологической точки зрения восстановленный раствор и инфузионный раствор Герцептина следует использовать немедленно. Продукт не следует хранить после восстановления и разбавления, если это не было сделано в контролируемых и утвержденных асептических условиях. Если продукт не используется сразу, ответственность за время и условия хранения несет пользователь.
06.4 Особые меры предосторожности при хранении
Хранить в холодильнике (2-8 ° C).
Условия хранения после первого открытия см. В разделах 6.3 и 6.6.
06.5 Характер непосредственной упаковки и содержимого упаковки
Герцептин флакон:
Один флакон объемом 15 мл из прозрачного стекла типа I с крышкой из ламинированного фторсодержащего полимера из бутилкаучука содержит 150 мг трастузумаба.
Каждая упаковка содержит один флакон.
06.6 Инструкции по эксплуатации и обращению
Придерживайтесь подходящих методов асептики. Каждый флакон Герцептина разводится 7,2 мл стерильной воды для инъекций (не входит в комплект). Избегайте использования других растворителей для восстановления. Это дает 7,4 мл одноразового раствора, содержащего примерно 21 мг / мл трастузумаба, с pH примерно 6,0. Избыток объема в 4% гарантирует аспирацию из флакона запрограммированного доза 150 мг.
С Герцептином следует обращаться осторожно во время процедуры восстановления. Чрезмерное пенообразование, вызванное восстановлением или встряхиванием восстановленного раствора, может вызвать проблемы с количеством Герцептина, которое может быть извлечено из флакона.
Восстановленный раствор нельзя замораживать.
Инструкции по восстановлению:
1) С помощью стерильного шприца медленно введите 7,2 мл воды для инъекций во флакон, содержащий лиофилизированный герцептин, направляя поток к лиофилизированному веществу.
2) Медленно покрутите флакон, чтобы облегчить восстановление. НЕ ТРЯЖИТЕСЬ!
Незначительное пенообразование во время восстановления не является чем-то необычным. Дайте флакону постоять примерно 5 минут. После восстановления Герцептин принимает вид прозрачного раствора от бесцветного до светло-желтого цвета без видимых частиц.
Определите необходимый объем раствора:
• на основе ударной дозы трастузумаба 4 мг / кг массы тела или последующей еженедельной дозы трастузумаба 2 мг / кг массы тела:
• исходя из ударной дозы трастузумаба 8 мг / кг массы тела или последующей дозы трастузумаба 6 мг / кг каждые 3 недели:
Достать необходимое количество раствора из флакона и добавить его в инфузионный мешок, содержащий 250 мл 0,9% раствора натрия хлорида. Не используйте растворы, содержащие глюкозу (см. Раздел 6.2). Пакет следует осторожно перевернуть, чтобы раствор перемешался и не вспенился. После приготовления настой следует вводить немедленно. В случае разведения в асептических условиях его можно хранить в течение 24 часов (при температуре ниже 30 ° C).
Перед введением растворы для парентерального введения следует визуально проверять на наличие каких-либо частиц или обесцвечивания.
Герцептин предназначен только для одноразового использования, так как продукт не содержит консервантов. Неиспользованные лекарства и отходы, полученные из этого лекарства, необходимо утилизировать в соответствии с местными правилами.
Между Герцептином и поливинилхлоридом, полиэтиленовыми или полипропиленовыми пакетами несовместимости не наблюдалось.
07.0 ДЕРЖАТЕЛЬ РАЗРЕШЕНИЯ НА МАРКЕТИНГ
Roche Registration Limited
6 Соколиный путь
Shire Park
Welwyn Garden City
AL7 1TW
Соединенное Королевство
08.0 НОМЕР РАЗРЕШЕНИЯ НА МАРКЕТИНГ
EU / 1/00/145/001
034949014
09.0 ДАТА ПЕРВОГО РАЗРЕШЕНИЯ ИЛИ ПРОДЛЕНИЯ РАЗРЕШЕНИЯ
Дата первого разрешения: 28 августа 2000 г.
Дата последнего обновления: 28 августа 2010 г.
10.0 ДАТА ПЕРЕСМОТРА ТЕКСТА
Сентябрь 2015 г.