Активные ингредиенты: кветиапин.
Кветиапин Милан 50 мг таблетки с пролонгированным высвобождением
Кветиапин Милан 150 мг таблетки пролонгированного действия
Кветиапин Милан 200 мг таблетки пролонгированного действия
Кветиапин Милан 300 мг таблетки пролонгированного действия
Кветиапин Милан 400 мг таблетки пролонгированного действия
Почему используется кветиапин - дженерик? Для чего это?
Кветиапин Милан содержит вещество под названием кветиапин. Это вещество относится к группе лекарств, называемых нейролептиками. Кветиапин Милан можно использовать для лечения нескольких заболеваний, например следующих:
- Биполярная депрессия и большие депрессивные эпизоды в контексте большого депрессивного расстройства: человек может чувствовать себя грустным, подавленным, виноватым, без энергии, без аппетита или с трудом засыпать.
- Мания: вы можете чувствовать себя очень возбужденным, находящимся в эйфории, возбуждении, энтузиазме или гиперактивности, или иметь плохие суждения, в том числе агрессивное или деструктивное поведение.
- Шизофрения: у человека возникает ощущение того, что он слышит или ощущает вещи, которых нет в действительности, он убеждается в вещах, которые не соответствуют истине, или он чувствует себя необычно подозрительным, тревожным, смущенным, виноватым, напряженным или подавленным.
Когда Кветиапин Милан принимается для лечения серьезных депрессивных эпизодов в контексте большого депрессивного расстройства, его следует использовать в дополнение к другому лекарству, показанному для лечения этого заболевания.
Ваш врач может продолжать назначать Кветиапин Милан, даже если вы почувствуете себя лучше.
Противопоказания при использовании кветиапина - дженерика
Не принимайте Кветиапин Милан:
- если у вас аллергия на кветиапин или какие-либо другие ингредиенты этого лекарства (перечислены в разделе 6)
- если вы принимаете какие-либо из следующих лекарств:
- некоторые лекарства от вируса ВИЧ
- препараты азола (при инфекциях, вызванных грибами)
- эритромицин или кларитромицин (от инфекций)
- нефазодон (от депрессии).
Не принимайте Кветиапин Милан, если он попадает в любую из категорий, описанных выше. Если вы не уверены, проконсультируйтесь с врачом или фармацевтом, прежде чем принимать Кветиапин Милан.
Меры предосторожности при использовании Что необходимо знать перед приемом кветиапина - дженерика
Перед приемом Кветиапина Милана проконсультируйтесь с врачом или фармацевтом, если:
- У вас или у кого-то из членов вашей семьи есть или когда-либо были проблемы с сердцем, например, нарушения сердечного ритма, или если вы принимаете какие-либо лекарства, которые могут повлиять на биение вашего сердца.
- У вас низкое кровяное давление.
- У него был инсульт, особенно если он пожилой.
- Страдает проблемами с печенью.
- У него были судороги (припадки).
- Страдают диабетом или подвержены риску развития диабета. В этом случае ваш врач может проверить уровень сахара в крови, пока вы принимаете Кветиапин Милан.
- Вы знаете, что в прошлом у вас был низкий уровень лейкоцитов (вызванный другими лекарствами или нет).
- Вы пожилой человек с деменцией (потеря определенных функций мозга). В этом случае вам не следует принимать Кветиапин Милан, потому что этот класс лекарств, к которому относится Кветиапин Милан, может увеличить риск инсульта, а в некоторых случаях риск смерти у пожилых пациентов с деменцией.
- У вас или у кого-то из членов вашей семьи в анамнезе были заболевания, связанные со сгустками крови, поскольку лекарства этого типа были связаны с образованием сгустков крови.
Немедленно обратитесь к врачу, если после приема Кветиапина Милана у вас возникнут следующие симптомы:
- Сочетание лихорадки, сильной жесткости мышц, потливости или низкого уровня сознания (заболевание, называемое «злокачественный нейролептический синдром»). Может потребоваться немедленная медицинская помощь.
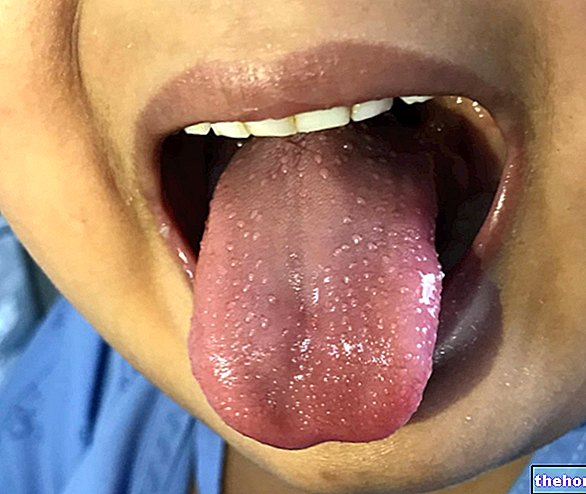
- Неконтролируемые движения, в основном лица или языка.
- Головокружение или сильное чувство сонливости. Это может увеличить риск случайных травм (падений) у пожилых пациентов.
- Судороги (припадки).
- Стойкая и болезненная эрекция (приапизм). Эти условия могут быть вызваны этим лекарством.
Обратитесь к врачу как можно скорее, если у вас возникли:
- Лихорадка, гриппоподобные симптомы, боль в горле или любая другая инфекция, поскольку они могут быть следствием очень низкого количества лейкоцитов, что может потребовать прекращения приема Кветиапина Милана и / или назначения лечения.
- Запор вместе с постоянной болью в животе или запором, который не поддается лечению, так как они могут привести к более серьезной кишечной непроходимости.
Мысли о самоубийстве и обострение депрессии
Если вы в депрессии, иногда у вас могут возникать мысли о том, чтобы навредить себе или убить себя. Эти чувства могут быть более интенсивными в начале лечения, так как этим лекарствам требуется время, чтобы подействовать, обычно около двух недель, но иногда и дольше. Эти мысли могут усилиться, даже если вы внезапно прекратите принимать лекарство.
Вероятность возникновения подобных ощущений выше у молодых людей. Данные клинических исследований показали повышенный риск суицидальных мыслей и / или суицидального поведения у молодых людей в возрасте до 25 лет, страдающих депрессией.
Если вам станет известно, что у вас есть мысли о причинении вреда или суицидальные наклонности, немедленно обратитесь к врачу или обратитесь в больницу. Возможно, вам будет полезно сказать родственнику или близкому другу, что у вас депрессия, и попросить их прочитать эту брошюру. Вы можете спросить их чтобы предупредить вас, если они думают, что ваше депрессивное состояние ухудшается, или если они обеспокоены некоторыми изменениями в вашем поведении.
Увеличение веса
Сообщалось об увеличении веса у пациентов, получавших кветиапин. Ваш вес тела должен регулярно проверяться и вами, и вашим врачом.
Дети и подростки
Кветиапин Милан не следует применять детям и подросткам в возрасте до 18 лет.
Взаимодействия Какие лекарства или продукты могут изменить действие кветиапина - дженерика
Сообщите своему врачу, если вы принимаете, недавно принимали или собираетесь принимать какие-либо другие лекарства, включая лекарства, отпускаемые без рецепта, и лекарственные травы.
Не принимайте Кветиапин Милан, если вы принимаете какие-либо из следующих лекарств:
- Некоторые лекарства от вируса ВИЧ.
- Азольные препараты (при инфекциях, вызванных грибками).
- Эритромицин или кларитромицин (от инфекций).
- Нефазодон (от депрессии).
Сообщите своему врачу, если вы принимаете какие-либо из следующих лекарств:
- Лекарства от эпилепсии (например, фенитоин или карбамазепин).
- Лекарства от высокого кровяного давления.
- Барбитураты (при нарушениях сна).
- Тиоридазин или литий (еще один антипсихотический препарат).
- Лекарства, влияющие на сердцебиение, например лекарства, которые могут вызвать дисбаланс электролитов (низкий уровень калия или магния), такие как диуретики (лекарства, увеличивающие выработку мочи) или некоторые антибиотики (лекарства для лечения инфекций).
- Лекарства, способные вызвать запор.
Прежде чем прекратить принимать какие-либо лекарства, поговорите со своим врачом.
Кветиапин Милан с пищей, напитками и алкоголем
- На Кветиапин Милан может повлиять еда, поэтому вам следует принимать таблетки по крайней мере за час до еды или перед сном.
- Обратите внимание на количество потребляемого алкоголя. Это важно, потому что совместное действие кветиапина милана и алкоголя может вызвать сонливость.
- Не пейте грейпфрутовый сок во время лечения Кветиапином Миланом, так как это может повлиять на действие лекарства.
Предупреждения Важно знать, что:
Беременность и кормление грудью
Если вы беременны, подозреваете, что беременны, планируете беременность или кормите грудью, перед приемом этого лекарства проконсультируйтесь с врачом или фармацевтом.
Вы не должны принимать Кветиапин Милан во время беременности, не посоветовавшись предварительно с врачом. Кветиапин Милан не следует принимать в период грудного вскармливания.
У новорожденных от матерей, принимавших кветиапин в течение последнего триместра (последних трех месяцев беременности), могут возникать следующие симптомы: дрожь, ригидность и / или слабость мышц, сонливость, возбуждение, проблемы с дыханием и трудности с приемом пищи. Если у вашего ребенка проявляются какие-либо из этих симптомов, обратитесь к врачу.
Вождение и использование машин
Таблетки вызывают сонливость. Не садитесь за руль и не используйте какие-либо инструменты или механизмы, пока не узнаете, какое действие на вас оказывают таблетки.
Влияние на скрининговые тесты мочи
Если вам необходимо пройти скрининговый анализ мочи, прием кветиапина может дать положительные результаты на метадон или некоторые лекарства от депрессии, называемые трициклическими антидепрессантами, когда используются определенные методы тестирования, даже если вы не принимаете метадон или трициклические антидепрессанты. тесты могут быть выполнены.
Доза, способ и время приема Как применять кветиапин - дженерик: дозировка
Всегда принимайте это лекарство точно так, как вам сказал врач. В случае сомнений проконсультируйтесь с врачом или фармацевтом. Ваш врач примет решение о вашей начальной дозе. Поддерживающая доза (суточная доза) будет зависеть от типа заболевания и индивидуальных потребностей, но обычно составляет от 150 до 800 мг.
- Таблетки необходимо принимать один раз в день.
- Таблетки нельзя разделять, жевать или измельчать.
- Глотать таблетки целиком, запивая небольшим количеством воды.
- Принимайте таблетки между приемами пищи (по крайней мере, за час до еды или перед сном, врач скажет вам, когда).
- Не пейте грейпфрутовый сок, пока вы принимаете кветиапин милан, так как это может повлиять на действие лекарства.
- Не прекращайте прием таблеток, даже если вы чувствуете себя лучше, если только ваш врач не скажет вам об этом.
Проблемы с печенью
Если у вас проблемы с печенью, ваш врач может изменить дозу.
Пожилые граждане
Если вы пожилой человек, ваш врач может изменить вашу дозу.
Применение у детей и подростков до 18 лет.
Кветиапин Милан не следует применять детям и подросткам в возрасте до 18 лет.
Передозировка Что делать, если вы приняли передозировку кветиапина - дженерика
Если вы приняли больше Кветиапина Милана, чем предусмотрено
Если вы приняли больше Кветиапина Милана, чем предписано врачом, вы можете почувствовать сонливость, головокружение и аномальное сердцебиение. Немедленно обратитесь к врачу или в ближайшую больницу. Возьмите с собой таблетки Кветиапин Милан.
Если вы забыли принять Кветиапин Милан
Если вы забыли принять дозу, примите ее, как только вспомните. Если уже почти пора принять следующую дозу, дождитесь назначенного времени.Не принимайте двойную дозу, чтобы восполнить пропущенную дозу.
Если вы перестанете принимать Кветиапин Милан
Если вы внезапно прекратите прием Кветиапина Милана, у вас могут возникнуть проблемы со сном (бессонница), тошнота (тошнота) или головная боль, диарея, тошнота (рвота), головокружение или раздражительность. Ваш врач может посоветовать вам постепенно снижать дозу перед прекращением лечения.
Если у вас есть дополнительные вопросы по использованию этого лекарства, спросите своего врача или фармацевта.
Побочные эффекты Каковы побочные эффекты кветиапина - дженерика?
Как и все лекарства, это лекарство может вызывать побочные эффекты, хотя они возникают не у всех. Если какой-либо из побочных эффектов станет серьезным или если вы заметите какие-либо побочные эффекты, не указанные в этой брошюре, обратитесь к своему врачу или фармацевту.
Очень часто (им может быть подвержено более 1 человека из 10):
- Головокружение (которое может вызвать падение), головная боль, сухость во рту.
- Чувство сонливости (которое может исчезнуть со временем, если вы продолжите лечение Кветиапином Миланом) (что может привести к падению)
- Симптомы абстиненции (симптомы, которые появляются после прекращения приема Кветиапина Милана), которые включают бессонницу (бессонницу), плохое самочувствие (тошноту), головную боль, диарею, тошноту (рвоту), головокружение и раздражительность. Рекомендуется постепенная отмена лекарства в течение как минимум 1-2 недель.
- Увеличение веса
- Аномальные мышечные движения, которые включают затруднения при запуске мышечных движений, тремор, чувство беспокойства или жесткости мышц без боли.
- Изменения количества определенных жиров в крови (триглицеридов и общего холестерина).
Часто (им может быть подвержено до 1 человека из 10):
- Быстрое сердцебиение
- Ощущение, что сердце колотится, сильно бьется или ощущение пропуска ударов
- Запор, расстройство желудка (несварение желудка)
- Чувство слабости
- Отек рук или ног
- Низкое артериальное давление при вставании. Это может вызвать головокружение или обморок (что может привести к падению).
- Повышенный уровень сахара в крови
- Затуманенное зрение
- Ненормальные сны и кошмары
- Повышенное чувство голода
- Раздражительность
- Нарушения в разговоре и речи
- Мысли о самоубийстве и обострение депрессии
- Хрипы
- Рвота (особенно у пожилых пациентов)
- Высокая температура
- Изменения количества гормонов щитовидной железы в крови
- Уменьшение количества определенных типов клеток крови
- Увеличение количества ферментов печени, измеряемых в крови
- Повышение уровня гормона пролактина в крови. Повышение уровня гормона пролактина в редких случаях может иметь следующие последствия:
- Увеличение груди и неожиданное производство молока из молочной железы как у мужчин, так и у женщин.
- Отсутствие или нарушение менструального цикла у женщин.
Нечасто (им может быть подвержено до 1 человека из 100):
- Судороги или припадки
- Аллергические реакции, которые могут включать синяки (синяки) на коже, отек кожи и области вокруг рта.
- Неприятное ощущение в ногах (также называемое синдромом беспокойных ног)
- Затруднение глотания
- Неконтролируемые движения, в основном лица или языка
- Сексуальные дисфункции
- Диабет
- Изменения электрической активности сердца на ЭКГ (удлинение интервала QT)
- Более медленная, чем обычно, частота сердечных сокращений, которая может возникнуть в начале лечения и может быть связана с низким артериальным давлением и обмороком.
- Затрудненное мочеиспускание
- Обморок (может вызвать падение)
- Заложенный нос
- Уменьшение количества эритроцитов в крови
- Уменьшение количества натрия в крови.
Редко (им может быть подвержено до 1 человека из 1000):
- Высокая температура тела (лихорадка), связанная с потоотделением, ригидностью мышц, повышенным чувством онемения или обморока (заболевание, называемое «злокачественный нейролептический синдром»).
- Пожелтение кожи и глаз (желтуха)
- Воспаление печени (гепатит)
- Длительная и болезненная эрекция (приапизм)
- Набухание груди и неожиданное выделение молока из железы (галакторея)
- Нарушения менструального цикла
- Сгустки крови в венах, особенно в ногах (симптомы включают отек, боль и покраснение в ногах), которые могут перемещаться по кровеносным сосудам в легкие, вызывая боль в груди и затруднение дыхания. Если вы заметили какой-либо из этих симптомов, немедленно обратитесь к врачу.
- Гулять, разговаривать, есть или заниматься другими делами во время сна
- Падение температуры тела (переохлаждение)
- Воспаление поджелудочной железы.
- Состояние (называемое «метаболическим синдромом»), при котором у вас может быть комбинация из 3 или более следующих симптомов: увеличение жира вокруг «живота», снижение «хорошего холестерина» (Х-ЛПВП), повышение одного типа жирность крови, вызываемая триглицеридами, повышение артериального давления и повышение уровня сахара в крови.
- Сочетание лихорадки, гриппоподобных симптомов, боли в горле или любой другой инфекции с очень низким количеством лейкоцитов, состояние, называемое агранулоцитозом.
- Кишечная непроходимость
- Повышение уровня креатинфосфокиназы (вещества, обнаруживаемого в мышцах).
Очень редко (им может быть подвержено до 1 человека из 10000):
- Сильная сыпь, волдыри или красные пятна на коже
- Тяжелая аллергическая реакция (называемая анафилаксией), которая может вызвать затруднение дыхания или шок.
- Быстрый отек кожи, обычно в области глаз, губ и горла (ангионевротический отек)
- Серьезное состояние с образованием волдырей на коже, рту, глазах и гениталиях (синдром Стивенса-Джонсона).
- Несоответствующая секреция антидиуретического гормона, контролирующего объем мочи.
- Разрушение мышечных волокон и мышечные боли (рабдомиолиз)
- Ухудшение ранее существовавшего диабета.
Частота неизвестна (частота не может быть оценена на основе имеющихся данных)
- Сыпь с нерегулярными красными пятнами (многоформная эритема)
- Внезапная тяжелая аллергическая реакция с такими симптомами, как лихорадка, образование волдырей и шелушение кожи (токсический эпидермальный некролиз)
- Симптомы отмены могут возникать у новорожденных от матерей, принимавших Кветиапин Милан во время беременности.
Класс лекарств, к которому принадлежит Кветиапин Милан, может вызывать проблемы с сердечным ритмом, которые могут быть серьезными, а в некоторых серьезных случаях могут привести к летальному исходу.
Некоторые побочные эффекты видны только после сдачи анализа крови. К ним относятся изменения количества определенных жиров (триглицеридов и общего холестерина) или сахаров, присутствующих в крови, изменения уровня гормонов щитовидной железы в крови, повышение ферментов печени, уменьшение количества определенных типов клеток крови, уменьшение количества красных кровяных телец, увеличивается креатинфосфокиназа сыворотки (вещество, обнаруживаемое в мышцах), уменьшается количество натрия в крови и увеличивается количество гормона пролактина в крови.
Повышение уровня гормона пролактина в редких случаях может иметь следующие последствия:
- Увеличение груди и неожиданное производство молока из молочной железы как у мужчин, так и у женщин.
- Отсутствие или нарушение менструального цикла у женщин.
Затем ваш врач время от времени будет назначать анализы крови.
Нежелательные эффекты у детей и подростков
Те же побочные эффекты, которые наблюдаются у взрослых, также могут возникать у детей и подростков.
Следующие побочные эффекты чаще наблюдались у детей и подростков или не наблюдались у взрослых:
Очень часто (им может быть подвержено более 1 человека из 10):
- Повышенный уровень гормона пролактина в крови. Такое увеличение количества пролактина в редких случаях может привести к следующим состояниям:
- Увеличение груди и неожиданное производство молока из молочной железы у мальчиков и девочек.
- Отсутствие или нерегулярность менструального цикла у девочек
- Повышенный аппетит
- Его рвало
- Аномальные мышечные движения, в том числе трудности с началом мышечных движений, тремор, чувство беспокойства или жесткость мышц без боли
- Повышенное артериальное давление.
Часто (им может быть подвержено до 10 человек):
- Чувство слабости, обморока (может вызвать падение)
- Заложенный нос
- Раздражительность.
Сообщение о побочных эффектах
Если вы заметили какие-либо побочные эффекты, обратитесь к врачу или фармацевту, включая любые возможные побочные эффекты, не указанные в данном информационном листке. Вы также можете сообщить о побочных эффектах напрямую через национальную систему отчетности по адресу https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
Сообщая о побочных эффектах, вы можете предоставить больше информации о безопасности этого лекарства.
Срок действия и удержание
Храните это лекарство в недоступном для детей месте.
Не используйте это лекарство по истечении срока годности, указанного на упаковке после «EXP». Срок годности относится к последнему дню этого месяца.
Кветиапин Милан не требует особых условий хранения.
Не выбрасывайте лекарства в сточные воды или бытовые отходы. Спросите своего фармацевта, как утилизировать лекарства, которые вы больше не используете. Это поможет защитить окружающую среду.
Что содержит Кветиапин Милан
- Действующее вещество - кветиапин. Кветиапин Милан содержит 50, 150, 200, 300 или 400 мг кветиапина (в виде кветиапина фумарата).
- Остальные ингредиенты:
Ядро таблетки: гипромеллоза 2910, гипромеллоза 2208, микрокристаллическая целлюлоза, безводный цитрат натрия, стеарат магния.
Покрытие таблеток: диоксид титана (E171), гипромеллоза 2910, макрогол / ПЭГ 400, полисорбат 80. Таблетки 50, 200 и 300 мг содержат желтый оксид железа (E172) и красный оксид железа (E172). Таблетки 50 мг и 300 мг также содержат черный оксид железа (E172).
Как выглядит Кветиапин Милан и что содержится в упаковке
Все формы таблеток Кветиапина Милана с пролонгированным высвобождением представляют собой таблетки в форме капсул с пленочным покрытием.
Таблетки по 50 мг коричневого цвета, с тиснением Q 50 с одной стороны и гладкими с другой.
Таблетки по 150 мг белого цвета с тиснением «Q 150» с одной стороны и гладкими с другой.
Таблетки по 200 мг желтого цвета, с тиснением «Q 200» с одной стороны и гладкими с другой.
Таблетки по 300 мг светло-желтого цвета, с тиснением «Q 300» с одной стороны и гладкими с другой.
Таблетки по 400 мг белого цвета с тиснением Q 400 с одной стороны и гладкими с другой.
- PVC / Aclar - Алюминиевые блистеры в картонных коробках.
50 мг: 10, 10x1 (стандартная доза с перфорированным блистером), 30, 30x1 (стандартная доза с перфорированным блистером), 60 или 60x1 (стандартная доза с перфорированным блистером) таблеток пролонгированного действия.
150 мг: 30, 30x1 (стандартная доза с перфорированным блистером), 60 или 60x1 (стандартная доза с перфорированным блистером) таблеток пролонгированного действия.
200 мг: 10, 10x1 (стандартная доза с перфорированным блистером), 30, 30x1 (стандартная доза с перфорированным блистером), 60, 60x1 (стандартная доза с перфорированным блистером), 100 или 100x1 (стандартная доза с перфорированным блистером) таблетки пролонгированного действия .
300 мг: 10, 10x1 (стандартная доза с перфорированным блистером), 30, 30x1 (стандартная доза с перфорированным блистером), 60, 60x1 (стандартная доза с перфорированным блистером), 100 или 100x1 (стандартная доза с перфорированным блистером) таблетки пролонгированного действия .
400 мг: 10, 10x1 (стандартная доза с перфорированным блистером), 30, 30x1 (стандартная доза с перфорированным блистером), 60, 60x1 (стандартная доза с перфорированным блистером), 100 или 100x1 (стандартная доза с перфорированным блистером) таблетки пролонгированного действия .
- Контейнеры ПНД по 60 таблеток.
Не все размеры упаковки могут быть проданы.
Листовка с исходным кодом: AIFA (Итальянское агентство по лекарственным средствам). Контент опубликован в январе 2016 года. Представленная информация может быть устаревшей.
Чтобы иметь доступ к самой последней версии, рекомендуется зайти на сайт AIFA (Итальянское агентство по лекарственным средствам). Заявление об ограничении ответственности и полезная информация.
01.0 НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
Таблетки пролонгированного высвобождения QUETIAPINA MYLAN
02.0 КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ
Каждая таблетка 50 мг содержит 50 мг кветиапина (в виде кветиапина фумарата).
Каждая таблетка 150 мг содержит 150 мг кветиапина (в виде кветиапина фумарата).
Каждая таблетка 200 мг содержит 200 мг кветиапина (в виде кветиапина фумарата).
Каждая таблетка 300 мг содержит 300 мг кветиапина (в виде кветиапина фумарата).
Каждая таблетка 400 мг содержит 400 мг кветиапина (в виде кветиапина фумарата).
Полный список вспомогательных веществ см. В разделе 6.1.
03.0 ФАРМАЦЕВТИЧЕСКАЯ ФОРМА
Таблетка пролонгированного действия.
50 мг: таблетки коричневого цвета, покрытые пленочной оболочкой, капсулы, с тиснением «Q 50» с одной стороны и гладкие с другой.
150 мг: белые таблетки в форме капсул, покрытые пленочной оболочкой, с тиснением «Q 150» с одной стороны и гладкие с другой.
200 мг: желтые таблетки в форме капсул, покрытые пленочной оболочкой, с тиснением «Q 200» с одной стороны и гладкие с другой.
300 мг: светло-желтые таблетки в форме капсул, покрытые пленочной оболочкой, с тиснением «Q 300» с одной стороны и гладкими с другой.
400 мг: Белые таблетки в форме капсул, покрытые пленочной оболочкой, с тиснением «Q 400» с одной стороны и гладкие с другой.
04.0 КЛИНИЧЕСКАЯ ИНФОРМАЦИЯ
04.1 Терапевтические показания
Кветиапин Милан показан при:
• лечение шизофрении,
• лечение биполярного расстройства:
• для лечения умеренных и тяжелых маниакальных эпизодов, связанных с биполярным расстройством.
• для лечения тяжелых депрессивных эпизодов, связанных с биполярным расстройством
• для предотвращения рецидивов у пациентов с биполярным расстройством, у пациентов, у которых маниакальный или депрессивный эпизод отреагировал на лечение кветиапином.
• дополнительное лечение эпизодов большой депрессии у пациентов с большим депрессивным расстройством (БДР), у которых был неоптимальный ответ на монотерапию антидепрессантами (см. Раздел 5.1). Перед началом лечения врачи должны рассмотреть профиль безопасности кветиапина (см. Раздел 4.4).
04.2 Дозировка и способ применения
Дозировка
Для каждого показания существуют разные графики дозирования. Поэтому необходимо гарантировать, что пациенты получают четкую информацию о наиболее подходящей дозировке для их состояния.
Взрослые
Для лечения шизофрении и маниакальных эпизодов средней и тяжелой степени, связанных с биполярным расстройством.
Кветиапин Милан следует вводить как минимум за час до еды. Суточная доза в начале терапии составляет 300 мг в 1-й день и 600 мг во 2-й день. Рекомендуемая суточная доза составляет 600 мг, однако, если это клинически оправдано, дозировка можно увеличить до 800 мг в сутки. Дозу следует корректировать в пределах эффективного диапазона доз от 400 мг до 800 мг в день, в зависимости от клинического ответа и переносимости пациента. Для поддерживающей терапии шизофрении коррекции дозировки не требуется.
Для лечения депрессивных эпизодов, связанных с биполярным расстройством.
Кветиапин Майлан следует назначать вечером перед сном. Общая суточная доза в течение первых четырех дней терапии составляет 50 мг (день 1), 100 мг (день 2), 200 мг (день 3) и 300 мг (день 4). Рекомендуемая суточная доза - 300 мг. В клинических исследованиях не наблюдалось дополнительных преимуществ в группе пациентов, получавших дозу 600 мг, по сравнению с пациентами, получавшими дозу 300 мг (см. Раздел 5.1). Отдельным пациентам может помочь лечение дозой 600 мг. Дозы выше 300 мг должны назначаться врачами, имеющими опыт лечения биполярного расстройства. У отдельных пациентов, в случае проблем с переносимостью, клинические исследования показали, что можно рассмотреть возможность снижения дозы до минимум 200 мг.
Для профилактики рецидивов биполярного расстройства.
Чтобы предотвратить рецидив маниакальных, смешанных или депрессивных эпизодов биполярного расстройства, пациенты, принимающие кветиапин милан для острого лечения биполярного расстройства, должны продолжать терапию кветиапином миланом в той же дозировке, которую давали перед сном. Доза кветиапина Mylan может быть скорректирована в зависимости от клинического ответа и переносимости отдельного пациента в диапазоне от 300 мг до 800 мг / день. Для поддерживающей терапии важно использовать самую низкую эффективную дозу.
Для дополнительного лечения эпизодов большой депрессии, связанных с БДР:
Кветиапин Майлан следует назначать вечером перед сном. Суточная доза в начале терапии составляет 50 мг в дни 1 и 2 и 150 мг в дни 3 и 4. Антидепрессивный эффект наблюдался при дозах 150 и 300 мг / день в краткосрочных клинических испытаниях в качестве терапии. (с амитриптилином, бупропионом, циталопрамом, дулоксетином, эсциталопрамом, флуоксетином, пароксетином, сертралином и венлафаксином - см. раздел 5.1) и в дозе 50 мг / день в краткосрочных клинических исследованиях монотерапии. При более высоких дозах повышается риск нежелательных явлений. Поэтому врачи должны убедиться, что используется самая низкая эффективная доза для лечения, начиная с 50 мг / день. Необходимость увеличения дозы со 150 до 300 мг / сут должна основываться на индивидуальной оценке пациента.
Переход с таблеток кветиапина с немедленным высвобождением:
Для более удобного дозирования пациенты, которые в настоящее время получают разделенные дозы таблеток кветиапина с немедленным высвобождением, могут быть переведены на лечение кветиапином миланом в эквивалентной общей суточной дозе, вводимой один раз в день. Может потребоваться индивидуальная корректировка дозировки.
Пожилые граждане
Как и другие нейролептики и антидепрессанты, Кветиапин Милан следует с осторожностью назначать пациентам пожилого возраста, особенно на начальных этапах лечения. Постепенное повышение дозы кветиапина милана может потребоваться медленнее, а суточную терапевтическую дозу, возможно, придется снизить по сравнению с более молодыми пациентами. Средний клиренс кветиапина из плазмы был снижен на 30-50% у пожилых пациентов по сравнению с более молодыми пациентами Начальная доза для пожилых пациентов - 50 мг / день. Доза может быть увеличена с шагом 50 мг / день до эффективной дозы, в зависимости от клинического ответа и переносимости индивидуального пациента.
У пожилых пациентов с большими депрессивными эпизодами, связанными с DDM, начальная доза должна составлять 50 мг / день в дни 1-3, увеличиваясь до 100 мг / день в день 4 и 150 мг / день в день 8. Следует использовать дозу. минимально эффективный, начиная с 50 мг / сут. Если по индивидуальной оценке пациента требуется увеличение дозы до 300 мг / сут, это следует делать не ранее 22 дня лечения.
Эффективность и безопасность не оценивались у пациентов старше 65 лет с депрессивными эпизодами, связанными с биполярным расстройством.
Педиатрическая популяция
Кветиапин Милан не следует применять детям и подросткам моложе 18 лет из-за отсутствия данных, подтверждающих его использование в этой возрастной группе. Имеющиеся в настоящее время данные плацебо-контролируемых клинических испытаний представлены в разделах 4.4, 4.8, 5.1 и 5.2.
Повреждение почек
У пациентов с почечной недостаточностью корректировка дозы не требуется.
Печеночная недостаточность
Кветиапин широко метаболизируется в печени. Таким образом, Кветиапин Милан следует применять с осторожностью пациентам с печеночной недостаточностью, особенно на начальных этапах лечения. Начальная доза для пациентов с нарушением функции печени должна составлять 50 мг / сут. Дозу можно корректировать с шагом 50 мг / день, пока не будет достигнута эффективная доза, в зависимости от клинического ответа и переносимости каждого отдельного пациента.
Способ применения
Кветиапин Милан следует принимать один раз в день между приемами пищи. Таблетки следует глотать целиком, а не разделять, разжевывать или измельчать.
04.3 Противопоказания
Повышенная чувствительность к действующему веществу или любому из вспомогательных веществ, перечисленных в разделе 6.1.
Противопоказано одновременное применение ингибиторов цитохрома P450 3A4, таких как ингибиторы протеазы ВИЧ, азольные противогрибковые средства, эритромицин, кларитромицин и нефазодон (см. Раздел 4.5).
04.4 Особые предупреждения и соответствующие меры предосторожности при использовании
Поскольку Кветиапин Милан имеет несколько показаний, следует принимать во внимание профиль безопасности препарата с учетом индивидуального диагноза пациента и вводимой дозы.
Долгосрочная эффективность и безопасность у пациентов с СДД не оценивались при дополнительной терапии, однако долгосрочная эффективность и безопасность оценивались у взрослых пациентов, получающих монотерапию (см. Раздел 5.1).
Педиатрическая популяция
Кветиапин не рекомендуется применять детям и подросткам младше 18 лет из-за отсутствия данных, подтверждающих его применение в этой возрастной группе.
Клинические исследования кветиапина показали, что в дополнение к известному профилю безопасности, наблюдаемому у взрослых (см. Раздел 4.8), некоторые побочные эффекты возникали с большей частотой у детей и подростков, чем у взрослых (повышенный аппетит, повышенный сывороточный пролактин, рвота, ринит и др.). обморок) или может иметь разные последствия для детей и подростков (экстрапирамидные симптомы и раздражительность), в то время как было выявлено одно, о котором ранее не сообщалось в исследованиях взрослых (повышение артериального давления). Изменения в тестах функции щитовидной железы также наблюдались у детей и подростки.
Кроме того, не изучалось долгосрочное влияние лечения кветиапином на рост и созревание после 26 недель. Долгосрочные последствия для когнитивного и поведенческого развития неизвестны.
В плацебо-контролируемых клинических испытаниях у детей и подростков кветиапин был связан с «повышенной частотой экстрапирамидных симптомов (ЭПС) по сравнению с плацебо у пациентов, лечившихся от шизофрении и биполярной мании (см. Раздел 4.8).
Суицид / суицидальные мысли или клиническое ухудшение
Депрессия связана с повышенным риском суицидальных мыслей, членовредительства и суицида (событий, связанных с самоубийством). Этот риск сохраняется до значительной ремиссии. Поскольку это улучшение может не наступить в течение первых нескольких недель или более лечения, за пациентами следует внимательно наблюдать, пока такое улучшение не будет достигнуто. Из общего клинического опыта было замечено, что риск суицида может увеличиваться на ранних стадиях улучшения.
Кроме того, врачи должны учитывать потенциальный риск суицидальных событий после резкого прекращения лечения кветиапином из-за известных факторов риска рассматриваемого состояния.
Другие психические расстройства, при которых назначают кветиапин, также могут быть связаны с повышенным риском суицидальных событий. В дополнение к этому, эти состояния могут существовать при сопутствующих заболеваниях с большими депрессивными эпизодами. Поэтому те же меры предосторожности, которые соблюдаются при лечении пациентов с большими депрессивными эпизодами, следует применять при лечении пациентов с другими психическими расстройствами.
Известно, что пациенты, у которых в анамнезе были события, связанные с суицидом, или те, у кого была значительная степень суицидальных мыслей до начала лечения, подвержены повышенному риску суицидальных мыслей или попытки самоубийства, и поэтому во время лечения должны находиться под тщательным наблюдением. Метаанализ плацебо-контролируемых клинических испытаний антидепрессантов у взрослых пациентов с психическими расстройствами показал повышенный риск суицидального поведения при использовании антидепрессантов по сравнению с плацебо у пациентов младше 25 лет.
Во время терапии следует проводить тщательный мониторинг пациентов, особенно из группы высокого риска, особенно на начальных этапах лечения и после изменения дозы. Пациенты (и лица, осуществляющие уход) должны быть предупреждены о необходимости отслеживать любое клиническое ухудшение, суицидальное поведение или мысли и необычные изменения в поведении, а также немедленно обращаться за медицинской помощью при появлении таких симптомов.
В краткосрочных плацебо-контролируемых клинических испытаниях с участием пациентов с большими депрессивными эпизодами, связанными с биполярным расстройством, у молодых взрослых пациентов (менее 25 лет), получавших кветиапин, наблюдался более высокий риск суицидальных событий, чем у пациентов, получавших лечение. с плацебо (3,0% против 0% соответственно). В клинических испытаниях пациентов с БДР частота суицидальных событий, наблюдаемых у молодых взрослых пациентов (младше 25 лет), составляла 2,1% (3/144) для кветиапина и 1,3% (1/75) для плацебо.
Метаболический риск
В связи с наблюдаемым риском ухудшения метаболического профиля, включая возможные изменения массы тела, уровня глюкозы в крови (см. Гипергликемия) и липидов, наблюдаемых в клинических исследованиях, метаболические параметры пациентов следует оценивать во время начала лечения и изменения этих параметров. следует регулярно контролировать в ходе лечения.Ухудшение этих параметров следует контролировать в соответствии с клинической практикой (см. также раздел 4.8).
Экстрапирамидные симптомы
В плацебо-контролируемых клинических испытаниях с участием взрослых пациентов, лечившихся от эпизодов большой депрессии, связанных с биполярным расстройством и большим депрессивным расстройством, кветиапин был связан с повышенной частотой экстрапирамидных симптомов (EPS) по сравнению с плацебо (см. Разделы 4.8 и 5.1).
Использование кветиапина связано с развитием акатизии, характеризующейся субъективно неприятным или тревожным возбуждением и потребностью в движении, часто сопровождающейся неспособностью сидеть или стоять на месте. Скорее всего, это произойдет в течение первых нескольких недель лечения. У пациентов, которые испытывают эти симптомы, увеличение дозы может быть вредным.
Поздняя дискинезия
При появлении признаков и симптомов поздней дискинезии следует рассмотреть возможность уменьшения дозировки или прекращения терапии кветиапином. Симптомы поздней дискинезии могут ухудшиться или даже возникнуть после прекращения лечения (см. Раздел 4.8).
Сонливость и головокружение
Лечение кветиапином ассоциируется с сонливостью и сопутствующими симптомами, такими как седативный эффект (см. Раздел 4.8). В клинических испытаниях по лечению пациентов с биполярной депрессией и большим депрессивным расстройством начало этого явления обычно происходит в течение первых 3 дней лечения и обычно бывает легкой или умеренной по интенсивности. Пациенты, испытывающие сильную сонливость, могут нуждаться в более частых проверках. минимум 2 недели с момента появления сонливости или до улучшения симптомов, и следует рассмотреть возможность прекращения лечения.
Ортостатическая гипотензия
Лечение кветиапином связано с соответствующей ортостатической гипотензией и головокружением (см. Раздел 4.8), которые, как и сонливость, обычно возникают во время начальной фазы титрования дозы. Это может увеличить количество случайных травм (падений), особенно у пожилых людей. Поэтому пациентам следует рекомендовать проявлять осторожность, пока они не узнают о потенциальных эффектах препарата.
Кветиапин следует с осторожностью назначать пациентам с сердечно-сосудистыми заболеваниями, цереброваскулярными заболеваниями или другими состояниями, предрасполагающими к гипотензии. При возникновении ортостатической гипотензии следует рассмотреть возможность снижения дозы или более постепенного титрования, особенно у пациентов с сердечно-сосудистыми заболеваниями. Ниже.
Судороги
Контролируемые клинические испытания не выявили различий в частоте приступов у пациентов, получавших кветиапин или плацебо. Данных о частоте приступов у пациентов с припадками в анамнезе нет. Как и в случае с другими нейролептиками, рекомендуется соблюдать осторожность при лечении пациентов с припадками в анамнезе (см. Раздел 4.8).
Нейролептический злокачественный синдром
Злокачественный нейролептический синдром был связан с лечением антипсихотическими препаратами, включая кветиапин (см. Раздел 4.8). Клинические проявления включают гипертермию, измененное психическое состояние, жесткость мышц, вегетативную нестабильность и повышение уровня креатинфосфокиназы. В таких обстоятельствах прием кветиапина следует прекратить и назначить соответствующую медикаментозную терапию.
Тяжелая нейтропения и агранулоцитоз
В клинических испытаниях кветиапина нечасто сообщалось о тяжелой нейтропении (количество лейкоцитов и нейтропения в анамнезе), однако некоторые случаи имели место у пациентов без ранее существовавших факторов риска.
Прием кветиапина следует прекратить у пациентов с числом нейтрофилов для выявления признаков и симптомов инфекции, а также следует регулярно контролировать число нейтрофилов (до тех пор, пока не будут превышены значения 1,5 x 109 / л) (см. Раздел 5.1).
Нейтропению следует рассматривать у пациентов с инфекцией или лихорадкой, особенно при отсутствии явных предрасполагающих факторов, и лечить ее в соответствии с клинической практикой.
Пациентам следует рекомендовать немедленно сообщать о признаках / симптомах, связанных с «агранулоцитозом» или инфекцией (например, лихорадка, слабость, летаргия или боль в горле) в любое время во время терапии Кветиапином Миланом.У таких пациентов следует незамедлительно проводить подсчет лейкоцитов и абсолютное количество нейтрофилов (АНН), особенно при отсутствии предрасполагающих факторов.
Взаимодействия
См. Также раздел 4.5.
Одновременное применение кветиапина с мощными индукторами печеночных ферментов, такими как карбамазепин или фенитоин, существенно снижает плазменные концентрации кветиапина, что, возможно, влияет на эффективность терапии кветиапином. У пациентов, получающих индукторы печеночных ферментов, лечение кветиапином следует начинать только в том случае, если врач считает, что преимущества терапии кветиапином перевешивают риски прекращения приема индукторов печеночных ферментов. Важно, чтобы любое изменение индуктора было постепенным и, при необходимости, заменялось лекарственным средством, не являющимся индуктором (например, вальпроатом натрия).
Масса тела
Сообщалось об увеличении массы тела у пациентов, получавших кветиапин; Пациенты должны находиться под наблюдением и лечиться в соответствии с клиническими показаниями в соответствии с рекомендациями по применяемым антипсихотическим средствам (см. разделы 4.8 и 5.1).
Гипергликемия
О гипергликемии и / или развитии или обострении диабета, иногда связанного с кетоацидозом или комой, сообщалось редко, включая некоторые случаи со смертельным исходом (см. Раздел 4.8). В некоторых случаях предрасполагающим фактором может быть предыдущее увеличение массы тела. Рекомендуется надлежащий клинический мониторинг в соответствии с руководящими принципами применяемого нейролептика. Пациенты, принимающие любые антипсихотические препараты, включая кветиапин, должны находиться под наблюдением на предмет возможных признаков и симптомов гипергликемии (таких как полидипсия, полиурия, полифагия и слабость), в то время как пациенты с сахарным диабетом или с факторами риска сахарного диабета должны находиться под регулярным наблюдением. возможное ухудшение контроля глюкозы. Следует регулярно проверять массу тела.
Липиды
В клинических исследованиях кветиапина наблюдалось повышение уровня триглицеридов, ЛПНП и общего холестерина, а также снижение холестерина ЛПВП (см. Раздел 4.8). Изменения липидов необходимо контролировать клинически приемлемым образом.
Удлинение интервала QT
Кветиапин не был связан со стойким увеличением абсолютного интервала QT в клинических исследованиях и во время использования в соответствии с инструкциями в SmPC. В постмаркетинговом опыте удлинение интервала QT наблюдалось при применении кветиапина в терапевтических дозах (см. Раздел 4.8. ) и при передозировке (см. раздел 4.9). Как и в случае с другими нейролептиками, следует соблюдать осторожность при назначении кветиапина пациентам с сердечно-сосудистыми заболеваниями или семейным анамнезом удлинения интервала QT. пожилые люди, у пациентов с врожденным синдромом удлиненного интервала QT, застойной сердечной недостаточностью, гипертрофией сердца, гипокалиемией или гипомагниемией (см. раздел 4.5).
Кардиомиопатия и миокардит
О кардиомиопатии и миокардите сообщалось в ходе клинических испытаний и в ходе постмаркетингового опыта, однако причинно-следственная связь с кветиапином не установлена. Лечение кветиапином следует пересмотреть у пациентов с подозрением на кардиомиопатию или миокардит.
Приостановка
После резкого прекращения терапии кветиапином были описаны острые симптомы отмены, такие как бессонница, тошнота, головная боль, диарея, рвота, головокружение и раздражительность. Рекомендуется «постепенное прекращение приема» в течение как минимум 1-2 недель (см. Раздел 4.8).
Пожилые пациенты с психозом, связанным с деменцией
Кветиапин не лицензирован для лечения психозов, связанных с деменцией.
В рандомизированных плацебо-контролируемых клинических испытаниях, проведенных на популяции пациентов с деменцией, получавших некоторые атипичные антипсихотические препараты, наблюдалось примерно 3-кратное повышение риска цереброваскулярных событий. Механизм этого повышенного риска неизвестен. Нельзя исключить повышенный риск для других нейролептиков или других групп пациентов. Кветиапин следует с осторожностью назначать пациентам с факторами риска инсульта.
В метаанализе атипичных антипсихотических препаратов сообщалось о повышенном риске смерти по сравнению с плацебо у пожилых пациентов с психозом, связанным с деменцией. Однако в двух 10-недельных плацебо-контролируемых клинических испытаниях кветиапина в той же популяции пациентов (n = 710); средний возраст: 83 года; диапазон: 56-99 лет) частота смертности у пациентов, получавших кветиапин, составляла 5,5% по сравнению с 3,2% в группе плацебо. Пациенты в этих исследованиях умерли от различных причин, соответствующих ожидаемым для этой популяции. лечение кветиапином и смерть пожилых пациентов с деменцией.
Дисфагия
Сообщалось о дисфагии при приеме кветиапина (см. Раздел 4.8). Кветиапин следует применять с осторожностью у пациентов с риском аспирационной пневмонии.
Запор и кишечная непроходимость
Запор является фактором риска кишечной непроходимости. При приеме кветиапина сообщалось о запорах и кишечной непроходимости (см. Раздел 4.8. Нежелательные эффекты). Летальные случаи включаются у пациентов с повышенным риском кишечной непроходимости, в том числе у тех, кто лечится несколькими сопутствующими терапиями, которые снизить перистальтику кишечника и / или те, которые могут не сообщать о симптомах запора. Пациентам с кишечной непроходимостью / кишечной непроходимостью следует вести тщательный мониторинг и оказывать неотложную медицинскую помощь.
Венозная тромбоэмболия (ВТЭ)
Сообщалось о случаях венозной тромбоэмболии (ВТЭ) при применении антипсихотических препаратов. Поскольку пациенты, принимавшие нейролептики, часто приобретали факторы риска ВТЭ, все возможные факторы риска ВТЭ должны быть выявлены до и во время лечения ВТЭ и принимать соответствующие меры. предупредительные меры.
Панкреатит
О панкреатите сообщалось в ходе клинических испытаний и во время постмаркетингового опыта. В постмаркетинговых отчетах, хотя не все случаи были связаны с факторами риска, у многих пациентов были факторы, которые, как известно, связаны с панкреатитом, такие как повышение уровня триглицеридов (см. раздел 4.4), камни в желчном пузыре и употребление алкоголя.
Дополнительная информация
Имеются ограниченные данные об использовании кветиапина в сочетании с вальпроевой кислотой / вальпроатом натрия (дивалпроекс) или литием при острых умеренных и тяжелых маниакальных эпизодах; однако комбинированная терапия хорошо переносилась (см. Разделы 4.8 и 5.1). аддитивный эффект на 3 неделе.
04.5 Взаимодействие с другими лекарственными средствами и другие формы взаимодействия
Из-за первичного воздействия кветиапина на центральную нервную систему Кветиапин Милан следует применять с осторожностью в сочетании с другими центральноактивными препаратами и алкоголем.
Цитохром P450 (CYP) 3A4 - это фермент системы цитохрома P450, который в первую очередь отвечает за метаболизм кветиапина. В исследовании взаимодействия на здоровых добровольцах совместное введение кветиапина (25 мг) с кетоконазолом, ингибитором CYP3A4, вызывало AUC кветиапина увеличивается в 5-8 раз. По этой причине одновременный прием кветиапина и ингибиторов CYP3A4 противопоказан, а также не рекомендуется принимать грейпфрутовый сок во время терапии кветиапином.
В исследовании с участием пациентов, получавших несколько доз, для оценки фармакокинетики кветиапина, вводимого до и во время лечения карбамазепином (известным индуктором печеночных ферментов), совместное введение карбамазепина значительно увеличивало клиренс кветиапина. Это увеличение клиренса снижает системное воздействие кветиапина (измеряемое с помощью AUC) в среднем до 13% от воздействия при введении одного кветиапина, хотя у некоторых пациентов наблюдался более выраженный эффект. Взаимодействие может приводить к снижению концентраций в плазме, которые может влиять на эффективность терапии кветиапином. Совместное введение кветиапина и фенитоина (другого индуктора микросомальной ферментной системы) привело к заметному увеличению клиренса кветиапина примерно на 450%. У пациентов, получающих лечение индукторами печеночных ферментов, лечение кветиапином можно начинать только в том случае, если врач считает, что преимущества кветиапина перевешивают риск прекращения приема индукторов печеночных ферментов. Важно, чтобы любые изменения в этих индукторах происходили постепенно и при необходимости заменялись неиндукторами (например, вальпроатом натрия) (см. Раздел 4.4).
Фармакокинетика кветиапина существенно не изменилась при одновременном приеме антидепрессантов на основе имипрамина (известного ингибитора CYP 2D6) или флуоксетина (известного ингибитора CYP 3A4 и CYP 2D6).
Фармакокинетика кветиапина существенно не изменилась при одновременном приеме антипсихотических средств рисперидона или галоперидола. Одновременное применение кветиапина и тиоридазина привело к увеличению клиренса кветиапина примерно на 70%.
Фармакокинетика кветиапина не изменилась после одновременного приема с циметидином.
Фармакокинетика лития не изменилась при совместном применении с кветиапином.
В 6-недельном рандомизированном исследовании с пролонгированным высвобождением лития и кветиапина vs.плацебо и кветиапин с пролонгированным высвобождением, у взрослых пациентов с острой манией, более высокая частота экстрапирамидных эффектов (особенно тремора), сонливости и увеличения веса наблюдалась в группе, получавшей добавку лития, по сравнению с группой, получавшей добавление плацебо (см. раздел 5.1. ).
Фармакокинетика вальпроата натрия и кветиапина существенно не изменилась при одновременном применении этих двух продуктов. В ретроспективном исследовании детей / подростков, получавших вальпроат, кветиапин или оба препарата, была обнаружена высокая частота лейкопении и нейтропении в группе комбинированной терапии по сравнению с группами монотерапии.
Официальных исследований взаимодействия с наиболее часто используемыми сердечно-сосудистыми препаратами не проводилось.
Следует соблюдать осторожность при одновременном применении кветиапина с препаратами, которые, как известно, вызывают нарушение электролитного баланса или удлинение интервала QT.
Сообщалось о ложноположительных результатах иммуноферментных анализов на метадон и трициклические антидепрессанты у пациентов, принимавших кветиапин. Сомнительные результаты иммуноферментных анализов рекомендуется подтверждать соответствующими хроматографическими методами.
04.6 Беременность и кормление грудью
Беременность
Первая четверть
Скромное количество опубликованных данных о воздействии во время беременности (то есть от 300 до 1000 исходов беременности), включая индивидуальные отчеты и некоторые обсервационные исследования, не свидетельствует о повышенном риске пороков развития в результате лечения. Однако на основании всех имеющихся данных нельзя сделать однозначных выводов. Исследования на животных показали репродуктивную токсичность (см. Раздел 5.3). Поэтому кветиапин следует использовать во время беременности только в том случае, если преимущества оправдывают потенциальный риск.
Третья четверть
Новорожденные, получавшие нейролептики (включая кветиапин) в третьем триместре беременности, подвержены риску побочных реакций, включая экстрапирамидные и / или абстинентные симптомы, которые могут различаться по степени тяжести и продолжительности после рождения. Поступали сообщения о возбуждении, гипертонии, гипотонии, треморе, сонливости, затрудненном дыхании или нарушениях кормления. Поэтому следует тщательно наблюдать за младенцами.
Время кормления
Основываясь на очень ограниченных данных из опубликованных отчетов об экскреции кветиапина с грудным молоком, выведение кветиапина в терапевтических дозах кажется непостоянным. Из-за отсутствия достоверных данных необходимо принять решение о прекращении грудного вскармливания или о прекращении терапии кветиапином с учетом пользы грудного вскармливания для ребенка и пользы терапии для матери.
Плодородие
Эффекты кветиапина на фертильность человека не отслеживались. Эффекты, связанные с повышенным уровнем пролактина, наблюдались у крыс, хотя они не имеют прямого отношения к человеку (см. Раздел 5.3 «Доклинические данные»).
04.7 Влияние на способность управлять автомобилем и работать с механизмами
Из-за своего первичного воздействия на центральную нервную систему кветиапин может мешать деятельности, требующей умственной активности. Поэтому пациентам следует рекомендовать не водить машину и не работать с механизмами, пока не станет известна их чувствительность к препарату.
04.8 Побочные эффекты
Наиболее частыми побочными реакциями (НЛР) кветиапина (≥10%) являются сонливость, головокружение, головная боль, сухость во рту, абстинентный синдром, повышение уровня триглицеридов в сыворотке крови, повышение общего холестерина (в основном холестерина ЛПНП), снижение холестерина ЛПВП, прибавка в весе. , снижение гемоглобина и экстрапирамидные симптомы.
Частота нежелательных реакций, связанных с терапией кветиапином, показана в таблице ниже в соответствии с форматом, рекомендованным Советом международных организаций медицинских наук (рабочая группа CIOMS III; 1995).
Таблица 1: Нежелательные реакции, связанные с терапией кветиапином
Частота нежелательных явлений классифицируется согласно следующему условию:
Очень часто (≥1 / 10), часто (≥1 / 100 и
1. См. Раздел 4.4.
2. Сонливость может возникать, как правило, в течение первых двух недель лечения, которая обычно проходит при продолжении приема кветиапина.
3. У некоторых пациентов, получавших кветиапин, наблюдалось бессимптомное (переход от нормального к> 3-кратному верхнему пределу нормы в любое время) повышение уровня сывороточных трансаминаз (АЛТ, АСТ) или гамма-GT. Это повышение обычно было обратимым при продолжении терапии кветиапином.
4. Как и другие нейролептики с альфа-адреноблокирующей активностью, кветиапин обычно может вызывать ортостатическую гипотензию, связанную с головокружением, тахикардией и, у некоторых пациентов, обмороками, особенно в период титрования начальной дозы (см. Раздел 4.4).
5. Частота этих побочных реакций рассчитывалась только на основании постмаркетинговых данных, основанных на препаратах кветиапина с немедленным высвобождением.
6. Уровень глюкозы в крови натощак ≥126 мг / дл (≥ 7,0 ммоль / л) или уровень глюкозы в крови не натощак ≥ 200 мг / дл (≥ 11,1 ммоль / л) хотя бы в одном "случае".
7. Увеличение частоты дисфагии при приеме кветиапина по сравнению с плацебо наблюдалось только в клинических испытаниях при биполярной депрессии.
8. На основе увеличения веса> 7% от исходного веса. Это происходит в основном в течение первых нескольких недель лечения у взрослых.
9. Следующие симптомы отмены чаще наблюдались в клинических испытаниях острой плацебо-контролируемой монотерапии, оценивающих симптомы отмены: бессонница, тошнота, головная боль, диарея, рвота, головокружение и раздражительность. Частота этих реакций значительно снизилась через 1 неделю после прекращения приема.
10. Триглицериды ≥ 200 мг / дл (≥ 2,258 ммоль / л) (пациенты в возрасте ≥ 18 лет) или ≥ 150 мг / дл (≥ 1,694 ммоль / л) (пациенты в возрасте
11. Холестерин ≥ 240 мг / дл (≥ 6,2064 ммоль / л) (пациенты в возрасте ≥ 18 лет) или ≥ 200 мг / дл (≥ 5,172 ммоль / л) (пациенты в возрасте
12. См. Текст ниже.
13. Тромбоциты ≤ 100 x 109 / л хотя бы один раз.
14.На основании отчетов о клинических испытаниях нежелательных явлений, связанных с повышением уровня креатинфосфокиназы, не связанных со злокачественным нейролептическим синдромом.
15. Уровни пролактина (пациенты> 18 лет):> 20 мкг / л (> 869,56 пмоль / л) у мужчин,> 30 мг / л (> 1304,34 пмоль / л) у женщин в любое время.
16. Может привести к падению
17. Холестерин ЛПВП.
18. Частота пациентов с изменением QTc от
19. Изменение с> 132 ммоль / л на ≤ 132 ммоль / л хотя бы один раз.
20. Сообщалось о случаях суицидальных мыслей и суицидального поведения во время терапии кветиапином или в начале после прекращения лечения (см. Разделы 4.4 и 5.1).
21. См. Параграф 5.1.
22. Снижение гемоглобина ≤ 13 г / дл (8,07 ммоль / л) у мужчин, ≤ 12 г / дл (7,45 ммоль / л) у женщин по крайней мере в одном «случае» наблюдалось у 11% пациентов, принимавших кветиапин, во всех исследованиях, включая расширенные открытые исследования. Для этих пациентов среднее максимальное снижение гемоглобина в любое время составило -1,50 г / дл.
23. Эти сообщения часто возникали при тахикардии, головокружении, ортостатической гипотензии и / или предшествующем сопутствующем заболевании сердца / дыхательных путей.
24. Основано на изменении от нормального исходного уровня до потенциально клинически важного значения в любое время после исходного уровня во всех исследованиях. Изменения общего T4, FT4, общего T3 и свободного T3 определяются как 5 mUI / L в любое время.
25. На основании частоты учащения рвоты у пожилых пациентов (≥ 65 лет).
26. На основании изменения нейтрофилов с> = 1,5 x 109 / л на исходном уровне a
27. Основано на изменении от нормального исходного уровня до потенциально клинически важного значения после исходного уровня во всех исследованиях. Изменения эозинофилов определяются как> 1 x 109 клеток / л в любое время.
28. Основано на изменении от нормального исходного уровня до потенциально клинически важного значения в любое время после исходного уровня во всех исследованиях. Изменения лейкоцитов определяются как ≤ 3x109 клеток / л в любой момент времени.
29. На основании отчетов о нежелательных явлениях метаболического синдрома во всех клинических испытаниях кветиапина.
30. У некоторых пациентов в клинических исследованиях наблюдалось ухудшение более чем одного из метаболических факторов веса, уровня глюкозы в крови и липидов (см. Раздел 4.4).
31. См. Раздел 4.6.
32. Это может произойти в начале лечения или незадолго до этого и быть связано с гипотензией и / или обмороком. Частота основана на отчетах о побочных реакциях брадикардии и связанных событий во всех клинических исследованиях с кветиапином.
Сообщалось о случаях удлинения интервала QT, желудочковой аритмии, внезапной необъяснимой смерти, остановки сердца и torsades de pointes после применения нейролептиков, которые считаются эффектами этого класса препаратов.
Педиатрическая популяция
Те же самые нежелательные реакции, описанные выше для взрослых, следует учитывать для детей и подростков. В таблице ниже приведены побочные эффекты, которые чаще встречаются у детей и подростков (в возрасте 10-17 лет), чем у взрослого населения, или нежелательные реакции, которые не были выявлены у взрослого населения.
Таблица 2: Нежелательные реакции у детей и подростков, связанные с терапией кветиапином, встречаются чаще, чем у взрослых, или не выявляются у взрослого населения.
Частота нежелательных явлений классифицируется согласно следующему условию: очень часто (≥1 / 10), часто (≥1 / 100,
1. Уровни пролактина (пациенты в возрасте 20 мкг / л (> 869,56 пмоль / л) у мужчин;> 26 мкг / л (> 1130,428 пмоль / л) у женщин в любое время. Менее чем у 1% пациентов наблюдалось повышение уровня пролактина. уровни> 100 мкг / л.
2. На основании превышения клинически значимых пороговых значений (адаптировано из критериев Национального института здоровья) или увеличения систолического артериального давления на> 20 мм рт. Ст. Или диастолического артериального давления> 10 мм рт. -контролируется у детей и подростков.
3. Примечание: частота аналогична частоте, наблюдаемой у взрослых пациентов, но раздражительность может быть связана с другими клиническими проявлениями у детей и подростков, чем у взрослых.
4. См. Параграф 5.1.
Сообщение о предполагаемых побочных реакциях
Сообщение о предполагаемых побочных реакциях, возникающих после получения разрешения на лекарственный препарат, важно, поскольку оно позволяет осуществлять непрерывный мониторинг баланса пользы и риска лекарственного средства. Медицинских работников просят сообщать о любых предполагаемых побочных реакциях через национальную систему отчетности. "Адрес: http : //www.agenziafarmaco.gov.it/it/responsabili.
04.9 Передозировка
Симптомы
В общем, указанные признаки и симптомы связаны с усилением известных фармакологических эффектов активного ингредиента, например, таких как. сонливость и седативный эффект, тахикардия и гипотония. Передозировка может привести к удлинению интервала QT, судорогам, эпилептическому статусу, рабдомиолизу, угнетению дыхания, задержке мочи, спутанности сознания, делирию и / или возбуждению, коме и смерти. Пациенты с ранее существовавшим тяжелым сердечно-сосудистым заболеванием могут быть более подвержены риску развития эффектов передозировки. (см. раздел 4.4 «Сердечно-сосудистые заболевания»).
Управление передозировкой
Специфического антидота кветиапина не существует. В случаях с тяжелыми проявлениями следует учитывать возможность участия нескольких лекарственных препаратов и рекомендовать процедуры интенсивной терапии, включая создание и поддержание проходимости дыхательных путей для поддержки адекватной оксигенации и вентиляции, а также мониторинг и поддержку сердечно-сосудистой системы.
Согласно опубликованной литературе, пациентов с делирием и возбуждением, а также с явным антихолинергическим синдромом можно лечить физостигмином в дозе 1-2 мг (при постоянном мониторинге ЭКГ). Это не рекомендуется в качестве стандартного лечения из-за потенциальных побочных эффектов. Физостигмин на сердечную проводимость. Физостигмин можно использовать, если нет изменений на ЭКГ. Не используйте физостигмин при нарушениях ритма, любой степени сердечной блокады или удлинении интервала QRS.
Хотя предотвращение абсорбции в случае передозировки не оценивалось, в случае тяжелой интоксикации можно рассмотреть возможность промывания желудка, которое должно быть выполнено, если возможно, в течение одного часа после приема внутрь. Следует также рассмотреть возможность проведения промывания желудка. Активированный уголь.
В случае передозировки кветиапином рефрактерную гипотензию следует лечить с помощью соответствующих мер, таких как внутривенное введение жидкости и / или симпатические миметики. Следует избегать применения адреналина и дофамина, поскольку бета-стимуляция может ухудшить гипотензию в начале «кветиапин-индуцированной альфа-блокады».
До выздоровления пациента необходимо обеспечить точное медицинское наблюдение и соответствующее наблюдение.
05.0 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
05.1 Фармакодинамические свойства
Фармакотерапевтическая группа: нейролептики; Диазепин, оксазепин и тиазепин.
Код УВД: N05A H04
Механизм действия
Кветиапин - атипичный антипсихотический препарат. Кветиапин и активный метаболит в плазме крови человека норкетиапин взаимодействуют с широким спектром рецепторов нейромедиаторов. Кветиапин и норветиапин обладают «сродством к серотонинергическим (5HT2) и допаминовым рецепторам D1- и D2 мозга. Сочетание антагонизма рецепторов с большей селективностью к рецепторам 5HT2 по сравнению с рецепторами D2, как полагают, вносит вклад в клинические и антипсихотические свойства. кветиапин вызывает экстрапирамидные побочные эффекты (EPS) по сравнению с типичными нейролептиками.
Кветиапин и норкетиапин не обладают «заметным сродством к бензодиазепиновым рецепторам, но» высоким сродством к гистаминергическим и альфа-1-адренергическим рецепторам, с меньшим сродством к альфа-2-адренергическим средствам и некоторым мускариновым рецепторам.
Ингибирование транспортера норадреналина (NET) и частичное агонистическое действие на сайтах 5HT1A норкетиапином может способствовать терапевтической эффективности кветиапина милана в качестве антидепрессанта.
Фармакодинамические эффекты
Кветиапин был активен в тестах оценки антипсихотической активности, таких как тест условного избегания.Он также способен блокировать действие дофаминергических агонистов, что оценивается как с поведенческой, так и с электрофизиологической точки зрения, и увеличивает концентрацию метаболитов дофамина, которые считаются нейрохимическими индикаторами активности блокирования рецептора D2.
В доклинических тестах для прогнозирования экстрапирамидных симптомов (ЭПС) кветиапин отличался от типичных нейролептиков и имел атипичный профиль. Хроническое введение кветиапина не вызывает сверхчувствительности дофаминергических рецепторов D2. Кветиапин вызывает только слабую каталепсию в дозах, эффективных для блокирования дофаминовых рецепторов D2. После хронического введения кветиапин демонстрирует селективность в отношении лимбической системы, блокируя деполяризацию мезолимбической области без воздействия на нигростриатальную область, где присутствуют дофаминергические нейроны. Кветиапин проявляет минимальную склонность к дистоническим проявлениям у сенсибилизированных галоперидолом обезьян Cebus или обезьян, не употребляющих лекарственные препараты, после острого введения или введения через роговицу (см. Раздел 4.8).
Клиническая эффективность
Шизофрения
Эффективность кветиапина пролонгированного действия при лечении шизофрении была продемонстрирована в 6-недельном плацебо-контролируемом клиническом исследовании, проведенном у пациентов, соответствующих критериям DSM-IV для диагностики шизофрении, а также в клиническом исследовании. Кветиапин немедленного высвобождения вместо кветиапина пролонгированного действия у клинически стабильных амбулаторных пациентов с шизофренией.
Первичной переменной результата в плацебо-контролируемом исследовании был переход от исходного контроля к окончательной оценке общего балла PANSS. Введение кветиапина с пролонгированным высвобождением 400 мг / день, 600 мг / день и 800 мг / день было связано со статистически значимым улучшением психотических симптомов по сравнению с плацебо. Величина эффекта от доз 600 мг и 800 мг была больше, чем от дозы 400 мг.
В 6-недельном активном клиническом исследовании, контролируемом компаратором, в котором сравнивали переход с одного препарата на другой, первичной переменной результата была доля пациентов, у которых не было эффективности, т.е. которые прекратили исследование из-за отсутствия терапевтической эффективности или чьи Общий балл PANSS был увеличен на 20% или более при посещениях после рандомизации. У пациентов, стабилизированных приемом кветиапина немедленного высвобождения в дозах от 400 мг до 800 мг, эффективность сохранялась неизменной, когда пациентов переводили на эквивалентную суточную дозу пролонгированного высвобождения. кветиапин в разовой дозе.
В долгосрочном исследовании у стабилизированных пациентов с шизофренией, получавших кветиапин с пролонгированным высвобождением в течение 16 недель, кветиапин с пролонгированным высвобождением был более эффективен, чем плацебо в предотвращении рецидива. Расчетный риск рецидива после 6 месяцев лечения составлял 14,3% для группы таблеток с пролонгированным высвобождением кветиапина по сравнению с 68,2% для пациентов, получавших плацебо. Средняя доза составила 669 мг. Дополнительных наблюдений за безопасностью лечения кветиапином с пролонгированным высвобождением в течение периода до 9 месяцев (в среднем 7 месяцев) не проводилось. В частности, не наблюдалось увеличения количества сообщений о нежелательных явлениях, связанных с ЭПС, и о наборе веса при длительном лечении кветиапином с пролонгированным высвобождением.
Биполярное расстройство
При лечении умеренных и тяжелых маниакальных эпизодов в двух клинических испытаниях монотерапии кветиапин продемонстрировал «превосходящую эффективность по сравнению с плацебо в уменьшении маниакальных симптомов на 3-й и 12-й неделях». Далее была продемонстрирована эффективность кветиапина с пролонгированным высвобождением, показав различия, значимые по сравнению с плацебо. в дополнительном 3-недельном исследовании. Кветиапин с пролонгированным высвобождением вводили в диапазоне доз от 400 до 800 мг / день, а средняя доза составляла приблизительно 600 мг / день. Данные относительно применения кветиапина в сочетании с вальпроевой кислотой / вальпроатом натрия (дивалпроекс) или литием при острых умеренных и тяжелых маниакальных эпизодах на 3-й и 6-й неделях ограничены; однако комбинированная терапия хорошо переносилась. Данные показали аддитивный эффект на 3-й неделе. Второе исследование не продемонстрировало аддитивного эффекта на 6-й неделе.
В клиническом исследовании у пациентов с депрессивными эпизодами, связанными с биполярным расстройством I или II типа, прием кветиапина пролонгированного действия в дозе 300 мг / день показал большую эффективность, чем плацебо, в снижении общего балла по шкале MADRS.
В 4 дополнительных клинических испытаниях кветиапина продолжительностью 8 недель у пациентов с умеренными и тяжелыми депрессивными эпизодами, связанными с биполярным расстройством I или II, кветиапин с немедленным высвобождением 300 мг и 600 мг значительно превосходил плацебо по результатам, связанным с оцененными параметрами эффективности: означает улучшение по шкале MADRS и клинический ответ пациента с улучшением не менее чем на 50% общей оценки по шкале MADRS по сравнению с исходным уровнем. Не было разницы в величине эффекта между пациентами, получавшими дозу кветиапина с немедленным высвобождением 300 мг, и пациентами, получавшими дозу 600 мг.
В фазе продолжения двух из этих исследований было показано, что длительное лечение пациентов, ответивших на лечение кветиапином 300 или 600 мг с немедленным высвобождением, было эффективным по сравнению с плацебо с точки зрения предотвращения депрессивных симптомов, но не маниакальных симптомов.
В двух исследованиях по профилактике рецидивов, в которых оценивался эффект кветиапина в сочетании со стабилизаторами настроения у пациентов с маниакальными, депрессивными или смешанными эпизодами, комбинация с кветиапином превосходила только стабилизаторы настроения в «увеличении времени до рецидива любого эпизода настроения (маниакального, смешанного). или депрессивный). Кветиапин вводили дважды в день в дозе 400-800 мг в день в сочетании с литием или вальпроатом.
В долгосрочном исследовании (до 2 лет лечения) по оценке предотвращения рецидивов у пациентов с маниакальными, депрессивными или смешанными эпизодами было показано, что кветиапин превосходит плацебо в увеличении времени до рецидива любого эпизода. Измененное настроение ( маниакальный, смешанный или депрессивный) у пациентов с биполярным расстройством I. Число пациентов, у которых возникло событие, связанное с настроением, составило 91 (22,5%) в группе кветиапина, соответственно, 208 (51,5%) в группе плацебо и 95 (26,1%) ) в литиевой группе. У пациентов, которые отреагировали на лечение кветиапином, при сравнении продолжения лечения кветиапином с переходом на литий результаты показали, что переход на литий, по-видимому, не связан с увеличением времени до рецидива «связанного события» - юмора.
Серьезные депрессивные эпизоды, связанные с СДД
В двух краткосрочных (6-недельных) исследованиях участвовали пациенты, которые показали неадекватный ответ хотя бы на один антидепрессант. Кветиапин 150 мг и 300 мг / день, вводимый в качестве дополнительной терапии к продолжающейся терапии антидепрессантами (амитриптилин, бупропион, циталопрам, дулоксетин, эсциталопрам, флуоксетин, пароксетин, сертралин или венлафаксин), продемонстрировал «более высокую эффективность, чем терапия только антидепрессантами в уменьшении депрессивных симптомов. , о чем свидетельствует улучшение общего балла MADRS (среднее изменение LS по сравнению с плацебо на 2-3,3 балла).
Долгосрочная эффективность и безопасность у пациентов с СДД не оценивались в качестве дополнительной терапии, однако эти параметры оценивались у взрослых пациентов, получающих монотерапию (см. Ниже).
Следующие исследования были проведены с одним кветиапином с пролонгированным высвобождением, однако кветиапин с пролонгированным высвобождением показан только для дополнительной терапии:
В трех из четырех краткосрочных (до 8 недель) исследований монотерапии у пациентов с большим депрессивным расстройством кветиапин с пролонгированным высвобождением 50 мг, 150 мг и 300 мг / день продемонстрировал «более высокую эффективность, чем плацебо, в уменьшении депрессивных симптомов, поскольку о чем свидетельствует улучшение общего балла по шкале оценки депрессии Монтгомери-Асберга (MADRS) (среднее изменение LS по сравнению с плацебо на 2–4 балла).
В исследовании профилактики рецидивов монотерапии пациенты с депрессивными эпизодами, стабилизировавшимися на открытом лечении кветиапином пролонгированного действия в течение не менее 12 недель, были рандомизированы для получения кветиапина пролонгированного действия один раз в день или плацебо в течение до 52 недель.Средняя доза кветиапина пролонгированного действия на этапе рандомизации составляла 177 мг / день. Частота рецидивов составила 14,2% для пациентов, получавших кветиапин с пролонгированным высвобождением, и 34,4% для пациентов, получавших плацебо.
В краткосрочном (9-недельном) исследовании с участием пожилых пациентов без деменции (в возрасте от 66 до 89 лет) с большим депрессивным расстройством кветиапин пролонгированного действия, вводимый в гибких дозах от 50 до 300 мг / день, продемонстрировал более высокую эффективность, чем плацебо. в уменьшении депрессивных симптомов, о чем свидетельствует улучшение общего балла MADRS (среднее изменение LS по сравнению с плацебо -7,54).
В этом исследовании пациенты, рандомизированные для получения кветиапина с пролонгированным высвобождением, получали лечение по 50 мг / день в дни 1-3, и затем доза могла быть увеличена до 100 мг / день в день 4, до 150 мг / день в день 8 и до 300 мг / сут, в зависимости от клинического ответа и переносимости. Средняя доза кветиапина пролонгированного действия составляла 160 мг / день. За исключением «случаев возникновения экстрапирамидных симптомов (см. Раздел 4.8 и« Клиническая безопасность »ниже), переносимость кветиапина с пролонгированным высвобождением один раз в день у пожилых пациентов была сопоставима с таковой у взрослых (в возрасте от 18 до 65 лет). рандомизированных пациентов старше 75 лет составляло 19%.
Клиническая безопасность
В краткосрочных плацебо-контролируемых клинических испытаниях шизофрении и биполярной мании совокупная частота экстрапирамидных симптомов была аналогична плацебо (шизофрения: 7,8% для кветиапина и 8,0% для плацебо; биполярная мания: 11, 2% для кветиапина и 11,4%). для плацебо) Более высокая частота экстрапирамидных симптомов наблюдалась у пациентов, получавших кветиапин, по сравнению с пациентами, получавшими плацебо, в краткосрочных плацебо-контролируемых клинических испытаниях при БДР и биполярной депрессии. Плацебо-контролируемые краткосрочные клинические испытания при биполярной депрессии, объединенные Частота экстрапирамидных симптомов составила 8,9% для кветиапина по сравнению с 3,8% для плацебо. В краткосрочных плацебо-контролируемых клинических испытаниях монотерапии при большом депрессивном расстройстве объединенная частота экстрапирамидных симптомов составила 5,4% для кветиапина с пролонгированным высвобождением и 3,2% для плацебо. . В краткосрочном плацебо-контролируемом клиническом исследовании монотерапии у пожилых пациентов с большим депрессивным расстройством объединенная частота экстрапирамидных симптомов составила 9,0% для кветиапина и 2,3% для плацебо. Как при биполярной депрессии, так и при БДР частота единичных нежелательных явлений (например, акатизия, экстрапирамидное расстройство, тремор, дискинезия, дистония, возбужденное состояние, непроизвольные сокращения мышц, психомоторная гиперактивность и ригидность мышц) не превышали 4% во всех группах лечения.
В краткосрочных (от 3 до 8 недель) и фиксированных дозах (от 50 до 800 мг / день) плацебо-контролируемых исследованиях средняя прибавка в весе у пациентов, получавших кветиапин, составляла от 0,8 кг в день. Суточная доза 50 мг и 1,4 кг для суточной дозы 600 мг (с меньшим увеличением для суточной дозы 800 мг) по сравнению с 0,2 кг у пациентов, получавших плацебо. кветиапин, который сообщил об увеличении массы тела на ≥7%, варьировался от 5,3% для Суточная доза 50 мг составляет 15,5% для суточной дозы 400 мг (с меньшим увеличением для суточных доз 600 и 800 мг) мг) по сравнению с 3,7% пациентов, получавших плацебо.
Шестинедельное рандомизированное исследование лития пролонгированного действия и кветиапина vs. плацебо и кветиапин с пролонгированным высвобождением у взрослых пациентов с острой манией показали, что комбинация кветиапина с пролонгированным высвобождением и литием приводит к более высокой частоте нежелательных явлений (63% против 48% при комбинации кветиапина с пролонгированным высвобождением. более высокая частота экстрапирамидных эффектов, о которых сообщалось у 16,8% пациентов в группе дополнительного приема лития и 6,6% в группе дополнительного приема плацебо, большинство из которых состояло из тремора, сообщалось у 15,6% пациентов в группе дополнительного приема лития. группа и 4,9% в группе дополнительного приема плацебо. Частота сонливости была выше в группе кветиапина пролонгированного действия и дополнительной терапии. литий (12,7%) по сравнению с группой добавления кветиапина пролонгированного действия и плацебо (5,5%). %). Кроме того, больший процент пациентов, получавших добавление лития (8,0%), имел прибавку в весе (≥7%) в конце лечения по сравнению с пациентами в группе добавления плацебо (4,7%).
Долгосрочные исследования профилактики рецидивов включали открытый период (от 4 до 36 недель), в течение которого пациенты получали кветиапин, с последующим рандомизированным периодом отмены, в течение которого пациенты были рандомизированы для получения кветиапина или плацебо. Для пациентов, рандомизированных для приема кветиапина, средняя прибавка веса в течение периода открытой метки составила 2,56 кг, а на 48 неделе периода рандомизации средняя прибавка веса составила 3,22 кг по сравнению с открытой базальной дозой. Для пациентов, рандомизированных в группу плацебо, средняя прибавка веса в течение периода открытой метки составила 2,39 кг, а на 48 неделе периода рандомизации средняя прибавка массы тела составила 0,89 кг по сравнению с открытой базальной дозой.
В плацебо-контролируемых исследованиях с участием пожилых пациентов с психозом, связанным с деменцией, частота цереброваскулярных нежелательных явлений на 100 пациенто-лет не была выше у пациентов, получавших кветиапин, чем у пациентов, получавших плацебо.
Во всех плацебо-контролируемых краткосрочных клинических испытаниях монотерапии, проведенных у пациентов с исходным числом нейтрофилов ≥1,5 X 109 / л, частота, по крайней мере, одного числа нейтрофилов 0,5 -
Лечение кветиапином было связано с небольшим дозозависимым снижением уровня гормонов щитовидной железы. Частота сдвигов уровня ТТГ составила 3,2% для кветиапина по сравнению с 2,7% для плацебо. Частота взаимно потенциально клинически значимых сдвигов уровней Т3 или Т4 и ТТГ в этих клинических испытаниях была редкой, а изменения уровней гормонов щитовидной железы обычно не связаны. при клинически симптоматическом гипотиреозе. Снижение общего и свободного Т4 было максимальным в первые шесть недель лечения кветиапином без дальнейшего снижения при длительном лечении. Примерно в 2/3 всех случаев прекращение терапии кветиапином было связано с «обращением» эффектов на общий и свободный Т4, независимо от продолжительности лечения.
Катаракта / помутнение хрусталика
В клиническом исследовании, проведенном для оценки катарактогенной силы кветиапина (200-800 мг / день) по сравнению с рисперидоном (2-8 мг) у пациентов с шизофренией или шизоаффективным расстройством, процент пациентов с продолжительностью воздействия не менее 21 месяца, которые показали, что увеличение степени помутнения хрусталика было не выше в группе кветиапина (4%), чем в группе рисперидона (10%).
Педиатрическая популяция
Клиническая эффективность
Эффективность и безопасность кветиапина оценивались в 3-недельном плацебо-контролируемом клиническом исследовании лечения мании (n = 284 пациента из США в возрасте 10-17 лет). 45% популяции пациентов имели дополнительный диагноз. СДВГ. Кроме того, для лечения шизофрении было проведено 6-недельное плацебо-контролируемое исследование (n = 222 пациента в возрасте 13-17 лет). В оба исследования были исключены пациенты с известной невосприимчивостью к лечению кветиапином. Лечение кветиапином включало начальная доза 50 мг / день, увеличивалась до 100 мг / день на 2-й день; после этого доза постепенно корректировалась для достижения целевой дозировки (мания 400-600 мг / день; шизофрения 400-800 мг / день) с шагом 100 мг / день, разделенные на два или три ежедневных приема.
В исследовании мании разница в среднем изменении LS от исходного уровня общего балла YMRS (активный минус плацебо) составила -5,21 для кветиапина 400 мг / день и -6,56 для кветиапина 600 мг / день. Частота ответивших (улучшение YMRS ≥ 50%) составляла 64% для кветиапина 400 мг / день, 58% для 600 мг / день и 37% в группе плацебо.
В исследовании шизофрении разница в среднем изменении LS от исходного уровня в общем балле PANSS (активный минус плацебо) составляла -8,16 для кветиапина 400 мг / день и -9,29 для кветиапина 800 мг / день.Кветиапин не превосходил плацебо как в режиме низких доз (400 мг / день), так и в режиме высоких доз (800 мг / день) с точки зрения процента пациентов, ответивших на лечение, определяемого как снижение ≥ 30% начальный общий балл по шкале PANSS. Более высокие дозы вызывали численно меньшую частоту ответа как в исследованиях мании, так и в исследованиях шизофрении.
В третьем краткосрочном плацебо-контролируемом исследовании монотерапии кветиапином пролонгированного действия у детей и подростков (10-17 лет) с биполярной депрессией эффективность не была продемонстрирована.
Нет данных о поддержании эффекта или предотвращении рецидивов в этой возрастной группе.
Клиническая безопасность
В краткосрочных педиатрических клинических испытаниях кветиапина, описанных выше, частота экстрапирамидных эффектов в активной группе по сравнению с плацебо составила 12,9% против 5,3% в исследовании шизофрении, 3,6% против 1,1% в исследовании биполярной мании и 1,1% в исследовании шизофрении. % против 0% в исследовании биполярной депрессии. Частота увеличения массы тела ≥7% от исходной массы тела в активной группе по сравнению с плацебо составила 17% против 2,5% в исследованиях шизофрении и биполярной мании и 12,5%. По сравнению с 6% в исследовании биполярной депрессии. Частота суицидальных событий в активной группе vs. плацебо было 1,4% по сравнению с 1,3% в исследовании шизофрении, 1,0% vs. 0% в исследовании биполярной мании и 1,1% vs. 0% в исследовании биполярного депрессона.
Во время продления фазы наблюдения после лечения в исследовании биполярной депрессии у двух пациентов было два дополнительных суицидальных события; один из этих пациентов принимал кветиапин во время события.
Долгосрочная безопасность
Расширение открытых клинических исследований острых заболеваний на период в 26 недель (n = 380 пациентов) с гибкими дозами кветиапина в диапазоне от 400 до 800 мг / день предоставило дополнительные данные о безопасности. Сообщалось о повышении артериального давления у детей и подростков, и с большей частотой у детей и подростков, чем у взрослых, наблюдались повышение аппетита, экстрапирамидные симптомы и повышение сывороточного пролактина (см. Разделы 4.4 и 4.8).
Что касается прибавки в весе, с поправкой на долгосрочное нормальное развитие, увеличение индекса массы тела не менее чем на 0,5 стандартного отклонения от исходного уровня использовалось в качестве меры клинически значимого изменения; Этому критерию соответствовали 18,3% пациентов, получавших кветиапин в течение 26 недель.
05.2 «Фармакокинетические свойства.
Абсорбция
Кветиапин хорошо всасывается после приема внутрь. Кветиапин с пролонгированным высвобождением достигает пиковых концентраций кветиапина и норкетиапина в плазме крови примерно через 6 часов после приема (Tmax). Пиковые постоянные молярные концентрации активного метаболита норкетиапина составляют 35% от концентраций, наблюдаемых для кветиапина.
Фармакокинетика кветиапина и норкетиапина линейна и пропорциональна дозе для доз до 800 мг, вводимых один раз в сутки. Когда кветиапин пролонгированного действия, вводимый один раз в день, сравнивается с такой же общей суточной дозой кветиапина фумарата немедленного высвобождения (кветиапин немедленного высвобождения), вводимой два раза в день, площадь под кривой зависимости концентрации в плазме от времени (AUC) эквивалентна, но максимальная Концентрация в плазме (Cmax) ниже на 13% в стабильном состоянии. Когда кветиапин с пролонгированным высвобождением по сравнению с кветиапином с немедленным высвобождением, AUC метаболита норкветиапина ниже на 18%.
В исследовании, посвященном влиянию пищи на биодоступность кветиапина, прием пищи с высоким содержанием жиров приводил к статистически значимому увеличению Cmax и AUC кветиапина с пролонгированным высвобождением на 50% и 20% соответственно. Нельзя исключить, что влияние еды с высоким содержанием жиров на рецептуру может быть больше. Для сравнения, легкая еда не оказала значительного влияния на Cmax и AUC кветиапина. Рекомендуется принимать кветиапин с контролируемым высвобождением. день, без еды.
Распределение
Кветиапин примерно на 83% связывается с белками плазмы.
Биотрансформация
После введения радиоактивно меченного кветиапина продукт интенсивно метаболизируется в печени и в неизмененном виде обнаруживается в моче и фекалиях в количестве менее 5% от исходного соединения.
Проведенные исследования in vitro продемонстрировали, что CYP3A4 является основным ферментом, ответственным за опосредованный цитохромом P450 метаболизм кветиапина. Норкветиапин в первую очередь продуцируется и выводится из организма CYP3A4.
Кветиапин и некоторые его метаболиты (включая норкетиапин) являются слабыми ингибиторами. in vitro активности 1A2, 2C9, 2C19, 2D6 и 3A4 человеческого цитохрома P450. В пробирке Ингибирование CYP наблюдалось только при концентрациях примерно в 5-50 раз выше, чем у людей при дозах от 300 до 800 мг / день. На основании этих результатов in vitro Совместное введение кветиапина и других препаратов вряд ли вызовет «клинически значимое ингибирование метаболизма других лекарственных средств, опосредованного цитохромом P450. Исследования на животных показали, что кветиапин может индуцировать ферменты цитохрома P450. Однако в конкретном исследовании взаимодействия цитохрома P450. При психотических заболеваниях». У пациентов после введения кветиапина не наблюдалось повышения активности цитохрома P450.
Устранение
Период полувыведения кветиапина и норкетиапина составляет приблизительно 7 и 12 часов соответственно.
Приблизительно 73% радиоактивно меченного лекарства выводится с мочой и 21% - с фекалиями, при этом менее 5% общей радиоактивности представляет собой неизмененный материал, связанный с наркотиками. Доля средней молярной дозы свободного кветиапина и активного метаболита норкетиапина, присутствующих в плазме крови человека, в определенной степени выводится с мочой.
Особые группы населения
Тип
Фармакокинетический профиль кветиапина не отличается у мужчин и женщин.
Пожилые граждане
У пожилых людей средний клиренс кветиапина примерно на 30-50% ниже, чем у взрослых в возрасте от 18 до 65 лет.
Повреждение почек
Средний клиренс кветиапина из плазмы снижается примерно на 25% у субъектов с тяжелой почечной недостаточностью (клиренс креатинина менее 30 мл / мин / 1,73 м2), но индивидуальные значения клиренса находятся в пределах нормы для здоровых субъектов.
Печеночная недостаточность
Средний клиренс кветиапина из плазмы снижается примерно на 25% у пациентов с печеночной недостаточностью (стабильный алкогольный цирроз). Поскольку кветиапин интенсивно метаболизируется в печени, пациенты с печеночной недостаточностью могут иметь более высокие уровни препарата в плазме и требовать корректировки дозы (см. Раздел 4.2).
Педиатрическая популяция
Фармакокинетические данные были собраны у 9 детей в возрасте от 10 до 12 лет и 12 подростков, получавших кветиапин в постоянной дозе 400 мг два раза в день. В стабильном состоянии нормализованные по дозе уровни исходного соединения кветиапина в плазме крови у детей и подростков (в возрасте от 10 до 17 лет) в целом были аналогичны таковым у взрослых, хотя Cmax у детей находился в верхней части диапазона значений. Наблюдались у взрослых. AUC и Cmax для активного метаболита норкетиапина были на 62% и 49% выше у детей (в возрасте от 10 до 12 лет) и на 28% и 14% соответственно у подростков (в возрасте 13-17 лет), чем Взрослые.
Информация об использовании кветиапина пролонгированного действия у детей и подростков отсутствует.
05.3 Доклинические данные по безопасности
В серии исследований генотоксичности in vitro А также in vivo генотоксичность не обнаружена. У лабораторных животных, подвергшихся воздействию клинически значимых уровней, наблюдались следующие изменения, которые на сегодняшний день не были подтверждены долгосрочными клиническими исследованиями: у крыс наблюдалось отложение пигмента в щитовидной железе; у обезьяны циномолгус Сообщалось о гипертрофии фолликулярных клеток щитовидной железы, пониженном уровне Т3 в плазме, пониженной концентрации гемоглобина и снижении количества красных и белых кровяных телец; Сообщалось о помутнении хрусталика и катаракте у собак (о помутнении хрусталика / катаракты см. Раздел 5.1).
В исследовании токсичности эмбриона и плода на кроликах частота сгибания запястья и предплюсны у плода была увеличена, что проявилось в присутствии очевидных материнских эффектов, таких как снижение прибавки в весе.Эти эффекты были очевидны при уровнях воздействия на мать, аналогичных или немного превышающих уровни воздействия на человека при максимальной терапевтической дозе. Актуальность этих результатов для людей неизвестна.
В исследовании фертильности на крысах наблюдалось следующее: предельное снижение фертильности самцов и псевдобеременность, длительные периоды течки, увеличение прекоитального интервала и снижение частоты беременностей. Эти эффекты связаны с повышенным уровнем пролактина и не имеют прямого отношения к человеку. из-за видовых различий в гормональном контроле воспроизводства.
06.0 ФАРМАЦЕВТИЧЕСКАЯ ИНФОРМАЦИЯ
06.1 Вспомогательные вещества
Ядро
Гипромеллоза 2910
Гипромеллоза 2208
Микрокристаллическая целлюлоза
Безводный цитрат натрия
Стеарат магния.
Покрытие
Диоксид титана (E171)
Гипромеллоза 2910
Макрогол / ПЭГ 400
Полисорбат 80
Оксид железа желтый (E172) (только таблетки по 50, 200 и 300 мг)
Оксид железа красный (E172) (только таблетки по 50, 200 и 300 мг)
Оксид железа черный (E172) (только таблетки по 50 и 300 мг).
06.2 Несовместимость
Непригодный.
06.3 Срок действия
2 года.
06.4 Особые меры предосторожности при хранении
Это лекарство не требует особых условий хранения.
06.5 Характер непосредственной упаковки и содержимого упаковки
• PVC / Aclar - алюминиевые блистеры в картонных коробках.
50 мг: 10, 10x1 (стандартная доза с перфорированным блистером), 30, 30x1 (стандартная доза с перфорированным блистером), 60 или 60x1 (стандартная доза с перфорированным блистером) таблеток пролонгированного действия
150 мг: 30, 30x1 (стандартная доза с перфорированным блистером), 60 или 60x1 (стандартная доза с перфорированным блистером) таблеток пролонгированного действия
200 мг: 10, 10x1 (стандартная доза с перфорированным блистером), 30, 30x1 (стандартная доза с перфорированным блистером), 60, 60x1 (стандартная доза с перфорированным блистером), 100 или 100x1 (стандартная доза с перфорированным блистером) таблетки пролонгированного действия
300 мг: 10, 10x1 (стандартная доза с перфорированным блистером), 30, 30x1 (стандартная доза с перфорированным блистером), 60, 60x1 (стандартная доза с перфорированным блистером), 100 или 100x1 (стандартная доза с перфорированным блистером) таблетки пролонгированного действия
400 мг: 10, 10x1 (стандартная доза с перфорированным блистером), 30, 30x1 (стандартная доза с перфорированным блистером), 60, 60x1 (стандартная доза с перфорированным блистером), 100 или 100x1 (стандартная доза с перфорированным блистером) таблетки пролонгированного действия .
• Контейнеры из ПНД по 60 таблеток.
Не все размеры упаковки могут быть проданы.
06.6 Инструкции по эксплуатации и обращению
Никаких особых инструкций.
07.0 ДЕРЖАТЕЛЬ РАЗРЕШЕНИЯ НА МАРКЕТИНГ
Mylan S.p.A., Via Vittor Pisani 20, 20124 Милан
08.0 НОМЕР РАЗРЕШЕНИЯ НА МАРКЕТИНГ
043057013 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 50 МГ" 10 ТАБЛЕТКОВ В БЛИСТЕРЕ PVC / ACLAR-AL
043057025 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 50 МГ" 30 ТАБЛЕТКОВ В БЛИСТЕРЕ ПВХ / ACLAR-AL
043057037 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 50 МГ" 60 ТАБЛЕТКОВ В БЛИСТЕРЕ PVC / ACLAR-AL
043057049 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 150 МГ" 30 ТАБЛЕТКОВ В БЛИСТЕРЕ ИЗ ПВХ / ACLAR-AL
043057052 - "ТАБЛЕТКИ ПРОДОЛЖЕННОГО ВЫПУСКА 150 МГ" 60 ТАБЛЕТКОВ В БЛИСТЕРЕ ИЗ ПВХ / ACLAR-AL
043057064 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 200 МГ" 10 ТАБЛЕТКОВ В БЛИСТЕРЕ ИЗ ПВХ / ACLAR-AL
043057076 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 200 МГ" 30 ТАБЛЕТКОВ В БЛИСТЕРЕ ИЗ ПВХ / ACLAR-AL
043057088 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 200 МГ" 60 ТАБЛЕТКОВ В БЛИСТЕРЕ PVC / ACLAR-AL
043057090 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 200 МГ" 100 ТАБЛЕТКОВ В БЛИСТЕРЕ PVC / ACLAR-AL
043057102 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 300 МГ" 10 ТАБЛЕТКОВ В БЛИСТЕРЕ ИЗ ПВХ / ACLAR-AL
043057114 - "ТАБЛЕТКИ ПРОДОЛЖЕННОГО ВЫПУСКА 300 МГ" 30 ТАБЛЕТКОВ В БЛИСТЕРЕ ИЗ ПВХ / ACLAR-AL
043057126 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 300 МГ" 60 ТАБЛЕТКОВ В БЛИСТЕРЕ PVC / ACLAR-AL
043057138 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 300 МГ" 100 ТАБЛЕТКОВ В БЛИСТРЕРЕ PVC / ACLAR-AL
043057140 - "ТАБЛЕТКИ ПРОДОЛЖЕННОГО ВЫПУСКА 400 МГ" 30 ТАБЛЕТКОВ В БЛИСТЕРЕ ИЗ ПВХ / ACLAR-AL
043057153 - "ТАБЛЕТКИ ПРОДОЛЖЕННОГО ВЫПУСКА 400 МГ" 60 ТАБЛЕТКОВ В БЛИСТЕРЕ PVC / ACLAR-AL
043057165 - "ТАБЛЕТКИ ПРОДОЛЖЕННОГО ВЫПУСКА 400 МГ" 100 ТАБЛЕТКОВ В БЛИСТЕРЕ PVC / ACLAR-AL
043057177 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 50 МГ" 10X1 ТАБЛЕТКИ В БЛИСТЕРЕ ОДНОЙ ДОЗЫ PVC / ACLAR-AL
043057189 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 50 МГ" ТАБЛЕТКИ 30X1 В БЛИСТЕРЕ ОДНОЙ ДОЗЫ PVC / ACLAR-AL
043057191 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 50 МГ" ТАБЛЕТКИ 60X1 В БЛИСТЕРЕ ОДНОЙ ДОЗЫ PVC / ACLAR-AL
043057203 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 50 МГ" 60 ТАБЛЕТКОВ В КОНТЕЙНЕРЕ ПНД
043057215 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «150 МГ» 30X1 ТАБЛЕТКИ В БЛИСТЕРЕ ОДНОЙ ДОЗЫ PVC / ACLAR-AL
043057227 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «150 МГ» 60X1 ТАБЛЕТКИ В БЛИСТЕРЕ ОДНОЙ ДОЗЫ PVC / ACLAR-AL
043057239 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 150 МГ" 60 ТАБЛЕТКОВ В КОНТЕЙНЕРЕ ПНД
043057241 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «200 МГ» 10X1 ТАБЛЕТКИ В ОДНОДОЗОВЫХ БЛИСТЕРАХ PVC / ACLAR-AL
043057254 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «200 МГ» 30X1 ТАБЛЕТКИ В ОДНОДОЗОВЫХ БЛИСТЕРАХ PVC / ACLAR-AL
043057266 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «200 МГ» 60X1 ТАБЛЕТКИ В ОДНОДОЗОВЫХ БЛИСТЕРАХ PVC / ACLAR-AL
043057278 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 200 МГ" ТАБЛЕТКИ 100X1 В БЛИСТЕРЕ ОДНОЙ ДОЗЫ PVC / ACLAR-AL
043057280 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 200 МГ" 60 ТАБЛЕТКОВ В КОНТЕЙНЕРЕ ПНД
043057292 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 300 МГ" 10X1 ТАБЛЕТКИ В БЛИСТЕРЕ ОДНОЙ ДОЗЫ PVC / ACLAR-AL
043057304 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «300 МГ» 30X1 ТАБЛЕТКИ В БЛИСТЕРЕ ОДНОЙ ДОЗЫ PVC / ACLAR-AL
043057316 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «300 МГ» 60X1 ТАБЛЕТКИ В ОДНОДОЗОВЫХ БЛИСТЕРАХ PVC / ACLAR-AL
043057328 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «300 МГ» 100X1 ТАБЛЕТКИ В ОДНОДОЗОВЫХ БЛИСТЕРАХ PVC / ACLAR-AL
043057330 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 300 МГ" 60 ТАБЛЕТКОВ В КОНТЕЙНЕРЕ ПНД
043057342 - "ТАБЛЕТКИ ПРОДОЛЖЕННОГО ВЫПУСКА 400 МГ" 10 ТАБЛЕТКОВ В БЛИСТЕРЕ ИЗ ПВХ / ACLAR-AL
043057355 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «400 МГ» 10X1 ТАБЛЕТКИ В ОДНОДОЗОВЫХ БЛИСТЕРАХ PVC / ACLAR-AL
043057367 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «400 МГ» 30X1 ТАБЛЕТКИ В ОДНОДОЗОВЫХ БЛИСТЕРАХ PVC / ACLAR-AL
043057379 - ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА «400 МГ» 60X1 ТАБЛЕТКИ В ОДНОДОЗОВЫХ БЛИСТЕРАХ PVC / ACLAR-AL
043057381 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 400 МГ" ТАБЛЕТКИ 100X1 В БЛИСТЕРЕ ДЛЯ ОДНОДозы ПВХ / ACLAR-AL
043057393 - "ТАБЛЕТКИ РАСШИРЕННОГО ВЫПУСКА 400 МГ" 60 ТАБЛЕТКОВ В КОНТЕЙНЕРЕ ПНД
09.0 ДАТА ПЕРВОГО РАЗРЕШЕНИЯ ИЛИ ПРОДЛЕНИЯ РАЗРЕШЕНИЯ
10.0 ДАТА ПЕРЕСМОТРА ТЕКСТА
Январь 2015