Активные ингредиенты: амисульприд
ДЕНИБАН 50 мг таблетки
Почему используется Денибан? Для чего это?
Фармакотерапевтическая группа
Психолептики, бензамиды.
Показания к применению
Лечение (краткосрочное - среднесрочное) дистимии.
Противопоказания Когда нельзя применять Денибан
Повышенная чувствительность к действующему веществу или любому из вспомогательных веществ.
Феохромоцитома.
Сочетание пролактинзависимых опухолей, таких как пролактиномы гипофиза и опухоли молочной железы.
Не применять при подтвержденной или предполагаемой беременности и в период кормления грудью. Женщинам детородного возраста, не использующим адекватные средства контрацепции.
Не применять детям и ни в коем случае не применять только в конце полового созревания.
Комбинация со следующими лекарствами из-за возможного возникновения пуантах де трепанации:
- антиаритмические средства класса Ia, такие как хинидин, дизопирамид;
- антиаритмические средства класса III, такие как амиодарон, соталол;
- другие лекарственные средства, такие как бепридил, цизаприд, сульфоприд, тиоридазин, метадон внутривенно, эритромицин внутривенно, винкамин, галофантрин, пентамидин, спарфлоксацин (см. раздел «Взаимодействие»).
Комбинация с леводопой (см. Раздел «Взаимодействие»).
Меры предосторожности при использовании Что следует знать перед приемом Денибана
У пациентов пожилого возраста амисульприд, как и другие нейролептики, следует применять с особой осторожностью из-за возможного риска развития артериальной гипотензии и седативного эффекта. Снижение дозировки также может потребоваться при почечной недостаточности.
Поскольку препарат выводится через почки, в случае почечной недостаточности дозу необходимо уменьшить или назначить прерывистое лечение (см. Раздел «Доза, способ и время приема»).
Амисульприд может снизить судорожный порог. Таким образом, пациенты с эпилептическими эпизодами в анамнезе должны находиться под пристальным наблюдением во время лечения.
Как и в случае с другими антидопаминергическими средствами, следует соблюдать особую осторожность при назначении амисульприда пациентам с паркинсонизмом, поскольку болезнь может обостриться. Амисульприд следует применять только в том случае, если нельзя избежать лечения нейролептиками.
Гипергликемия наблюдалась у пациентов, получавших некоторые атипичные нейролептики, включая амисульприд. Таким образом, пациенты с определенным диагнозом сахарного диабета или с факторами риска развития диабета должны проходить соответствующий гликемический мониторинг при терапии амисульпридом.
Сообщалось о лейкопении, нейтропении и агранулоцитозе при приеме нейролептиков, включая Денибан. Необъяснимые инфекции или лихорадка могут указывать на дискразию крови (см. Раздел «Нежелательные эффекты»), что требует «немедленного гематологического исследования.
Взаимодействия Какие лекарства или продукты могут изменить действие Денибана
Сообщите своему врачу или фармацевту, если вы принимаете или недавно принимали какие-либо другие лекарства, даже те, которые не отпускаются по рецепту.
Связь с другими психотропными препаратами требует особой осторожности и бдительности со стороны врача, чтобы избежать неожиданных нежелательных эффектов от взаимодействия.
При одновременном применении нейролептиков с препаратами, удлиняющими интервал QT, повышается риск развития сердечной аритмии.
Противопоказанные ассоциации
Препараты, способные вызывать пуанты:
- антиаритмические средства класса Ia, такие как хинидин, дизопирамид;
- антиаритмические средства класса III, такие как амиодарон, соталол;
- другие препараты, такие как бепридил, цизаприд, сультоприд, тиоридазин, внутривенно метадон, внутривенно эритромицин, внутривенно винкамин, галофантрин, пентамидин, спарфлоксацин.
Леводопа: взаимный антагонизм эффектов между леводопой и нейролептиками. Амисульприд может противодействовать эффекту агонистов дофамина, таких как бромокриптин и ропинирол.
Не применяйте одновременно с препаратами, вызывающими изменения электролитов, такими как препараты, вызывающие гипокалиемию, такие как гипокалиемические диуретики, стимулирующие слабительные средства, амфотерицин B внутривенно, глюкокортикоиды, тетракозактиды.
Гипокалиемия требует коррекции.
Ассоциации не рекомендуются
Амисульприд может усиливать основные эффекты алкоголя.
Лекарства, которые увеличивают риск возникновения Torsades de Pointes или могут удлинять интервал QT:
- препараты, вызывающие брадикардию: бета-адреноблокаторы, блокаторы кальциевых каналов, квалидилтиазем и верапамил, клонидин, гуанфацин, дигиталис
- нейролептики, такие как пимозид, галоперидол, имипрамин, антидепрессанты, литий
- некоторые антигистаминные препараты
- некоторые противомалярийные средства (например, мефлохин)
Ассоциации, на которые следует обратить внимание
- Депрессанты ЦНС: снотворные, транквилизаторы, анестетики, анальгетики, седативные антигистаминные препараты H1, барбитураты, бензодиазепины и другие анксиолитики, клонидин и производные;
- гипотензивные препараты и другие гипотензивные препараты.
Предупреждения Важно знать, что:
Сообщалось о потенциально смертельном симптомокомплексе, называемом злокачественным нейролептическим синдромом, во время лечения нейролептическими препаратами. Для этого синдрома характерны: гиперпирексия, ригидность мышц, акинезия, вегетативные расстройства (нерегулярность пульса и артериального давления, потоотделение, тахикардия, аритмия), повышенные значения креатинфосфокиназы; изменения в сознании, которые могут прогрессировать до ступора и комы. В случае гипертермии, особенно в высоких дозах, лечение всеми нейролептическими препаратами, включая амисульприд, следует прекратить.
Удлинение интервала QT
С осторожностью применять пациентам с сердечно-сосудистыми заболеваниями или удлинением интервала QT в семейном анамнезе.
Избегайте одновременной терапии с другими нейролептиками.
Амисульприд вызывает дозозависимое удлинение интервала QT (см. Раздел «Нежелательные эффекты»). Известно, что этот эффект увеличивает риск тяжелых желудочковых аритмий, таких как пуанты.
Перед введением и, если возможно, в зависимости от клинического состояния пациента, рекомендуется контролировать факторы, которые могут способствовать возникновению этого нарушения ритма, такие как:
- брадикардия менее 55 ударов в минуту;
- нарушение электролитного баланса, особенно гипокалиемия;
- врожденный или приобретенный удлиненный интервал QT;
- продолжающееся лечение препаратами, способными вызвать выраженную брадикардию (
Цереброваскулярные события
Приблизительно трехкратное увеличение риска цереброваскулярных событий наблюдалось в рандомизированных клинических испытаниях по сравнению с плацебо в популяции пожилых пациентов с деменцией, получавших некоторые атипичные нейролептики. Механизм этого повышенного риска неизвестен. Нельзя исключить повышенный риск для других нейролептиков или других групп пациентов. Денибан следует применять с осторожностью пациентам с факторами риска инсульта.
Пожилые пациенты с деменцией:
Пожилые пациенты с психозом, связанным с деменцией, принимающие антипсихотические препараты, имеют повышенный риск смерти.
Анализ семнадцати плацебо-контролируемых клинических испытаний (10-недельная продолжительность) с участием пациентов, которые в основном принимали атипичные антипсихотические препараты, выявил риск смерти 1,6: 1 у пациентов, получавших препарат, что в 7 раз больше, чем у пациентов, получавших плацебо. В 10-недельном контролируемом исследовании уровень смертности пациентов, получавших препарат, составил примерно 4,5% по сравнению с 2,6% в группе плацебо.
Хотя причины смерти во время клинических испытаний атипичных нейролептиков были разными, большинство из них были либо сердечно-сосудистыми (например, сердечная недостаточность, внезапная смерть), либо инфекционными (например, пневмония).
Наблюдательные исследования показывают, что, как и в случае с атипичными антипсихотическими препаратами, лечение обычными антипсихотическими препаратами может также увеличить смертность. Неясна степень, в которой обнаружение повышенной смертности в обсервационных исследованиях может быть связано с антипсихотическими препаратами, а не с некоторыми конкретными характеристиками пациента.
Венозная тромбоэмболия
Сообщалось о случаях венозной тромбоэмболии (ВТЭ) при применении антипсихотических препаратов. Поскольку пациенты, принимающие антипсихотические препараты, часто имеют приобретенные факторы риска ВТЭ, все возможные факторы риска ВТЭ должны быть выявлены до и во время лечения. При применении Денибана необходимо принять профилактические меры. .
После резкого прекращения приема высоких терапевтических доз антипсихотических препаратов были описаны симптомы отмены, включая тошноту, рвоту и бессонницу. Психотические симптомы также могут повторяться, и при приеме амисульприда сообщалось о развитии непроизвольных двигательных расстройств (таких как акатизия, дистония и дискинезия). Поэтому рекомендуется постепенное прекращение приема амисульприда.
Беременность, кормление грудью и фертильность:
Прежде чем принимать какое-либо лекарство, посоветуйтесь со своим врачом или фармацевтом.
Беременность
Он противопоказан в случаях известной или предполагаемой беременности. У новорожденных от матерей, которые принимали обычные или атипичные нейролептики, включая Денибан, в последнем триместре (последние три месяца беременности) наблюдались следующие симптомы: тремор, скованность и / или o мышечная слабость, сонливость, возбуждение, проблемы с дыханием и трудности с приемом пищи (см. «Побочные эффекты»). Если у вашего ребенка проявляются какие-либо из этих симптомов, обратитесь к врачу.
У животных амисульприд не проявлял прямого токсического действия на репродуктивную функцию. Наблюдалось снижение фертильности, связанное с фармакологическими эффектами препарата (опосредованное действием пролактина). Тератогенных эффектов не наблюдалось.
Время кормления
Неизвестно, выделяется ли амисульприд с грудным молоком; поэтому грудное вскармливание противопоказано.
Влияние на способность управлять автомобилем и работать с механизмами
Даже при использовании в соответствии с рекомендациями амисульприд может вызвать сонливость и, следовательно, способность управлять автомобилем или работать с механизмами может быть нарушена (см. Раздел «Нежелательные эффекты»).
Важная информация о некоторых ингредиентах:
ДЕНИБАН содержит лактозу, поэтому, если врач сказал вам, что у вас непереносимость некоторых сахаров, обратитесь к врачу, прежде чем принимать это лекарство.
Дозировка и способ применения Как применять Денибан: Дозировка
Одна таблетка в день или второе медицинское заключение.
Пациенты пожилого возраста: безопасность амисульприда была оценена у ограниченного числа пациентов пожилого возраста. Амисульприд следует применять с особой осторожностью из-за возможного риска гипотензии и седативного эффекта. Дозировка должна быть тщательно установлена врачом, который должен будет оценить возможное снижение дозировки, указанной выше. Снижение дозировки также может потребоваться при почечной недостаточности.
Дети: эффективность и безопасность амисульприда от полового созревания до 18 лет не установлены. Поэтому применение амисульприда от полового созревания до 18 лет не рекомендуется. Амисульприд противопоказан детям до полового созревания, так как его безопасность еще не установлена (см. Раздел «Противопоказания»).
Почечная недостаточность: амисульприд выводится почками. В случае почечной недостаточности дозу следует уменьшить наполовину у пациентов с клиренсом креатинина от 30 до 60 мл / мин и на одну треть у пациентов с клиренсом от 10 до 30 мл / мин. Тяжелая почечная недостаточность (клиренс креатинина <10 мл / мин). / мин) этим пациентам рекомендуется особая осторожность (см. раздел «Меры предосторожности при применении»).
Печеночная недостаточность: амисульприд плохо метаболизируется, поэтому снижение дозы не требуется.
Передозировка Что делать, если вы приняли слишком много Денибана
Опыт применения амисульприда при передозировке ограничен. Сообщалось об усилении известных фармакологических эффектов препарата. К ним относятся сонливость, седативный эффект, гипотензия, экстрапирамидные симптомы и кому. Сообщалось о случаях летального исхода в основном в сочетании с другими агентами. Психотропные.
В случае острой передозировки следует учитывать возможность приема нескольких препаратов.
Поскольку амисульприд плохо поддается диализу, гемодиализ бесполезен для отмены препарата. Специфического антидота не существует. Следовательно, необходимо ввести соответствующие терапевтические меры и тщательный мониторинг жизненно важных функций: постоянный мониторинг сердца (риск удлинения интервала QT) до тех пор, пока пациент не перестанет стабилизированный. При появлении тяжелых экстрапирамидных симптомов следует назначить холинолитики.
В случае случайного проглатывания / приема передозировки ДЕНИБАН немедленно сообщите об этом своему врачу или обратитесь в ближайшую больницу.Если у вас есть дополнительные вопросы по использованию ДЕНИБАН, спросите своего врача или фармацевта.
Побочные эффекты Каковы побочные эффекты Денибана
Как и все лекарства, ДЕНИБАН может вызывать побочные эффекты, но не у всех.
Нежелательные эффекты были отсортированы по частотным классам, используя следующее соглашение: очень часто (> 1/10); общие (> 1/100, 1/1000, 1/10 000,
Данные клинических исследований
Следующие побочные эффекты наблюдались в контролируемых клинических испытаниях. Следует отметить, что в некоторых случаях бывает сложно отличить нежелательные явления от симптомов основного заболевания.
Со стороны нервной системы:
Очень часто: могут появиться экстрапирамидные симптомы: тремор, ригидность, гипокинез, гиперсаливация, акатизия, дискинезия. Эти симптомы обычно слабо выражены при оптимальных дозировках и частично обратимы при приеме противопаркинсонических препаратов даже без отмены амисульприда. Дозозависимая частота экстрапирамидных симптомов остается чрезвычайно низкой при лечении пациентов с преимущественно негативными симптомами в дозах от 50 до 300 мг / день.
Часто: может возникнуть острая дистония (спастическая кривошея, окулогирный криз, тризм), которая обратима при приеме противопаркинсонических препаратов, даже без прекращения терапии амисульпридом. Сонливость.
Нечасто: сообщалось о поздней дискинезии, характеризующейся ритмичными непроизвольными движениями, преимущественно затрагивающими язык и / или лицо, обычно после длительного приема амисульприда. Лечение противопаркинсоническими препаратами неэффективно или может вызвать ухудшение симптомов. Судороги.
Психиатрические расстройства:
Часто: бессонница, беспокойство, возбуждение, психомоторная возбудимость, нарушения оргазма.
Частота неизвестна: путаница.
Желудочно-кишечные расстройства:
Часто: запор, тошнота, рвота, сухость во рту, диспепсия.
Эндокринные расстройства:
Часто: амисульприд вызывает обратимое повышение уровня пролактина в плазме после отмены препарата. Это увеличение может быть связано с началом галактореи, аменореи, гинекомастии, мастодинии и эректильной дисфункции.
Нарушения обмена веществ и питания:
Нечасто: гипергликемия (см. Раздел «Меры предосторожности при использовании»). Частота неизвестна: гипертриглицеридемия и гиперхолестеринемия.
Сердечные расстройства:
Часто: гипотония.
Нечасто: брадикардия и сердцебиение.
Диагностические тесты:
Часто: увеличение веса.
Нечасто: повышение активности печеночных ферментов, особенно трансаминаз.
Со стороны иммунной системы:
Нечасто: аллергические реакции.
Также наблюдались: склонность к ознобу низкой интенсивности, одышка низкой интенсивности, мышечные боли.
Постмаркетинговые данные
О следующих побочных реакциях сообщалось только как спонтанные:
- Заболевания крови и лимфатической системы
Частота неизвестна: лейкопения, нейтропения и агранулоцитоз (см. Раздел «Меры предосторожности при применении»).
- Со стороны нервной системы:
Частота неизвестна: злокачественный нейролептический синдром, опасное для жизни осложнение (см. Раздел «Особые предупреждения»).
- Сердечные расстройства:
Частота неизвестна: удлинение интервала QT, желудочковые аритмии, такие как torsades de pointes, желудочковая тахикардия, которая может привести к фибрилляции желудочков или остановке сердца, внезапная смерть (см. Раздел «Особые предупреждения»).
- Сосудистые расстройства:
Частота неизвестна: венозная тромбоэмболия, включая тромбоэмболию легочной артерии, иногда со смертельным исходом, и тромбоз глубоких вен (см. Раздел «Особые предупреждения»).
- Со стороны кожи и подкожной клетчатки:
Частота неизвестна: ангионевротический отек, крапивница.
- Условия беременности, послеродового периода и перинатальные состояния
Частота неизвестна: неонатальный абстинентный синдром, экстрапирамидные симптомы (см. Раздел «Беременность и лактация»).
Если вы заметили какие-либо побочные эффекты, поговорите со своим врачом или фармацевтом, включая любые возможные побочные эффекты, не указанные в данном информационном листке. Вы также можете сообщить о побочных эффектах непосредственно через веб-сайт Итальянского агентства по лекарственным средствам: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse Сообщив о побочных эффектах, вы поможете получить дополнительную информацию о безопасности этого лекарства.
Срок действия и удержание
Срок годности: см. Срок годности, указанный на упаковке.
Срок годности относится к продукту в неповрежденной упаковке, правильно хранящемуся.
Предупреждение: не используйте лекарство после истечения срока годности, указанного на упаковке.
Лекарства нельзя выбрасывать в канализацию или бытовые отходы. Узнайте у фармацевта, как утилизировать лекарства, которые вы больше не используете. Это поможет защитить окружающую среду. Храните это лекарство в недоступном для детей месте.
Состав и лекарственная форма
Состав
Каждая таблетка содержит:
Действующее вещество: амисульприд 50 мг.
Вспомогательные вещества: карбоксиметилкрахмал натрия (тип А), моногидрат лактозы, микрокристаллическая целлюлоза, гипромеллоза, стеарат магния.
Лекарственная форма и содержание
12 таблеток для перорального применения.
Листовка с исходным кодом: AIFA (Итальянское агентство по лекарственным средствам). Контент опубликован в январе 2016 года. Представленная информация может быть устаревшей.
Чтобы иметь доступ к самой последней версии, рекомендуется зайти на сайт AIFA (Итальянское агентство по лекарственным средствам). Заявление об ограничении ответственности и полезная информация.
01.0 НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
ДЕНИБАН ТАБЛЕТКИ 50 МГ
02.0 КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ
Каждая таблетка содержит:
Активный принцип: амисульприд 50 мг
Вспомогательные вещества: Моногидрат лактозы 34,8 мг.
Список вспомогательных веществ см. В разделе 6.1.
03.0 ФАРМАЦЕВТИЧЕСКАЯ ФОРМА
Таблетки.
04.0 КЛИНИЧЕСКАЯ ИНФОРМАЦИЯ
04.1 Терапевтические показания
Лечение (краткосрочное и среднесрочное) дистимии.
04.2 Дозировка и способ применения
Одна таблетка в день или второе медицинское заключение.
Пожилые пациенты: Безопасность амисульприда была оценена на ограниченном количестве пожилых пациентов. Амисульприд следует применять с особой осторожностью из-за возможного риска гипотензии и седативного эффекта. Дозировка должна быть тщательно установлена врачом, который должен будет оценить возможное снижение дозировки, указанной выше. Снижение дозировки также может потребоваться при почечной недостаточности.
Дети: эффективность и безопасность амисульприда от полового созревания до 18 лет не установлены. Поэтому применение амисульприда от полового созревания до 18 лет не рекомендуется. Амисульприд противопоказан детям до полового созревания, поскольку его безопасность еще не установлена (см. Раздел 4.3).
Почечная недостаточность: амисульприд выводится почками. В случае почечной недостаточности дозу следует уменьшить наполовину у пациентов с клиренсом креатинина от 30 до 60 мл / мин и до одной трети у пациентов с клиренсом от 10 до 30 мл / мин. Нет данных у пациентов с тяжелой почечной недостаточностью (клиренс креатинина
Печеночная недостаточность: амисульприд плохо метаболизируется, поэтому снижения дозы не требуется.
04.3 Противопоказания
Повышенная чувствительность к действующему веществу или любому из вспомогательных веществ.
Феохромоцитома.
Сочетание пролактинзависимых опухолей, таких как пролактиномы гипофиза и опухоли молочной железы.
Не применять при подтвержденной или предполагаемой беременности и в период кормления грудью. Женщинам детородного возраста, не использующим адекватные средства контрацепции.
Не применять детям и ни в коем случае не применять только в конце полового созревания.
Связь со следующими препаратами при возможном возникновении пуантах де torsades:
• антиаритмические средства класса Ia, такие как хинидин, дизопирамид;
• антиаритмические препараты III класса, такие как амиодарон, соталол;
• другие препараты, такие как бепридил, цизаприд, сульфоприд, тиоридазин, метадон внутривенно, эритромицин внутривенно, винкамин, галофантрин, пентамидин, спарфлоксацин (см. Раздел 4.5).
Комбинация с леводопой (см. Раздел 4.5).
04.4 Особые предупреждения и соответствующие меры предосторожности при использовании
• Сообщалось о потенциально смертельном симптомокомплексе, называемом злокачественным нейролептическим синдромом, во время лечения нейролептическими препаратами. Для этого синдрома характерны: гиперпирексия, ригидность мышц, акинезия, вегетативные расстройства (нерегулярность пульса и артериального давления, потоотделение, тахикардия, аритмия), повышенные значения креатинфосфокиназы; изменения в сознании, которые могут прогрессировать до ступора и комы. В случае гипертермии, особенно в высоких дозах, следует прекратить лечение всеми антипсихотическими препаратами, включая амисульприд.
• Как и в случае с другими антидопаминергическими средствами, следует соблюдать особую осторожность при назначении амисульприда пациентам с паркинсонизмом, поскольку болезнь может обостриться. Амисульприд следует использовать только тогда, когда нельзя избежать лечения нейролептиками.
• Удлинение интервала QT.
Используйте с осторожностью у пациентов с сердечно-сосудистыми заболеваниями или с семейным анамнезом удлинения интервала QT.
Избегайте одновременной терапии с другими нейролептиками.
Амисульприд вызывает дозозависимое удлинение интервала QT (см. Раздел 4.8). Известно, что этот эффект увеличивает риск серьезных желудочковых аритмий, таких как пуанты.
Перед введением и, если возможно, в зависимости от клинического состояния пациента, рекомендуется контролировать факторы, которые могут способствовать возникновению этого нарушения ритма, такие как:
• брадикардия менее 55 ударов в минуту;
• нарушение электролитного баланса, особенно гипокалиемия;
• врожденный или приобретенный удлиненный интервал QT;
• продолжающееся лечение препаратами, способными вызвать выраженную брадикардию (
• Цереброваскулярные нарушения
В рандомизированных клинических исследованиях против Примерно трехкратное увеличение риска цереброваскулярных событий наблюдалось в популяции пожилых пациентов с деменцией, получавших некоторые атипичные нейролептики. Механизм этого повышенного риска неизвестен. Нельзя исключить повышенный риск для других нейролептиков или других групп пациентов. Денибан следует применять с осторожностью пациентам с факторами риска инсульта.
• Пожилые пациенты с деменцией:
Пожилые пациенты с психозом, связанным с деменцией, принимающие антипсихотические препараты, имеют повышенный риск смерти.
Анализ семнадцати плацебо-контролируемых клинических испытаний (10-недельная продолжительность) с участием пациентов, которые в основном принимали атипичные антипсихотические препараты, выявил риск смерти 1,6: 1 у пациентов, получавших препарат, что в 7 раз больше, чем у пациентов, получавших плацебо. В 10-недельном контролируемом исследовании уровень смертности пациентов, получавших препарат, составил примерно 4,5% по сравнению с 2,6% в группе плацебо.
Хотя причины смерти во время клинических испытаний атипичных нейролептиков были разными, большинство из них были либо сердечно-сосудистыми (например, сердечная недостаточность, внезапная смерть), либо инфекционными (например, пневмония).
Наблюдательные исследования показывают, что, как и в случае с атипичными антипсихотическими препаратами, лечение обычными антипсихотическими препаратами может также увеличить смертность. Неясна степень, в которой обнаружение повышенной смертности в обсервационных исследованиях может быть связано с антипсихотическими препаратами, а не с некоторыми конкретными характеристиками пациента.
• Венозная тромбоэмболия
Сообщалось о случаях венозной тромбоэмболии (ВТЭ) при применении антипсихотических препаратов.
Поскольку пациенты, получающие нейролептики, часто имеют приобретенные факторы риска ВТЭ, все возможные факторы риска ВТЭ должны быть идентифицированы до и во время лечения Денибаном и приняты профилактические меры.
• Гипергликемия наблюдалась у пациентов, получавших некоторые атипичные нейролептики, включая амисульприд. Таким образом, пациенты с определенным диагнозом сахарного диабета или с факторами риска развития диабета должны проходить соответствующий гликемический мониторинг при терапии амисульпридом.
• Амисульприд может снизить судорожный порог. Таким образом, пациенты с эпилептическими эпизодами в анамнезе должны находиться под пристальным наблюдением во время лечения.
• Поскольку препарат выводится почками, в случае почечной недостаточности дозу необходимо уменьшить или назначить периодическое лечение (см. Раздел 4.2).
• У пожилых пациентов амисульприд, как и другие нейролептики, следует применять с особой осторожностью из-за возможного риска гипотензии и седативного эффекта. Снижение дозировки также может потребоваться при почечной недостаточности.
• Симптомы отмены, включая тошноту, рвоту и бессонницу, были описаны после резкого прекращения приема высоких терапевтических доз антипсихотических препаратов. Психотические симптомы также могут повторяться, и при приеме амисульприда сообщалось о развитии непроизвольных двигательных расстройств (таких как акатизия, дистония и дискинезия). Поэтому рекомендуется постепенное прекращение приема амисульприда.
• Сообщалось о лейкопении, нейтропении и агранулоцитозе при приеме нейролептиков, включая Денибан. Необъяснимые инфекции или лихорадка могут указывать на дискразию крови (см. Раздел 4.8), требующие немедленного гематологического исследования.
Важная информация о некоторых ингредиентах
ДЕНИБАН содержит лактозу, поэтому пациенты с редкими наследственными проблемами непереносимости галактозы, лактазной недостаточностью Лаппа или мальабсорбцией глюкозы-галактозы не должны принимать это лекарство.
04.5 Взаимодействие с другими лекарственными средствами и другие формы взаимодействия
Связь с другими психотропными препаратами требует особой осторожности и бдительности со стороны врача, чтобы избежать неожиданных нежелательных эффектов от взаимодействия.
При одновременном применении нейролептиков с препаратами, удлиняющими интервал QT, повышается риск развития сердечной аритмии.
Противопоказанные ассоциации
Препараты, способные вызывать пуанты:
• антиаритмические средства класса Ia, такие как хинидин, дизопирамид;
• антиаритмические препараты III класса, такие как амиодарон, соталол;
• другие препараты, такие как бепридил, цизаприд, сульфоприд, тиоридазин, метадон внутривенно, эритромицин внутривенно, винкамин внутривенно, галофантрин, пентамидин, спарфлоксацин.
Леводопа: взаимный антагонизм эффектов между леводопой и нейролептиками. Амисульприд может противодействовать эффекту агонистов дофамина, таких как бромокриптин и ропинирол.
Не применяйте одновременно с препаратами, вызывающими изменения электролитов, такими как препараты, вызывающие гипокалиемию, такие как гипокалиемические диуретики, стимулирующие слабительные средства, амфотерицин B внутривенно, глюкокортикоиды, тетракозактиды.
Гипокалиемия требует коррекции.
Ассоциации не рекомендуются
Амисульприд может усиливать основные эффекты алкоголя.
Препараты, которые увеличивают риск возникновения пуантах или могут продлить интервал QT:
• препараты, вызывающие брадикардию: бета-адреноблокаторы, блокаторы кальциевых каналов, такие как дилтиазем и верапамил, клонидин, гуанфацин; наперстянка
• нейролептики, такие как пимозид, галоперидол, имипрамин, антидепрессанты, литий
• некоторые антигистаминные препараты
• некоторые противомалярийные средства (например, мефлохин)
Ассоциации, на которые следует обратить внимание
• Депрессанты ЦНС: снотворные, транквилизаторы, анестетики, анальгетики, седативные антигистаминные препараты H1, барбитураты, бензодиазепины и другие анксиолитики, клонидин и их производные.
• гипотензивные препараты и другие гипотензивные препараты.
04.6 Беременность и кормление грудью
Беременность
Противопоказан при подтвержденной или предполагаемой беременности.
Младенцы, получавшие обычные или атипичные нейролептики, включая Денибан, в третьем триместре беременности, подвержены риску побочных реакций, включая экстрапирамидные симптомы или симптомы отмены, которые могут различаться по степени тяжести и продолжительности после рождения (см. 4.8). Поступали сообщения о возбуждении, гипертонии, гипотонии, треморе, сонливости, респираторной недостаточности, нарушениях приема пищи. Поэтому следует тщательно наблюдать за младенцами.
У животных амисульприд не проявлял прямого токсического воздействия на репродуктивную функцию. Наблюдалось снижение фертильности, связанное с фармакологическими эффектами препарата (эффект, опосредованный пролактином). Тератогенных эффектов не наблюдалось.
Время кормления
Неизвестно, выделяется ли амисульприд с грудным молоком; поэтому грудное вскармливание противопоказано.
04.7 Влияние на способность управлять автомобилем и работать с механизмами
Даже при использовании в соответствии с рекомендациями амисульприд может вызвать сонливость, и, следовательно, способность управлять автомобилем или работать с механизмами может быть нарушена (см. Раздел 4.8).
04.8 Побочные эффекты
Нежелательные эффекты были отсортированы по частотным классам согласно следующему соглашению::
очень часто (≥ 1/10); общие (≥ 1/100;
Данные клинических исследований
Следующие побочные эффекты наблюдались в контролируемых клинических испытаниях. Следует отметить, что в некоторых случаях бывает сложно отличить нежелательные явления от симптомов основного заболевания.
• Расстройства нервной системы.
Очень часто: могут появиться экстрапирамидные симптомы: тремор, ригидность, гипокинез, гиперсаливация, акатизия, дискинезия. Эти симптомы обычно слабо выражены при оптимальных дозировках и частично обратимы при приеме противопаркинсонических препаратов даже без отмены амисульприда. Дозозависимая частота экстрапирамидных симптомов остается чрезвычайно низкой при лечении пациентов с преимущественно негативными симптомами в дозах от 50 до 300 мг / день.
Часто: может возникнуть острая дистония (спастическая кривошея, окулогирный криз, тризм), которая обратима при приеме противопаркинсонических препаратов, даже без прекращения терапии амисульпридом.
Сонливость.
Нечасто: сообщалось о поздней дискинезии, характеризующейся ритмичными непроизвольными движениями, преимущественно затрагивающими язык и / или лицо, обычно после длительного приема амисульприда. Лечение противопаркинсоническими препаратами неэффективно или может вызвать обострение симптомов.
Судороги.
• Психиатрические расстройства
Часто: бессонница, беспокойство, возбуждение, психомоторная возбудимость, нарушения оргазма.
Частота неизвестна: путаница.
• Желудочно-кишечные расстройства
Часто: запор, тошнота, рвота, сухость во рту, диспепсия.
• Эндокринные патологии
Часто: амисульприд вызывает обратимое повышение уровня пролактина в плазме после отмены препарата. Это увеличение может быть связано с началом галактореи, аменореи, гинекомастии, мастодинии и эректильной дисфункции.
• Нарушения обмена веществ и питания.
Нечасто: гипергликемия (см. Раздел 4.4).
Частота неизвестна: гипертриглицеридемия и гиперхолестеринемия.
• Сердечные заболевания
Часто: гипотония.
Нечасто: брадикардия и сердцебиение.
• Диагностические тесты
Часто: увеличение веса.
Нечасто: повышение активности печеночных ферментов, особенно трансаминаз.
• Нарушения иммунной системы.
Нечасто: аллергические реакции.
Также наблюдались: склонность к ознобу малой интенсивности, одышка низкой интенсивности, мышечные боли.
Постмаркетинговые данные
О следующих побочных реакциях сообщалось только как спонтанные:
• Нарушения со стороны крови и лимфатической системы.
Частота неизвестна: лейкопения, нейтропения и агранулоцитоз (см. Раздел 4.4).
• Расстройства нервной системы.
Частота неизвестна: злокачественный нейролептический синдром, опасное для жизни осложнение (см. Раздел 4.4).
• Сердечные заболевания
Частота неизвестна: удлинение интервала QT, желудочковые аритмии, такие как torsade de pointes, желудочковая тахикардия, которая может привести к фибрилляции желудочков или остановке сердца, внезапная смерть (см. Раздел 4.4).
• Сосудистые патологии.
Частота неизвестна: венозная тромбоэмболия, включая тромбоэмболию легочной артерии, иногда со смертельным исходом, и тромбоз глубоких вен (см. Раздел 4.4).
• Заболевания кожи и подкожной клетчатки:
Частота неизвестна: ангионевротический отек, крапивница.
• Условия беременности, послеродового периода и перинатального периода.
Частота неизвестна: неонатальный абстинентный синдром, экстрапирамидные симптомы (см. Раздел 4.6).
Сообщение о предполагаемых побочных реакциях.
Отчетность о предполагаемых побочных реакциях, которые возникают после выдачи разрешения на лекарственный препарат, важна, так как позволяет осуществлять постоянный мониторинг соотношения польза / риск лекарственного средства.
Медицинских работников просят сообщать о любых предполагаемых побочных реакциях через веб-сайт Итальянского агентства по лекарственным средствам: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Передозировка
Опыт применения амисульприда при передозировке ограничен. Сообщалось об усилении известных фармакологических эффектов препарата. К ним относятся сонливость, седативный эффект, гипотензия, экстрапирамидные симптомы и кому. Сообщалось о случаях летального исхода в основном в сочетании с другими агентами. Психотропные.
В случае острой передозировки следует учитывать возможность приема нескольких препаратов.
Поскольку амисульприд плохо поддается диализу, гемодиализ бесполезен для отмены препарата. Специфического антидота не существует. Следовательно, необходимо ввести соответствующие терапевтические меры и тщательный мониторинг жизненно важных функций: постоянный мониторинг сердца (риск удлинения интервала QT) до тех пор, пока пациент не перестанет стабилизированный. При появлении тяжелых экстрапирамидных симптомов следует назначить холинолитики.
05.0 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
05.1 Фармакодинамические свойства
Фармакотерапевтическая группа: Психолептики, бензамиды - код АТХ: N05AL05.
Амисульприд представляет собой молекулу, принадлежащую к группе замещенных бензамидов.
Амисульприд избирательно связывается с высокой степенью сродства с подтипами рецепторов дофамина человека D2 и D3, в то время как он не имеет сродства к подтипам рецепторов D1, D4 и D5.
Амисульприд не имеет сродства к серотонинергическим, α-адренергическим, гистаминергическим и холинергическим рецепторам H1 и не связывается с сигма-сайтами.
У животных амисульприд в высоких дозах в основном блокирует постсинаптические рецепторы D2, расположенные в лимбических структурах, по сравнению с рецепторами в полосатом теле. Он не вызывает каталепсию, и после повторного лечения не развивается гиперчувствительность дофаминергических рецепторов D2.
В низких дозах амисульприд преимущественно блокирует пресинаптические рецепторы D2 / D3, вызывая высвобождение дофамина, ответственного за растормаживающее действие препарата.
Кроме того, снижение склонности амисульприда к побочным экстрапирамидным эффектам может быть связано с его предпочтительной активностью на лимбическом уровне.
05.2 Фармакокинетические свойства
У людей амисульприд имеет два пика абсорбции: первый быстро достигается через час после приема, а второй - через 3-4 часа. Соответствующие концентрации в плазме составляют 39 ± 3 и 54 ± 4 нг / мл после введения 50 мг.
Объем распределения 5,8 л / кг. Поскольку связывание с белками низкое (16%), взаимодействие с другими лекарствами маловероятно.
Абсолютная биодоступность - 48%. Амисульприд плохо метаболизируется: были идентифицированы два неактивных метаболита, что соответствует примерно 4% дозы. Накопления не происходит, и кинетика остается неизменной после повторного дозирования. После приема внутрь период полувыведения амисульприда составляет примерно 12 часов.
Амисульприд выводится с мочой в неизмененном виде. 50% внутривенной дозы выводится с мочой, 90% которой выводится в первые 24 часа. Почечный клиренс составляет порядка 20 л / ч или 330 мл / мин.
Прием пищи, богатой углеводами (с жидкой частью, равной 68%), значительно снижает AUC, Tmax и Cmax амисульприда, в то время как после приема пищи с высоким содержанием жиров никаких изменений не наблюдается. Однако значение этих данных для клинической практики неизвестно.
Почечная недостаточность: период полувыведения не изменяется у пациентов с почечной недостаточностью, в то время как системный клиренс снижается в 2,5-3 раза. AUC амисульприда увеличивается в два раза в случае легкой почечной недостаточности и примерно в 10 раз в случае почечной недостаточности. умеренная почечная недостаточность. Однако опыт ограничен, и нет данных о дозах выше 50 мг.
Амисульприд плохо диализируется.
У пожилых пациентов (> 65 лет) фармакокинетические данные ограничены и демонстрируют увеличение Cmax, T½ и AUC на 10-30% после перорального приема в дозе 50 мг. Данных о повторных дозах нет.
05.3 Доклинические данные по безопасности
Глобальная оценка проведенных исследований переносимости показывает, что амисульприд не имеет общих, органоспецифических, тератогенных, мутагенных и канцерогенных факторов риска. Изменения, наблюдаемые у крыс и собак при дозах ниже максимально переносимых, в условиях, предусмотренных экспериментом, либо зависят от фармакологического эффекта, либо не имеют значительной токсикологической значимости. Было подтверждено, что максимально переносимые дозы у крыс (200 мг / кг / день) и у собак (120 мг / кг / день), выраженные как AUC, соответственно в 2 и 7 раз превышают максимальные рекомендуемые дозы для людей. Канцерогенного риска, актуального для человека, у мышей (до 120 мг / кг / сутки) и крыс (до 240 мг / кг / сутки) не выявлено, что соответствует 1,5-4 для крысы., 5 раз AUC, ожидаемый для человека.
Исследования репродукции на крысах, кроликах и мышах не выявили тератогенного или эмбриотоксического потенциала препарата.
Амисульприд также лишен мутагенного потенциала (5 тестов на мутагенность).
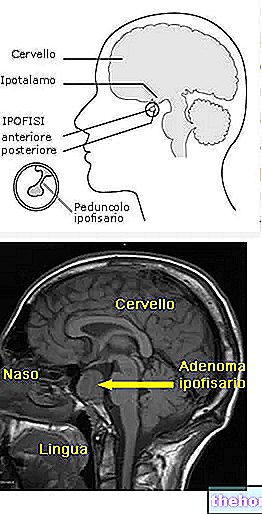
Обнаруженные эффекты связаны со всеми антидофаминовыми продуктами.Их антагонистическое действие проявляется на рецепторах аденопофиза, способствуя высвобождению пролактина, который на расстоянии влияет на ось гипоталамус-гипофиз-гонад.
06.0 ФАРМАЦЕВТИЧЕСКАЯ ИНФОРМАЦИЯ
06.1 Вспомогательные вещества
карбоксиметилкрахмал натрия (тип A), моногидрат лактозы, микрокристаллическая целлюлоза, гипромеллоза, стеарат магния.
06.2 Несовместимость
Не имеет значения.
06.3 Срок действия
3 года
06.4 Особые меры предосторожности при хранении
Это лекарство не требует особых условий хранения.
06.5 Характер непосредственной упаковки и содержимого упаковки
Коробка по 12 таблеток в непрозрачном блистере из ПВХ / алюминия.
06.6 Инструкции по эксплуатации и обращению
Никаких особых инструкций.
07.0 ДЕРЖАТЕЛЬ РАЗРЕШЕНИЯ НА МАРКЕТИНГ
Sanofi S.p.A. - Viale L. Bodio, 37 / B - Милан
08.0 НОМЕР РАЗРЕШЕНИЯ НА МАРКЕТИНГ
A.I.C. п. 027491012
09.0 ДАТА ПЕРВОГО РАЗРЕШЕНИЯ ИЛИ ПРОДЛЕНИЯ РАЗРЕШЕНИЯ
Первое разрешение: 5 марта 1993 г.
Обновление: 16 марта 2008 г.
10.0 ДАТА ПЕРЕСМОТРА ТЕКСТА
Октябрь 2014 г.